阅读:0
听报道
12月10日,美国FDA对辉瑞/BioNTech新冠疫苗BNT162b2进行独立专家评审,决定是否批准疫苗的紧急授权使用(EUA)。引人瞩目的是,本次听证会对公众开放,全球直播。
整场会议长达9小时。先由FDA和CDC代表陈述EUA相关规定、疫情流行的最新情况以及疫苗安全有效性监测、分配计划等信息。
随后是1个小时的公共听证会,由多个公益团体组织代表在线发言,包括美国公共利益科学中心(CSIP)、世界病患联盟(World Patients Alliance)、艾滋病公益团体以及女性公益团体等。
最后,疫苗研发方与FDA顾问委员会讨论,并由委员会成员投票表决。最终,委员会以17票赞成,4票反对和1票弃权的结果通过了新冠疫苗BNT162b2的全美紧急授权使用。
那么,这5张非赞成票来自谁?FDA专家们纠结的是什么?
撰文 | 小叶
图片来源:F.Hoemann
上周五(12月11日),美国食品和药品管理局(FDA)经过前一天的专家顾问委员会公开评审投票之后,正式批准辉瑞制药与德国BioNTech联合开发的新冠疫苗紧急使用授权。在此之前,这款疫苗已在上周二和周三分别获得了英国、加拿大的批准,如今成为了美国首个批准紧急使用的新冠疫苗。
不同于传统的灭活/减活病毒疫苗,这款新冠疫苗BNT162b2由美国辉瑞制药和德国BioNTech公司联合制成,属于核糖核酸(mRNA)疫苗,基于RNA编码的新冠病毒SARS-CoV-2刺突糖蛋白(S)抗原,利用脂质体包埋技术将mRNA制成纳米颗粒,将疫苗“伪装”成病毒。注射后,疫苗以胞吞方式进入细胞,在细胞内释放出纳米颗粒内的mRNA,发挥mRNA的作用。疫苗通过肌肉注射,总共接种两次,期间间隔21天,每次接种剂量为30 µg。
早在今年8月20日,辉瑞官网上就报告了BNT162b2在美国展开1期临床试验所取得的积极结果:疫苗在年轻和年长受试者身上产生了强大的免疫原性。12月10日,辉瑞在《新英格兰医学》(NEJM)上发表了后续临床试验结果的论文,在展开的跨国、安慰剂对照、观察者单盲的关键性有效试验中,总共有43548名16岁以上受试者,其中43448人接受注射,分为疫苗组(21720人)和安慰剂组(21728人)。最终疫苗组中,只有8人在第二次接种过了至少7天后确认感染新冠病毒。
简而言之,通过两次接种,BNT162b2疫苗提供了95%的有效性(置信区间为90.3-97.6)。而且,在由年龄、性别、人种、族裔、体重指数(BMI)基线和共存疾病(如基础病)限定的受试者亚组分析中,也观察到相似的疫苗有效性。
美国FDA的紧急使用授权(EUA)批准原则
11月20日,辉瑞已向美国政府提交了紧急使用授权(Emergency Use Authorization,EUA)申请。根据规定,要获得FDA的批准,需要满足以下原则:
美国卫生及公共服务部(HHS)秘书处于2020年3月27日的紧急使用授权声明中提到,EUA适用于化学、生物、放射性或者核物质会产生严重或威胁生命的疾病或环境。此处指的正是新型冠状病毒SARS-CoV-2造成的大流行病已成为严重威胁国家安全的公共卫生紧急事件。
基于所有获得的充足科学证据,包括来自严格对照试验的数据,有正当理由相信所申请药品可能有效预防、诊断或者治疗新冠病毒引起的严重或者威胁生命的疾病,或者缓解相关疾病。
在诊断、预防或者治疗上述确认的严重或者威胁生命的疾病过程中,所申请药品已知的潜在益处多于已知的潜在风险。
不存在数量充沛、已获批的有效替代药品可取代所申请药品,以用于诊断、预防或者治疗上述疾病和症状。
(来源:FDA Briefing Document Pfizer-BioNTech COVID-19 Vaccine第8页)
FDA的在线专家评审会投票环节丨来源:youtube
12月10日,就在辉瑞提交申请近三周之后,FDA组织了一场独立的专家评审会,邀请疫苗研发方辉瑞/BioNTech和疫苗及相关生物产品顾问委员会(Vaccines and Related Biological Products Advisory Committee)出席,针对BNT162b2疫苗报告进行讨论。委员会由22位传染病、儿科、免疫学、生物学、统计学、遗传学等多位领域专家组成,其中还包括一名律师代言消费者和患者权益(具体名单链接:)。
专家担心的几个问题
1 疫苗副作用
早在评审会之前,已经有多方媒体报道,四位参与三期疫苗组的志愿受试者出现了贝尔氏麻痹症(Bell's palsy),俗称面瘫,其中三名患者在10到21天内康复。FDA对此的解释是,目前没有明确证据证明面瘫和疫苗之间存在因果关系,而这4名病例的发生频率并不高于普通人群中该病的总体发生率。
但是,国立卫生研究院(NIH)的专家Michael G.Kurilla指出,新冠患者会丧失味觉和嗅觉,可能是病毒诱发的免疫反应伤害了特殊的神经细胞所致,那么对于面瘫这种明显的面部肌肉神经失常,如何能够解读为与疫苗诱导无关呢?会上FDA没有给出明晰解释。
接下来,马里兰大学药理教授Peter Doshi提出,疫苗副作用包括头疼、发烧、肌肉疼痛等,非常类似于新冠轻症患者的症状。因此他的顾虑是,是不是有可能注射疫苗7天后感染新冠而头疼发热的人误以为这是疫苗的延迟副作用,而没有去医院检测,从而低估了疫苗组的感染率?因为三期试验的样本总共超过4万人,而感染数太少,疫苗组只有8例,哪怕增加一两个人,与巨大的基数相乘,都可能足够降低疫苗的有效率。不过FDA也在会上表示:“在通过向更广泛的人群发放该疫苗之前,还是要对相关副作用进行监控。”
2 过敏人群怎么办?
此外,来自费城儿童医院的疫苗专家Paul Offit对于严重过敏反应这一问题表示了担心。据报道,英国两名参与首批疫苗接种的卫生工作者在注射后出现了严重的过敏样反应,虽然经治疗都已康复,但目前关于这两名案例没有具体数据,英国国家医疗服务体系(NHS)只是发布警告,建议对药物、食物或疫苗有严重过敏史的人不要接种该疫苗。于是Offit指出,这很可能会“劝退”上千万有严重过敏史的美国人,建议辉瑞/BioNTech需要研究一下有普通过敏史的人群,他表示:“我们需要更好的数据来彻底解决这个问题。”
3 病毒可能突变
来自匹兹堡大学的微生物和遗传学教授Patrick S.Moore教授对辉瑞报告的8例接种后依然感染新冠病毒的病例很感兴趣,他想知道,这8个人是否由于病毒突变而让疫苗失去了保护力。他问辉瑞有没有收集他们的病毒样本并测序以及抗体证据,辉瑞表示还没有进行相关分析,但在计划中。前文已经提过,mRNA疫苗编码了新冠病毒S蛋白上的特异性片段,诱导人体产生免疫力对抗病毒入侵,但如果病毒的蛋白片段突变了,那么就算产生了免疫力,也不具备抗击突变病毒的能力。
而我们已经知道,今年流行的新冠病毒已存在突变体,11月12日发表在《科学》杂志上的论文分析了D614G突变的新冠病毒变异,确认该突变的病毒株具有更高的传播能力和更快的复制速度,但幸运的是没有增强病毒致病性。因此,面对病毒突变,现有疫苗该如何应对,这个问题相当重要。不过,与其他类型疫苗相比,mRNA疫苗有一个非常灵活的优势,即使出现病毒突变,只要确定了突变性质,研发方改变相应的mRNA序列便可重新匹配病毒突变体,大大减轻了后续试验的复杂性。
4 孕产妇、未成年适用疫苗吗?
儿童、怀孕女性和哺乳期女性并不属于此次辉瑞的研究对象范围,虽然23名女性受试者在临川实验期间怀孕了,有一名对照组女性流产了,但现在要讲清楚疫苗最终是否会影响这些女性和她们的孩子,为时尚早。
至于儿童受试者,12到15岁儿童的试验才刚刚开始,而在辉瑞/BioNTech试验中,16和17岁的受试者数量只有一百多人,与此相比,其他年龄段受试者数量多达上万名,因此也有专家质疑16到18岁受试者样本数量不足以支持16岁这个疫苗接种年龄下限。
经过一天漫长的讨论,在最后投票时刻,辉瑞/BioNTech的BNT162b2疫苗获得了17票赞成,4票反对和1票弃权的结果,芝加哥医学院院长Archana Chatterjee、公共卫生专家David Kimt和NIH的Michael G.Kurilla投了反对票,在接受不同媒体采访时表示,他们反对的主要理由是前面提到的16、17岁问题,希望能够将年龄下限改为18岁。来自塔夫茨大学医学院的Cody Meissner博士也是因为同样理由而选择了弃权。而最后一位投反对票的是来自密歇根大学医学院微生物学和免疫学助理教授 Oveta Fuller,她表示这次投票意义重大,性命攸关,她本人并不是完全反对疫苗,而是希望能够看到更多临床试验数据以支持她坚定地投出同意票。总而言之,专家组投票结果表明,尽管还有可能的疑问,但该疫苗产生的益处仍会大于其风险。
据最新消息,美国从本周一(12月14日)起,各州接种点已收到新疫苗,争取在一周时间内完成疫苗的初步交付,覆盖约300万人,优先为医疗工作者、在疫情一线战斗的工作人员,和养老院居民提供首批疫苗。
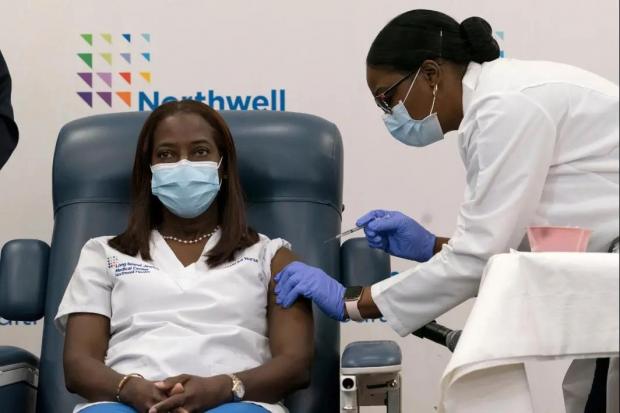
在长岛犹太医学中心工作的护士Sandra Lindsay在周一正式接种了新冠疫苗,图片来源:Mark Lennihan
参考文献
[1]
[2]
[3]
[4]
[5] FDA新冠疫苗专家评审会,他们纠结的是什么?
[6]
[7]
[8]
[9]
[10]
[11]
[12]
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 