阅读:0
听报道
原子结合成分子的各种作用中,氢键是一种特别的存在。DNA的双螺旋结构便是由氢键构成,还有诸多神奇的现象可以用氢键解释。但是,这种特别的存在自其被提出开始,就有个特别的问题,它到底属于分子间作用力还是共价键?尽管很长时间里教科书都把它定义为分子间作用力,但它也具有不可忽视的共价键特性。科学家还发现氢键在这两者之间转变,那界限到底在哪?最近一篇发表在Science的论文揭开了氢键的“隐秘行动”。现在,我们对氢键本质的了解更深了。
撰文 | 李存璞(重庆大学化学化工学院副教授)
许多有趣的现象被归结于氢键的存在:例如冰作为一种固体,其密度却比液态水要小;乙醇、乙酸的沸点比类似分子量的有机物要高得多;又如氢离子和氢氧根在溶液中的迁移比其他各类阴、阳离子更为迅捷;以及DNA中由氢键绑定的双螺旋结构保证了遗传物质相对稳定,等等。
那么氢键到底是什么?近百年来许多科学家一直致力于氢键的理论和应用,研究但一个核心问题一直未得到完美的回答,氢键与化学键如何过渡?近期, Science上刊登一篇关于氢键的论文引发热议,科学家对氢键的理解再进一步。本文将揭示氢键的一些理论与应用锁链。
氢键和其百年争论:共价键还是分子间作用力
1923年,著名化学家Gilbert Lewis在其著作Valence and the Structure of Atoms and Molecules中首次提出了氢键的概念[1] 。而从氢键概念被提出,一个问题就摆在了科学家的面前:氢键到底属于分子间作用力还是共价键?
作为元素周期表中的1号元素,H的原子核外只有一个电子,这使得当H元素与N、O、F等吸电子能力强的非金属原子形成化学键的时候,由于电子被N、O、F等元素吸引过去,导致H原子外围几乎没有电子包围——这意味着H原子核几乎裸露在外,缺少电子保护的H原子核成为孤家寡人,不像其他原子总多少有电子陪伴在身边。此时,如果H周围存在具有孤对电子(或π键等)的原子,那么H就会与孤对电子产生强烈的静电相互作用。同时,H原子核倾向于指向孤对电子所在轨道最为集中的区域,与一般的静电吸引相比又具有了一些共价键特有的轨道指向性特征,这种相互作用即为氢键。
如上所言,氢键的概念一旦提出,就会陷入其到底是 “共价键”还是“分子间作用力”的争论。而到今天,这一争论已经持续了接近100年。
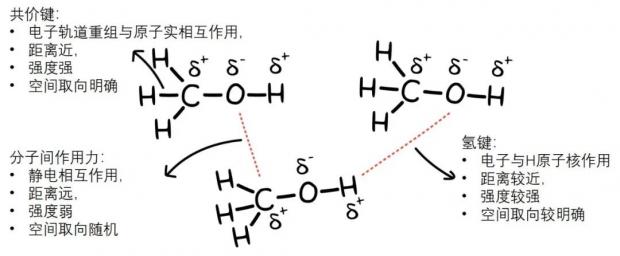
图1 共价键,分子间作用力,与氢键的特点[2]
如图1所示,共价键来自于电子轨道的重组,而轨道是有特定的空间取向的。通过电子与“原子实”(原子核与除共用电子以外的其他电子)的强相互作用,将原子相互绑定,就可以形成空间取向明确的分子或离子。另一方面,分子内部电荷分布不均会形成偶极,偶极之间的正负静电相互吸引,可以形成分子间作用力。由于不存在轨道空间约束,并且分子之间距离较远,因此分子间作用力强度弱,且没有明确的空间取向。
氢键则兼具共价键与分子间作用力的特点:它虽然来源于电子和H原子核的相互作用,却没有明确的轨道重组;同时,H原子核往往与孤对电子在空间中指向明确,以形成类似共价键轨道最大重叠的效果:而这也导致了冰的密度比水小(图2)。
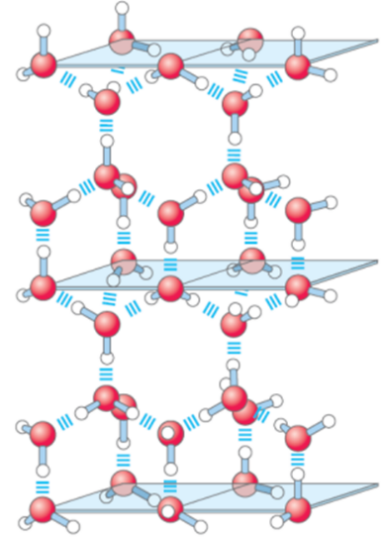
图2 在冰中,H为了充分靠近O的孤对电子,形成了具有特定空间取向的氢键[3],在分子间产生大量空隙,使固体冰的密度反而比液态水小。
如上所述,定义氢键并非易事。即使在国际上最为权威的“国际应用与纯粹化学联合会,IUPAC”关于氢键的定义中,也对其相互作用的来源略显含糊其辞[4] :
Hydrogen Bond:A form of association between an electronegative atom and a hydrogen atom attached to a second, relatively electronegative atom. It is best considered as an electrostatic interaction, heightened by the small size of hydrogen, which permits proximity of the interacting dipoles or charges. Both electronegative atoms are usually (but not necessarily) from the first row of the Periodic Table, i.e. N, O or F.
氢键:一种产生于一个电负性大的原子与氢原子之间的相互作用,这一氢原子需要某一连接至另一电负性较大的原子上。氢键最好被认为是静电相互作用,具有较小尺寸的H原子提升了偶极或电荷的相互作用。前述的两种电负性大的原子一般而言(但不是必须的)位于元素周期表的第二行,例如N,O,或者F等。
因此,氢键体系中是否含有、以及含有多少共价键的成分,一直是学界研究的热点[5]。了解氢键,不仅有物理化学意义,更有利于人们系统认识宇宙与生命,开发新的应用体系。
氢键是生命之源:从有序排列到低势垒氢键
氢键的争论有着重要的意义。在公众的认知当中,水当然是生命之源,但进一步思考,似乎氢键是更本质的生命之源。生命起源于水,在生命形成之初,地球温度波动剧烈,在温度低于零下时,水面会结冰隔绝空气温度,让水中的生命不至被冻死。如果冰的密度比水大,那么结成的冰块会沉于水底,其保护作用自然荡然无存;当环境温度迅速升高时,强度较大的氢键要吸收大量热量才被破坏,导致水的比热容很大,从而可以吸收环境热量来阻止水温剧烈变化。DNA的双螺旋结构通过氢键进行绑定,使生命体的遗传物质保持稳定。在遗传物质转录、翻译的过程,同样有氢键参与来保证物质合成的准确性。
前述的关于氢键的百年争论,在生命体中的酶催化过程中具有重要的讨论意义。酶催化似乎异常神奇,可以在温和的温度、特定的pH值和水体系实现高效率的催化反应。许多生物教科书将酶的作用归结于其可以使底物分子以特定的构象嵌入,从而诱使反应发生:但从能量角度而言,构象上的些许优势远不能解释酶的催化作用。那要靠什么解答呢?
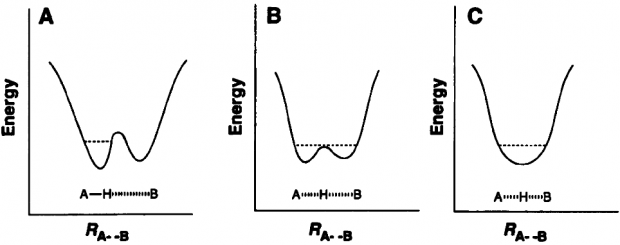
图3 几种氢键状态的势垒图。氢键体系会倾向于带到势垒的谷底,两个谷底之间的小山峰越高,则H越难在A、B二者之间进行穿梭。(A)双阱氢键,(B)低势垒氢键,(C)单阱氢键
没错,又是氢键。1994年,美国威斯康辛大学和明尼苏达大学的W. W. Cleland与Maurice M. Kreevoy[6] ,与威斯康辛大学的PA Frey[7],在同一期Science期刊上发表了两篇论文,认为一种“低势垒氢键(Low-barrier hydrogen bond)”对酶催化反应至关重要。
如图3所示,一般情况下,在氢键中,H与其中一个原子A形成共价键,与另一个原子B距离较远,形成传统意义上的更接近分子间作用力的氢键;而当A、B二者的距离逐渐接近(比如A、B均为O原子,O-O距离小于0.25 nm时),H可以在A、B两个原子之间自由移动,此时难以明确区分H与A、B之间何者为共价键,何者为分子间作用力:即成为图3(B)所展示的低势垒氢键。在酶催化的过程中,参与反应的底物或过渡态可以与酶形成低势垒氢键,低势垒氢键相当稳定:这意味着底物在与催化剂形成低势垒氢键的过程中,将释放出许多能量(10到20 kcal/mol),这部分能量恰好被用来活化底物,使催化反应得以在温和的条件下迅速进行。与此同时,低势垒氢键中A···H···B距离很近,也可以阻止其他分子的孤对电子靠近H原子,进一步提高了反应效率。
补齐最后一环:超瞬态光谱找到单阱氢键
在低势垒氢键中,氢键的“共价键”与“分子间作用力”这两种特性之间的界限被模糊,而随着A、B二者之间的距离更加接近,氢键的分子间作用力特征彻底消亡,进一步形成如图3(C)所示的单阱氢键,H原子同时与A、B两个原子形成共价键:即三中心共价键。人们之前相信这种单阱氢键可能存在于HF2-和[HO···HOH]-这两种离子中,而这个“可能”在2021年1月8日出版的Science的一篇文章中被成功地拿掉了[8]。
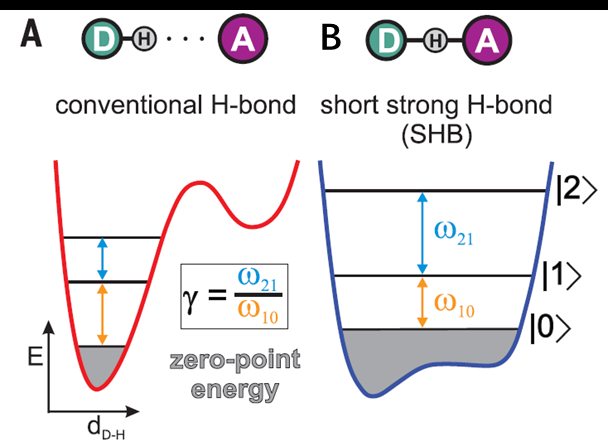
图4 (A)传统双阱氢键,(B)单阱氢键(短强氢键,SHB)
美国芝加哥大学的Andrei Tokmakoff与埃默里大学的合作者们进行了这一创造性的研究。如图4所示,作者注意到了传统双阱氢键与单阱氢键(作者称为为短强氢键,SHB)在分子光谱上存在一个重要的区别:传统双阱氢键更接近分子间作用力,其能级差随着能级的升高而逐渐缩小;而SHB更接近共价键,其能级差随着能级的升高而逐渐增加。化学家提出通过分子光谱学的方法来观测,寻找HF2-这一离子的能级差,就有机会验证到底HF2-离子中的氢键是不是人们之前认为的单阱氢键。
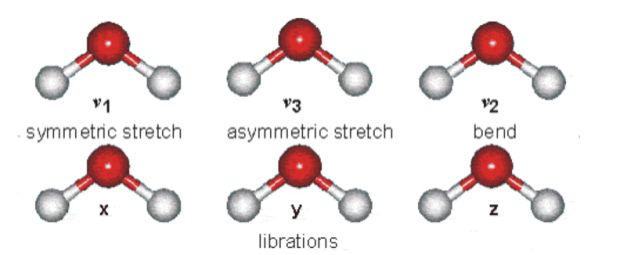
图5 分子中共价键的各种振动
但这很难。如图5所示,分子中共价键、氢键等都是广场舞大师,无时无刻不在进行各种各样的振动。它们振动的能量很低,在红外线波长范围内。传统的红外吸收光谱可以通过探测分子振动来研究共价键,但在SHB的研究中,是要观测找到振动的能级差规律。这意味着需要在很短的时间内(本研究为25飞秒,1飞秒为一千万亿分之一秒),连续用两种红外光激发分子,并记录结果。这类红外光谱仪被称为“超瞬态红外光谱仪”,作者团队是世界上为数不多可以使用到这种大型仪器的研究组,通过精妙的实验设计,他们成功证明了HF2-的能级差确实随着能级的升高而增大:HF2-中的氢键已经彻底成为一种三中心原子共价键。也就是说,氢键变成了一种新的化学键形式。
研究并没有到此为止。研究团队还进行了理论计算,通过量子化学的方法找到了传统双阱氢键、低势垒氢键与单阱氢键之间的转化界限。如图6所示,对于HF2-离子而言,在F与F原子距离在约0.248 nm时,[F-H···F]-开始具有低势垒氢键的特征;而当F与F原子距离进一步缩小到约0.238 nm时,[F-H···F]-则开始具有SBH特性;在0.23 nm则完全转化为结构对称的[F···H···F]-单阱氢键(图6(B))。
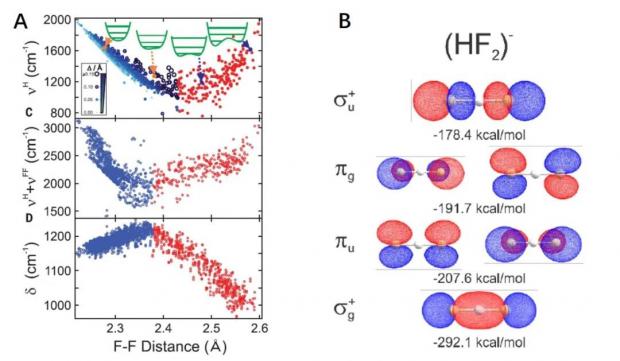
图6(A)双阱氢键、低势垒氢键与单阱氢键的转化;(B)具有对称单阱氢键的[F···H···F]-的离子结构与分子轨道
新发现具有实际意义
这项研究用昂贵的超瞬态光谱,似乎只是为了证明单阱氢键的存在,并没有除了理论认识拓展之外的其他意义。但就实验本身而言,新发现又为我们开启了许多新问题等待回答:比如环境起到了什么作用,分子运动如何触发了转化,等等。事实上,在应用领域,这一发现有更加深远的意义:比如在催化领域模拟低势垒氢键或单阱氢键,有望在温和条件下催化各类反应高
效进行;又比如在能源领域的燃料电池中,模拟单阱氢键提升氢离子或氢氧根离子的传输效率;又或者通过观测星际光谱,研究地外世界的各类化学反应……
况且,就算一时没有想到特别重要的应用意义,弄清楚氢键从分子间作用力到共价键的转变过程,给氢键的百年争论划上一个休止符,不也很有趣么?
参考文献
[1] Lewis G N. Valence and the Structure of Atoms and Molecules[M]. Chemical Catalog Company, Incorporated, 1923.
[2] :in-in-states-of-matter/xfbb6cb8fc2bd00c8:in-in-intermolecular-forces/a/intramolecular-and-intermolecular-forces
[3]
[4]
[5] Gilli G, Gilli P. The nature of the hydrogen bond: outline of a comprehensive hydrogen bond theory[M]. Oxford University Press, 2009.
[6] Cleland W W, Kreevoy M M. Low-barrier hydrogen bonds and enzymic catalysis[J]. Science, 1994, 264(5167): 1887-1890.
[7] Frey P A, Whitt S A, Tobin J B. A low-barrier hydrogen bond in the catalytic triad of serine proteases[J]. Science, 1994, 264(5167): 1927-1930.
[8] Dereka B, Yu Q, Lewis N H C, et al. Crossover from hydrogen to chemical bonding[J]. Science, 2021, 371(6525): 160-164.
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 