绿色荧光蛋白能够通过自身催化形成生色团并在蓝光或紫外光激发下发出绿色荧光,通过基因工程与其它蛋白融合,它可以让不可见的蛋白质成为可见,因此在过去的二十多年里成为生物学家和医学科学家研究细胞内各类生物化学过程的指路星,可以说是生物学研究的重要工具。对其的原创性发现和后来的重要发展斩获了2008年诺贝尔化学奖,投身其中的诸位科学家的探索之旅则堪称科学史上的一段传奇佳话。
撰文 | 徐亦迅
生命科学史的发展脉络是从容易观测的宏观层面(比如物种分类和大体解剖学)进入需要仪器才能观测的微观层面(比如显微解剖学研究的组织和细胞)。十七世纪荷兰科学家列文虎克 (Antonie van Leeuwenhoek) 用他改进的光学显微镜首先观察并描述了单细胞生物,就是生物学历史上的一个分水岭。在显微镜的帮助下,生物学家们逐渐观察到了以前都不知其存在的细菌、细胞、细胞器等微观研究对象。这样的还原论研究一旦达到分子水平,就连电子显微镜也很难让我们直接观测蛋白质等生物大分子在活体细胞中的表达和定位。从维多利亚多管发光水母 (Aequorea victoria,下文简称发光水母或水母) 中分离的绿色荧光蛋白 (Green Fluorescent Protein, GFP),让曾经不可见的蛋白质成为可见,在过去的二十多年里成为生物学家和医学科学家研究细胞内各类生物化学过程的指路星。本文要讲述的就是几位科学家的故事,他们为GFP引发的生物学革命做出了重要贡献。
生物发光现象的早期研究
GFP发现的缘起与生物发光现象(bioluminescence)密不可分,因此我们首先要介绍一下不同类型的低温发光(luminescence)。

图1:各种类型的低温发光现象及其激发模式
火是人类历史上最重要的发明,与它相联的白炽发光(incandescence)通常定义为物体被加热到高温时发出的可见光。低温发光则是一种由不与环境处于热平衡的激发态化学组分自发放射的可见光。两千五百多年前的古希腊科学家亚里士多德,就在《论颜色》一书中写道:“有些不是火而且与火的产生无关的物体似乎可以自然发光”。这意味着人类很早就意识到白炽发光和低温发光的重要区别:白炽灯泡在照明时效率不高,只能把一小部分电能转化为光能,而其余能量以热的形式被耗散;而生物发光则是一种高效的化学反应,在将化学能转化为光能的过程中几乎不产生热,因此也称为“冷光”。
按照不同的激发模式,我们可以把低温发光分为光致发光 (photoluminescence)、电致发光 (electroluminescence)、化学发光 (chemiluminescence,生物发光是一种特殊的化学发光) 等很多种类 (图1)。最为常见的光致发光是荧光 (fluorescence) 和磷光 (phosphorescence) ,请读者们特别注意荧光与生物发光的区别。
自然界中最为常见的一种生物发光现象就是萤火虫。每到夏日的夜晚,萤火虫在草丛里点点飞舞,构筑成奇幻的美景。唐代大诗人李白曾作《咏萤火》一诗:“雨打灯难灭,风吹色更明。若飞天上去,定作月边星”。

图2:生物发光的研究肇始于科学家们对萤火虫现象的着迷
除了萤火虫,自然界还有很多物种有低温发光的能力,其中包括细菌、原生动物、真菌、水母、乌贼等。科学家们很早就对生物发光现象有深入研究的好奇之心,但一直缺乏有效的科研手段。直到1667年,英国化学家波义耳 (Robert Boyle) 用气泵将钟罩内的空气抽去,发现里面的真菌不再发光。当他再将空气导入时,真菌的生物发光能力恢复。在十七世纪的化学界,人们对空气的成分还一无所知。只有等到1770年代,瑞典化学家舍勒 (Carl Wilhelm Scheele) 和英国化学家普利斯特里 (Joseph Priestley) 独立发现了最终由法国化学家拉瓦锡 (Antoine Lavoisier) 阐明的氧气,生物发光对氧气的依赖性终于浮出水面。
又经历了一个多世纪的徘徊不前,生物发光的化学机理探索由法国生理学教授杜勃瓦 (Raphael Dubois) 带来新的转折点。在1885年的一个实验中,杜勃瓦先用冷水将叩头虫 (Pyrophorus) 的发光组织在试管里匀浆,发现抽提物在短暂发光后变暗。他用沸水取得的组织抽提物则完全不发光,令他惊讶的是,当冷却的热水抽提物被加入已经停止发光的冷水抽提物时,混合物居然再度发光 (图3) 。若想让冷水抽提物持续发光,杜勃瓦就需要不断补加冷却的热水抽提物。
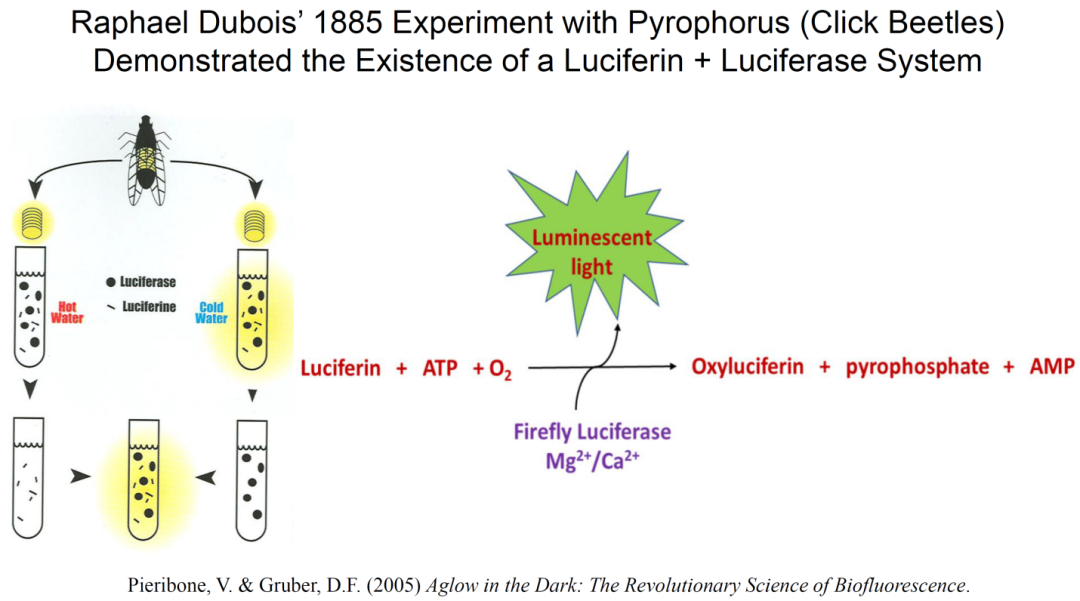
图3:杜勃瓦1885年首先发现“萤光素-萤光素酶”生物发光原理的著名实验 [Pieribone, V. & Gruber, D.F. (2005) Aglow in the Dark: The Revolutionary Science of Biofluorescence, Belknap Harvard.]
杜勃瓦随后在其它包括萤火虫在内的发光生物中得到了相似的实验结果,于是他得出了两个重要结论:(1) 生物发光的反应除了氧气之外,至少还需要两个化学组分;(2) 发光反应中的“燃料”组分可以耐受沸水的高温,而“点燃剂”或催化剂不耐热。杜勃瓦决定借用来自罗马神话的拉丁词Lucifer (字面意思是“光之使者”) 来命名这两个组分:不耐热的催化剂名为萤光素酶 (luciferase),而耐热的小分子则名为萤光素 (法语:luciferine,英语:luciferin)。
很多生物学家的后续研究表明:对于很多发光物种而言,萤光素酶有不同的蛋白序列,而萤光素也呈现多样化的有机小分子结构,但“萤光素-萤光素酶”的生物发光原理都是成立的。生物发光研究者的目标也就可以具体化,选择一个感兴趣的发光物种,用生物化学手段来分离纯化不同的萤光素和萤光素酶。通过对萤火虫发光系统的深入研究,科学家们很快又发现在氧气、萤光素、萤光素酶之外,ATP和Mg2+离子也是必要条件 (图3)。
生物发光对于陆生物种而言并不常见,而在深海里却有超过90%的海洋生物能够发光。从海平面每往下75米,阳光的强度就要减弱10倍。在阳光无法到达的深度以下,会发光的动物在寻找食物、逃避敌害和吸引配偶上拥有明显的优势。在大致阐明萤火虫的发光机理之后,很多科学家就把目光转向海洋发光生物,其中最有名的就是美国普林斯顿大学开宗立派的哈维教授 (E. Newton Harvey)。
1916年,时年28岁的哈维携夫人前往日本蜜月旅行。三崎临海实验所附近的海域适合两人在夜间游泳,哈维在畅游之余迷上了一种叫做希氏弯喉海萤 (Vargula hilgendorfii, 曾用属名Cypridina) 的发光海洋生物。海萤在采集和抽干后可以长期保存,用水濡湿后又能发光,因此被哈维视为用生物化学手段研究生物发光的最佳实验材料。哈维实验室发现海萤的发光系统比萤火虫要简单,只需萤光素、萤光素酶、氧气,而无需ATP和Mg2+离子 (图4)。但哈维团队在部分纯化了海萤的萤光素之后,努力钻研了二十多年也无法获得其结晶。而没有高纯度的萤光素,他们就无法通过确定其分子结构来深入研究海萤发光的化学机理。
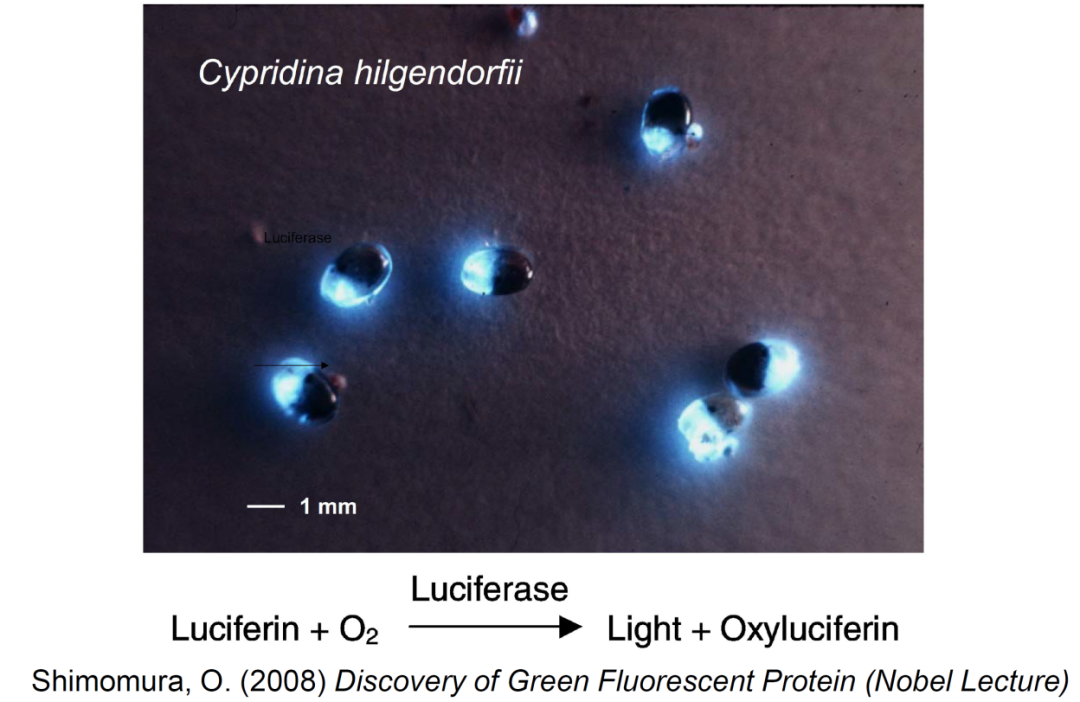
图4:希氏弯喉海萤的萤光素-萤光素酶生物发光系统
下村修结晶纯化海萤的萤光素
海萤的萤光素难以被完全纯化,为GFP故事的第一位主角下村修 (Osamu Shimomura) 登上历史舞台提供了契机。下村修“人生的起跑线”和同样出生于1928年的沃森 (James Watson) 相比,简直就是后者的“阴性对照” (negative control) ,充满了崎岖与坎坷。由于父亲是军人,下村修主要由居住在长崎县谏早市的祖母抚养长大。1941年4月,刚升入谏早中学初一的下村修,和他的同学们都要遵照日本政府在当年3月修订的《国家总动员法》参加军训。1944年秋季升入初三后,学校又开始经常性取消课程,要求学生们去大村市的一家军用飞机修理厂义务劳动。美军很快盯上了这家军工厂,出动了二十多架B-29轰炸机将其彻底摧毁,下村修有好几位跑得不够快的同学不幸遇难。
正所谓“福无双至,祸不单行”。1945年8月9日早上10点57分,长崎市又不幸迎来了美军的第二颗原子弹。当时下村修和几位同学正在长崎市中心15公里外的另一家军工厂里工作,熟悉的空袭警报刚拉响时,他们还处变不惊地走出厂房爬上附近一个小山丘观望。下村修看到一架B-29轰炸机飞往南边市中心方向,空投下三个载物降落伞。事后才知道,这是在他们没看到的原子弹投放与最后爆炸的间隔期内,“大艺术家”号飞机投放的三个无线电高空测候器。此时大家还误以为这次轰炸可能威胁不大,于是决定回到厂房试图继续工作。刚一坐下,窗外袭来的强烈闪光就让同学们暂时失明半分钟,随后是一声巨响和气压的骤变 …… 军工厂和长崎之间的距离显然是下村修和小伙伴们能够劫后余生的关键。
第二次世界大战虽然随着日本投降而宣告结束,年仅17岁的下村修依然看不到任何未来的曙光。谏早中学很多师生在原子弹爆炸时罹难,所有的学生档案都被炸毁,因此近几届的初中生都不能正常毕业。下村修连续两年报考高中 (日语:高等学校) 或技术高校 (日语:高等工业学校),都因没法提供初中成绩而失利。直到1948年4月,长崎医学院的师生由于在原子弹爆炸时伤亡惨重,重建的迫切需要才使下村修被他并不感兴趣的药学院录取 (图5),这也是他当时接受高等教育的唯一机会。

图5:1948年长崎药学院的临时校园
刚刚在一片废墟上重建的长崎医学院教学资源极度匮乏,原先的20名教授中有12位在原子弹爆炸时遇难,4位受了重伤。药学院课程的教学任务大都只能由经验不足的讲师们来担当。由于教学经费的限制,下村修在三年本科期间以分析化学和物理化学方面的训练为主,只有少数机会学习有机化学知识或进行有机合成实验。下村修的分析化学课老师安永峻五 (Shungo Yasunaga) 很快发现这位学生出众的动手能力,特别准许他把一些试剂带回家去钻研利用毛细管色谱的分离纯化。这项研究最终让下村修在1953年与安永教授联名用日语发表了他学术生涯的第一篇论文。
1951年3月,下村修以总成绩全班第一从长崎药学院毕业,并向武田药品公司递交了入职申请,但一位面试官坦率地指出他的个性不适合在公司环境里发展。安永教授对下村修及时伸以援手,邀请他留校担任分析化学课助教。下村修对自己将来的人生并没有刻意规划,只要有一份工作就专心去做,也从未想过报考研究生院以获得更高的学位。安永教授在下村修工作四年之后,为他争取到了一个带薪去其他院校学术访问一年的机会。
作为下村修职业生涯里的第一位贵人,安永教授还主动帮助他寻找合适的访学实验室。安永在日本化学界的人脉主要在名古屋大学,他认为专攻生物化学的江上不二夫教授 (Fujio Egami) 是开阔下村修科研视野的最佳人选。日本的电话通讯系统在战后多年也未能全面恢复,安永教授只能亲自带着下村修,从长崎坐十几个小时的火车来到名古屋,没想到江上教授那几天外出参加学术会议而未得一见。偶然事件改变历史发展轨迹的例子比比皆是,如果当天下村修见到了江上教授而顺利进入他的实验室,那么读者朋友们此刻恐怕就不会读到这个有趣的故事。两人转而去拜访有机化学家平田义正教授 (Yoshimasa Hirata),简短谈话几分钟后,平田教授就欢迎下村修随时到他实验室来做访问学生。
1955年4月,平田教授指着一个真空干燥器对刚来实验室报到的下村修说:“这里面有大量已被抽干的希氏弯喉海萤,这种海洋动物通过萤光素和萤光素酶的相互作用而发光。海萤的萤光素很不稳定,一遇到氧气就会降解。你是否愿意尝试一下这个萤光素的纯化和结晶?”下村修深知这个高难度的课题不适合平田教授的研究生们,而身为访问学生的他没有攻读学位的负担,决心以一种“初生牛犊”的放松心态大胆尝试。早在1935年,哈维实验室的安德森 (Rubert Anderson) 发明了两步抽提法,可以将这个很不稳定的萤光素部分纯化2000倍左右,并通过吸收光谱推测出其分子结构中有氨基酸的组分。下村修在此基础上推算,想要得到结晶纯度的萤光素至少需要500克抽干海萤作为起始原料,这是哈维实验室用量的10倍,也就需要他搭建一个巨大的索氏提取器 (图6左)。
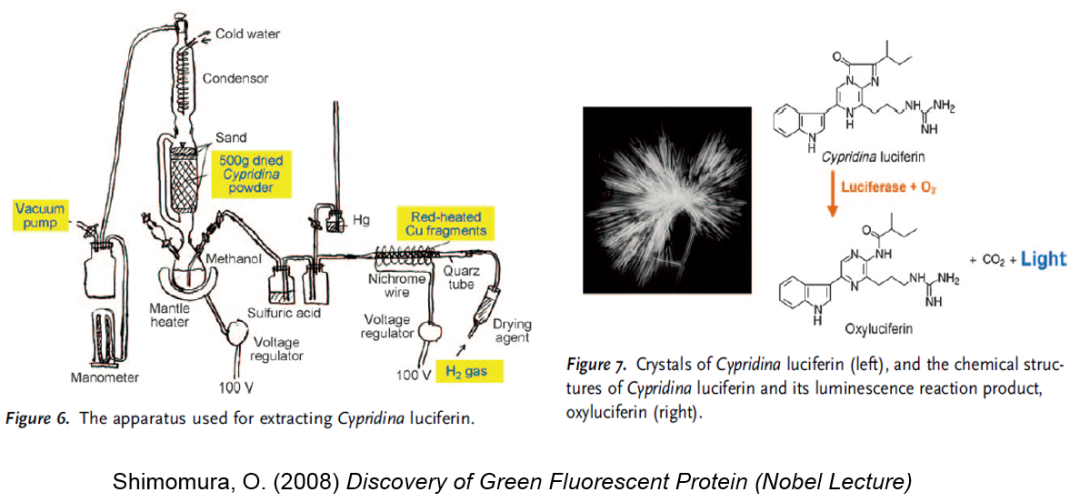
图6:下村修在1956年经过十个月的艰苦努力完成海萤的萤光素纯化与结晶 (黑白照片无法显示晶体实际的深红色)
下村修在艰辛的科研探索过程中发现,用氮气或者惰性气体都不足以消除抽提系统中痕量氧气对萤光素的消耗。他必须往系统中通入氢气,这样痕量氧气就会被转化为液态水而被硫酸吸收。化学工作者无人不知对氢气操作不当就会引发爆炸事故,因此平田实验室其他成员在下村修紧张实验时都会与他保持相当的距离。氢气的使用虽然为下村修带来了突破性进展,但用各种方法试图结晶总是失败。每次尝试结晶前的抽提物制备,都需要他在极少睡眠的状态下连续工作一周,失败后的抽提物在报废前只能做一些简单的组分分析。不离不弃的下村修平均每个月要这样辛苦一周,直到1956年2月的一个晚上,看来又要面临一次失败。他在回家前决定在将要报废的抽提物中加入等体积的浓盐酸,等黄色的溶液变为暗红色后放在实验台上过夜,准备第二天再尝试检测其中有哪几个氨基酸。
下村修早上回到实验室却发现溶液由暗红色变为无色,第一感以为是盐酸导致萤光素水解后的结果。随后他在试管底部发现了少量黑色沉淀物,通过显微镜细看,居然是红色的针状晶体 (图6右)!这些晶体通过与海萤的萤光素酶提取液混合后可以发光,正式宣告萤光素结晶取得成功。事后回看,浓盐酸促成萤光素的结晶在其结构未知时只能来自意外发现,并且当晚平田实验室的煤气炉关闭,溶液在室温持续下降时过夜对结晶过程的帮助也不容忽视。
“苦心人,天不负”,下村修十个月的科研拼搏取得了出乎意料的突破,他在名古屋大学的学术访问也被平田教授延期一年,确保其第一篇英语学术论文在1957年顺利发表。哈维教授的衣钵传人约翰逊 (Frank Johnson) 此时已是美国普林斯顿大学的正教授,他在读到这篇论文后不由惊叹一个困扰了哈维学派二十多年的难题,居然被一位只有本科学历的年轻日本学者解决!这次难得的成功为下村修带来了职业生涯的一个重要机遇:1959年春天,他回到长崎药学院不久就收到约翰逊教授的邀请信,定于下一年秋季前往普林斯顿大学担任为期三年的访问学者。
下村修与发光水母和星期五港的不解之缘
下村修于1960年9月抵达普林斯顿大学。约翰逊教授告诉他,本实验室现在最感兴趣的研究对象是发光水母,希望他借着研究海萤发光的成功势头,在水母发光的机理研究上取得突破 (图7)。想要获得足够的实验材料,当时全美只有华盛顿州圣胡安群岛 (San Juan Islands) 上的星期五港 (Friday Harbor) 海域,每年夏天会有大量的水母可以捕捞。

图7 改编自:Chalfie, M. (2008) Nobel Lecture.
从1961年开始,约翰逊几乎每年夏天都要与研究组骨干成员自带仪器,从普林斯顿长途开车七天来到星期五港采集水母。为了用生化手段研究水母发光,他们先要手工切割大量打捞上来的水母伞膜 (图8),利用当地华盛顿大学分校的实验室条件,把伞膜边缘发光器官的挤出液 (squeezates) 冷冻保存。
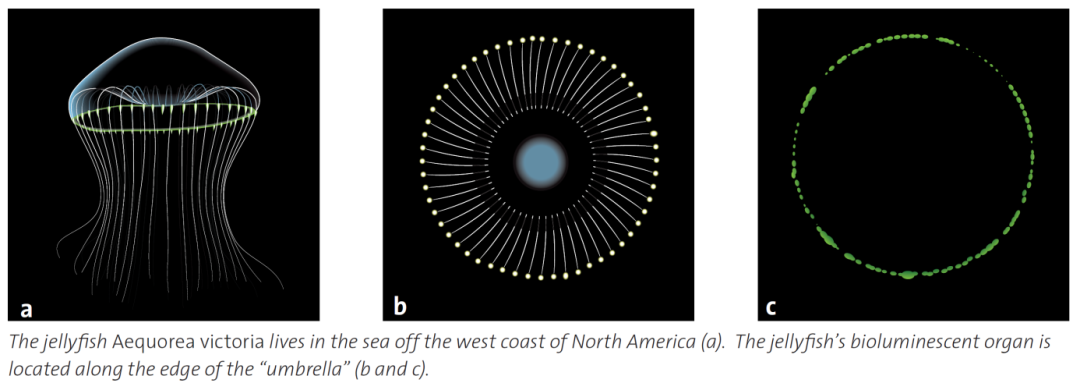
图8:分布在北美洲西岸的维多利亚多管发光水母及其伞膜边缘的生物发光器官。来源:
下村修和约翰逊首次上岛的第一周研究很不顺利,他们沿着杜勃瓦的“萤光素-萤光素酶”思路总是无法分离出耐热和不耐热的两个组分。此时年轻的下村修觉得不必拘泥于杜勃瓦理论,可以在没有任何假设的前提下分离水母的发光物质。但约翰逊基于多年来杜勃瓦理论在多个发光物种被毫无例外地反复验证,不愿轻易放弃它而改换思路。师生二人由于坚持己见不让步而只能在一个实验桌的两端各自为阵,气氛相当紧张而尴尬。
下村修每当研究受阻时喜欢暂停手中的实验,寻找安静之处冥思新的想法。在星期五港可以通过小船前往那些无人的僻静水域,下村修连续几天划船出海,然后独自一人躺在船里闭目思考,他有好几次在小船随着风浪漂移时进入梦乡。某天下午当下村修在船中小睡醒来后突然有了灵感:就算水母的生物发光与萤光素和萤光素酶无关,但很可能还是会需要蛋白质。而蛋白质的活性对pH值敏感,能否通过调控溶液的pH值来可逆抑制水母的发光?下村修此时非常激动,赶快用力划船返回实验室,制备了几种不同pH值的缓冲液。当pH值分别是7,6,5的时候,水母抽提液都还能发出弱光;而当pH值被调到4的时候,溶液的弱光消失,提示酸性可以抑制发光物质!当他用碳酸氢钠把pH值调回中性时,弱光再次出现,说明酸性的抑制作用果然可逆 (图9)。

图9 来源:Shimomura, O. (2008) Nobel Lecture
这个进展让下村修无比振奋,但他还是对抽提液为何只发弱光感到困惑。此时难以捉摸的机遇在下村修职业生涯中第二次光顾了他这个“有准备的头脑”。1961年的一个仲夏之夜,独自工作到很晚的下村修身心疲惫,觉得中和了酸性的水母抽提液已没有多大用处,就将其倒入水槽后收工。关灯出门前他下意识回望了一眼,惊讶地看到刚倒入抽提液不久的水槽中发出闪亮的蓝光!善于思考的下村修开始分析这一现象背后的原因,在第二天他注意到旁边一个养鱼缸的海水也流入同一个水槽,于是假设海水中的某种物质把水母抽提液的弱光激发成了强光。沿着这个思路,下村修用“加减法”逐个排查海水中浓度较高的离子组分,很快发现钙离子可以在瞬间激发水母抽提液中的发光蛋白。约翰逊教授在见证了下村修发现钙离子作用的突破之后,开始对他的科研能力彻底放心。
了解钙离子的发光引发剂作用后,下村修不再需要调控酸碱度,而只需在抽提液中先加入著名的钙离子螯合剂EDTA,就能更加有效地可逆抑制发光蛋白,保证在进一步的分离纯化过程中,目标蛋白不会因为发光而被损耗。1961年8月底之前,约翰逊团队总共采集了1万多只水母,制成含有EDTA的粗提液后用干冰冷冻,全部带回普林斯顿后再开始系统的蛋白纯化工作 (图9)。几个月后,他们就纯化得到两个蛋白:其中浓度较高的蛋白产量约为5毫克,被命名为水母素 (Aequorin),这就是能被钙离子激活的发光蛋白;先于水母素从液相色谱柱上洗脱的另一个“副产品”,在阳光下显出暗绿色,被命名为绿色蛋白( Green Protein, GP;后来改名为GFP)。没想到这个彼时不起眼的“副产品”,却最终成为生物科学史上的一个重量级角色。
随着下村修纯化水母发光蛋白的几篇论文先后发表,他在约翰逊实验室的三年访学可谓成果颇丰。1963年,回到日本的下村修被名古屋大学聘为水科学的助理教授,但他在两年后意识到,自己还是更愿意回到约翰逊实验室进一步研究水母的发光机理。经过几年的不懈努力,下村修彻底阐明了水母素在钙离子调控下的发光机理 (图10)。脱辅水母素 (Apoaequorin) 需要在有氧条件下与腔肠素 (Coelenterazine) 这个小分子辅因子共价结合,形成具有生物发光能力的水母素稳定中间体。而这个共价键居然是过氧化桥,一种“内蕴的氧气” (intrinsic oxygen)!这个过氧化键在钙离子的激发下可以快速断裂,在形成二氧化碳的同时发出闪亮的蓝光 (图10)。
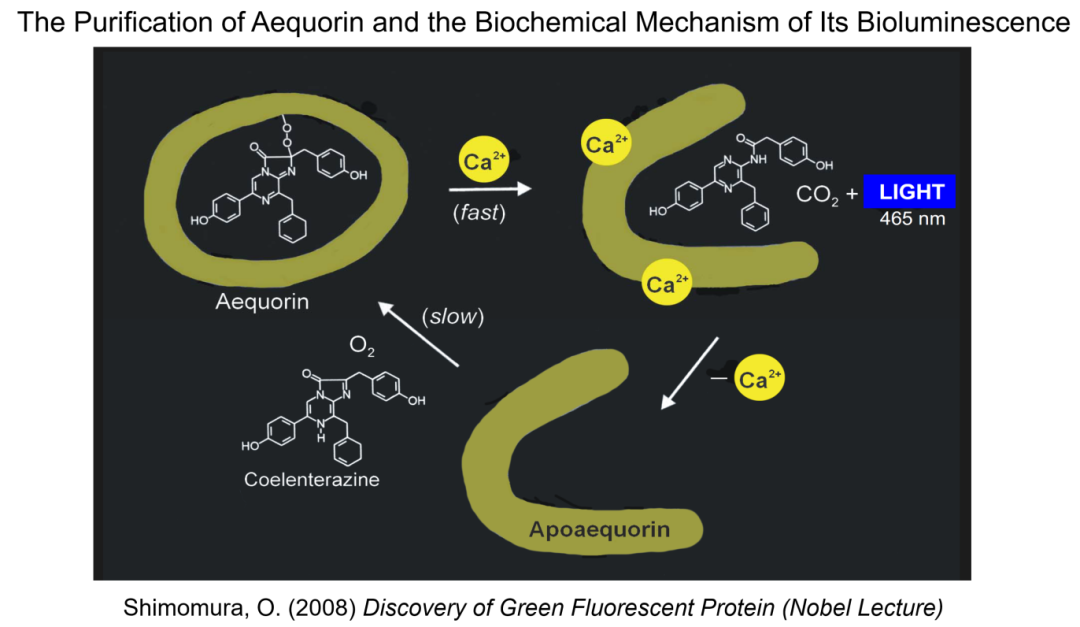
图10:水母素发光的生物化学机理
更为引人入胜的是,腔肠素在化学结构上与海萤的萤光素 (下村修的成名之作) 有显见的相似性,它其实是一种“内蕴的萤光素” (图11)。下村修此时恍然大悟,终于明白为何1961年夏天沿着传统的杜勃瓦理论思路研究水母会碰壁,这真是“终点又回到起点,到现在我才发觉”。我们在研究这段有趣的科学史时,不由想起了著名遗传学家杜布赞斯基 (Theodosius Dobzhansky) 的名言:“没有演化论之光,生物学的一切都将无法理解” (Nothing in Biology Makes Sense Except in the Light of Evolution)。从萤火虫发光需要五个组分 (萤光素,萤光素酶,氧气,ATP和Mg2+离子),到海萤发光只需三个组分 (萤光素,萤光素酶,氧气),再到水母素这个发光蛋白把内蕴的萤光素和氧气像充电电池那样隐藏在分子当中,自然选择下的生物演化真是“八仙过海,各显神通”!
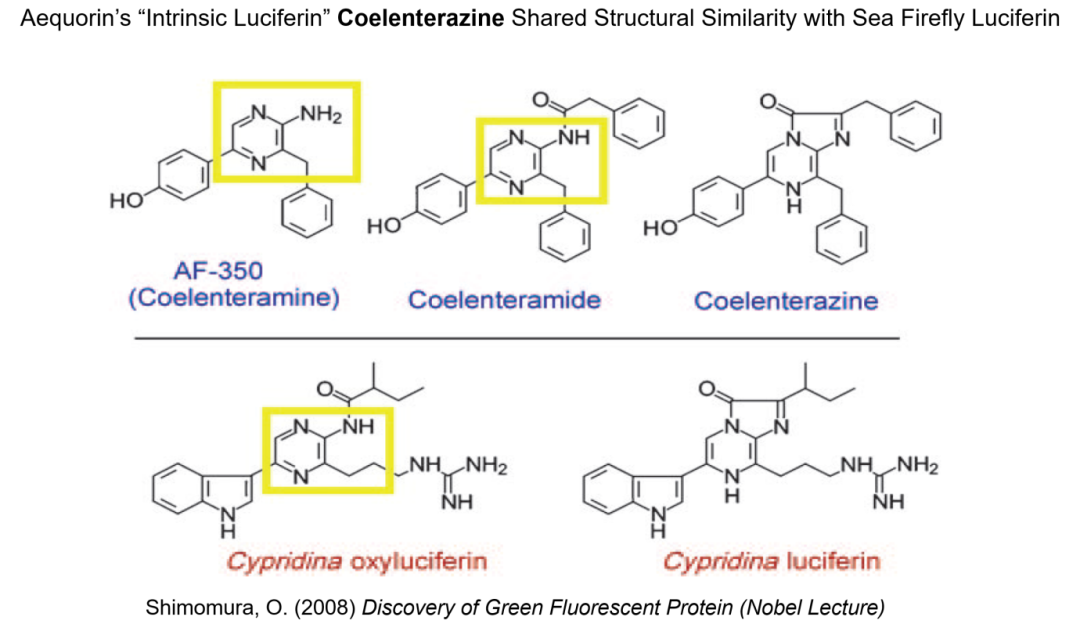
图11:水母素的辅因子腔肠素是一种“内蕴萤光素”
在探明水母素发光的生物化学机理后,下村修并没有忘记那个绿色蛋白副产品GFP。只是GFP在水母中的含量偏低,根据他的初步估算,大概需要打捞几十万个水母才能有足够的原材料来纯化并结晶GFP。下村修对科研的执着让他天生具有愚公移山的精神,为了进一步研究GFP,他不惜每年夏天长途跋涉去一次星期五港,年复一年直到采集了足够的原材料为止。
江涛演唱的歌曲《愚公移山》
从1962年到1974年,十二年光阴弹指一挥间,下村修在约翰逊实验室终于纯化了足够量并成功获得GFP的绿色结晶 (图12)。而想要进一步研究GFP的发光机理,下村修预计需要消耗100毫克的纯GFP蛋白,而每年夏天打捞4万多只水母也只能获得20毫克GFP。于是他又通过连续五年的积累,直到1979年才初步鉴定了GFP的荧光生色团 (图12和图13)。1977年,年近70岁的约翰逊教授决定退休,而普林斯顿大学无意挽留独立获得科研经费能力有限的下村修。约翰逊只能说服生物系领导给下村修足够的时间找工作,并提供一个在主校园几英里外的临时实验室,GFP生色团的研究工作就由他在职业前途未卜的情况下独自完成。
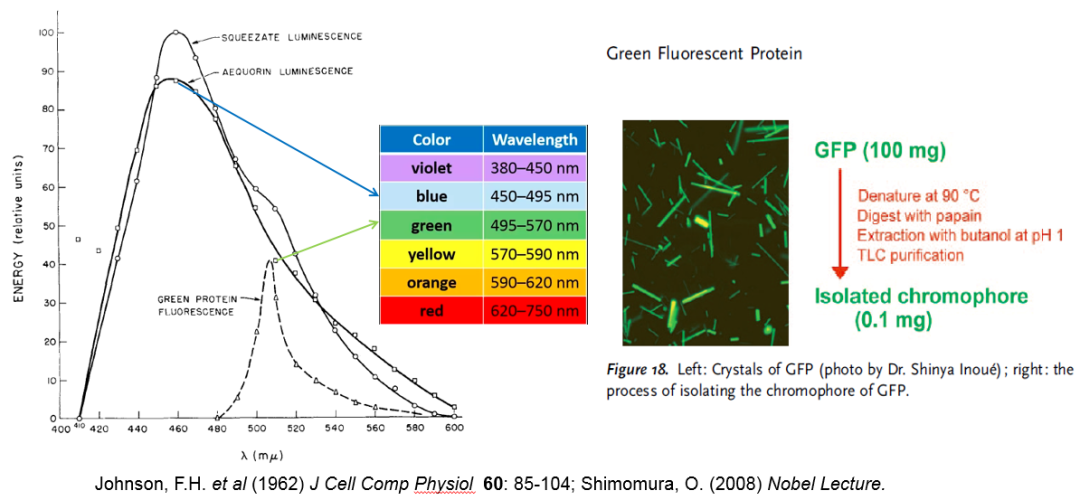
图12:下村修在约翰逊实验室以十几年的跨度完成了水母GFP蛋白的纯化、结晶、和生色团初步鉴定。
约翰逊实验室一直没有掌握蛋白片段测序技术,他们也没有去主动寻找这方面的合作者。在蛋白序列未知的情况下,下村修对GFP生色团的推断比较粗略 (图13),而且他也无法对生色团是否只来自GFP的氨基酸侧链 (而不需要辅因子) 给出确定性结论。图13中GFP包含内蕴的荧光生色团这一改变历史的突破性认识,需要等到十几年后的1990年代中期。
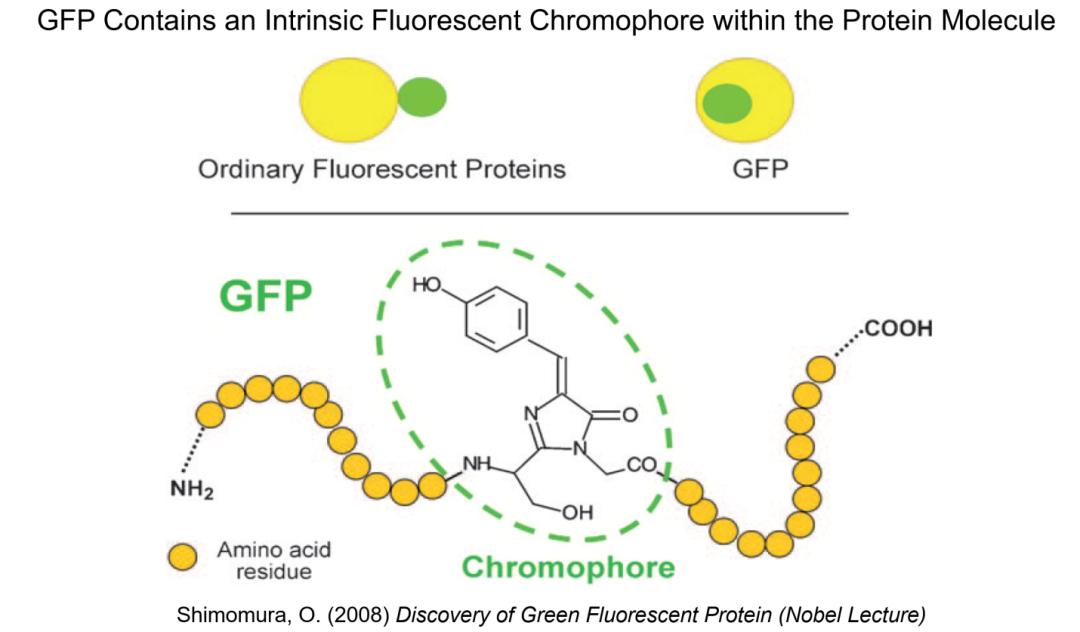
图13:水母GFP蛋白分子含有内蕴的荧光生色团
1981年,在多位学术界朋友的帮助下,下村修终于在约翰逊教授退休四年后被美国麻州伍兹霍尔的海洋生物学实验室 (Marine Biological Laboratory, MBL) 聘为资深研究员。自此他的研究工作开始转向其它发光生物,不再涉及水母的GFP。我们在此借用多年后的知识体系来总结下村修研究水母发光的几个重要发现:在钙离子的激发下,水母伞膜边缘发光器官中的水母素通过其萤光素酶活性,利用与之共价结合的腔肠素和过氧化键这一“内蕴的氧气”实现生物发光。而水母素产生的光能马上通过生物发光共振能量转移 (Bioluminescence Resonance Energy Transfer, BRET) 传递给邻近的GFP,最终发出肉眼可见的GFP绿色荧光 (图14)。
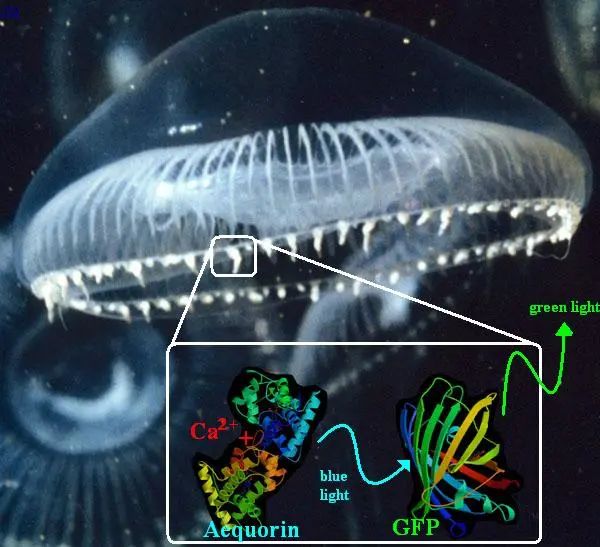
图14:水母运用BRET机制将水母素的蓝色生物发光能量转移给邻近的GFP并引发出绿色荧光。来源:
普瑞舍对水母发光蛋白的分子克隆
在下村修和约翰逊发现水母素和GFP的1960年代,分子生物学尚在孕育过程中,生物学家若想要研究某个蛋白的功能,只能走传统的“华山一条路”:制备大量的目标物种抽提物样品,然后用生化手段来进行蛋白纯化。对于那些可以人工大量培养的生物或者细胞株而言,蛋白纯化所需的原材料可以取之不尽。但是水母这样的海洋生物至今无法人工养殖,实验用的纯蛋白需要靠劳动力密集的不断打捞和制备才能保障供给。目标物种一旦由于生态环境的改变而不再出现在固定水域,蛋白功能的研究也会陷入止步的境地。幸运的是,随着遗传密码的解读与分子生物学中心法则的确立,重组DNA技术在1970年代末应运而生,而来自病毒的反转录酶又催生了威力巨大的cDNA分子克隆技术。生物学家一旦能将编码目标蛋白的cDNA克隆到大肠杆菌的质粒中,就能通过培养细菌而轻易获得大量纯蛋白,不但对功能的基础研究不再有后顾之忧,而且在开发应用上也将事半功倍。
美国佐治亚大学的科米尔教授 (Milton Cormier) 从1950年代起就研究生物发光,早年主要研究海堇 (Renilla, sea pansy)。在下村修和约翰逊的突破性工作发表后,科米尔实验室也开始把一部分研究精力转向了水母。GFP故事的第二位主角普瑞舍 (Douglas Prasher) 于1983年来到科米尔实验室,开始他的第二轮博士后训练。普瑞舍在上一个博士后实验室主攻细菌遗传学,成功掌握了新兴的分子克隆技术,这在当时并非易事。1982年,著名实验手册《Molecular Cloning: A Laboratory Manual》的出版 (图15) 有力推动了基因克隆技术的普及,但包括聚合酶链式反应 (PCR) 在内的很多技术手段还没有被发明。
图15:1982年第一版《Molecular Cloning》实验手册的封面
科米尔希望新来的普瑞舍能接受克隆水母素基因的挑战,一旦成功,该实验室一个晚上通过大肠杆菌产生的水母素蛋白量,就能超过他们整个夏天能在星期五港通过打捞水母纯化的总和。能够从单个水母中制备的总mRNA量并不高,普瑞舍也需要像下村修那样前往星期五港采集大量的水母样品。1985年,普瑞舍经过连续两个夏天的积累,抽提出足够的mRNA来构建cDNA文库。随后根据已知蛋白序列设计的分子探针,筛选cDNA文库后成功分离出6个编码水母素的cDNA克隆,对应了5种蛋白异构体 (isoforms)。普瑞舍把这些基因克隆在大肠杆菌中表达后,却连续几周无法在蛋白凝胶电泳上检测到水母素对应的条带。科米尔的科研直觉告诉他电泳检测的灵敏度不够,马上请技术员麦卡恩 (Richard McCann) 帮助普瑞舍设计了水母素的生物发光检测,终于确认了基因克隆的成功!通过在大肠杆菌中的超量表达,作为钙离子染料的水母素价格很快大幅度降低,成为一种常用的实验试剂。
借着成功克隆水母素基因的势头,普瑞舍终于完成了漫长的两轮博士后训练,于1987年10月被美国麻州的伍兹霍尔海洋研究所 (Woods Hole Oceanographic Institution, WHOI) 聘为独立的助理研究员。在正式离开科米尔实验室之前,普瑞舍很自然地设定了下一个基因克隆目标:GFP。考虑到GFP的蛋白和mRNA丰度远低于水母素,普瑞舍需要每年再去星期五港采集将近7万只水母,才为将来的GFP克隆积累了足量的总mRNA。
普瑞舍在WHOI虽然独立,但由于启动经费有限而无法招募研究生、博士后、或者技术员,只能单枪匹马投入克隆水母GFP基因的战斗。同时他对下村修提出的GFP蛋白发荧光需要一个辅因子的假说持怀疑态度,设想一旦拿到了 GFP基因并在大肠杆菌中表达,如果能直接观测到绿色荧光,那么通过重组DNA技术将GFP基因与任何物种的一个基因融合,就能用荧光来定位蛋白产物在细胞中的表达。普瑞舍根据这个令人激动的想法,递交了多份科研基金申请书,但大多都遭到了评审委员会的否决,只有美国癌症协会 (American Cancer Society) 同意提供20万美元的经费。
1989年初,普瑞舍经过了近两年的苦战,在水母基因文库中筛选到了一个他命名为pGFP1的cDNA克隆,该质粒包含了编码168个氨基酸的序列。已知GFP蛋白的全长是238个氨基酸,普瑞舍注意到这个cDNA的5’端和3’端都不完整。这个168个氨基酸的蛋白序列对与他合作的沃德实验室 (William W. Ward) 帮助巨大,让他们大幅度完善了下村修1979年的GFP生色团工作,确定GFP内部的三个相连的氨基酸侧链 (Ser65-Tyr66-Gly67) 就是产生绿色荧光的分子基础 (图16)。但普瑞舍若想把GFP的荧光应用为分子定位的工具,就必须克隆GFP的全长cDNA,这意味着他要回头去构建新的水母cDNA文库。
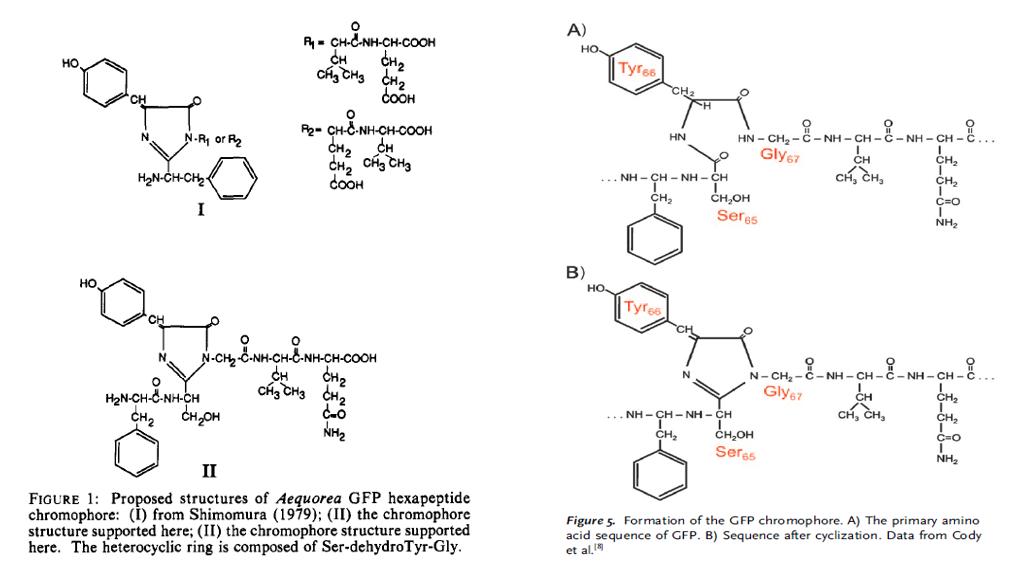
图16 来源:Cody, C.W., Prasher, D.C., et al (1993) Biochemistry 32: 1212 - 1218
查尔菲和钱永健创立GFP标记技术
就在普瑞舍开始为构建新的cDNA文库而重新采集水母的同时,GFP故事的第三位主角查尔菲 (Martin Chalfie) 以一种出人意料的方式登场。查尔菲在美国哥伦比亚大学的实验室致力于研究秀丽线虫的触觉神经生物学,1989年4月25日,他照例参加了系里每周二中午的讲座。来自塔夫茨大学的布莱姆 (Paul Brehm) 介绍了多种生物的发光蛋白,查尔菲对用作钙染料的水母素早有耳闻,而对发绿光的水母GFP则是首次听说。被紫外线或者蓝光激发的单体GFP蛋白,很可能不需要辅因子就能发出荧光,这个特性让查尔菲这个有心人激动不已。
秀丽线虫固然有全身透明这一天然优势,但当时常用的几种基因和蛋白表达定位技术都需要冗长的样品制备步骤,而且由于染色试剂需要渗透进入线虫体内,因此无法用于直接观测活体动物 (图17左)。只有238个氨基酸的GFP若真能发光,研究者可以用分子生物学手段将其与感兴趣的线虫基因融合,通过融合蛋白上的GFP荧光标记就能直接在显微镜中观测该基因在哪些细胞中表达。查尔菲在第二天通过辗转的电话咨询,四处打听是否已有科学家成功克隆了水母GFP的基因,最后发现只有WHOI的普瑞舍可能给他想要的答案 (图17右)。
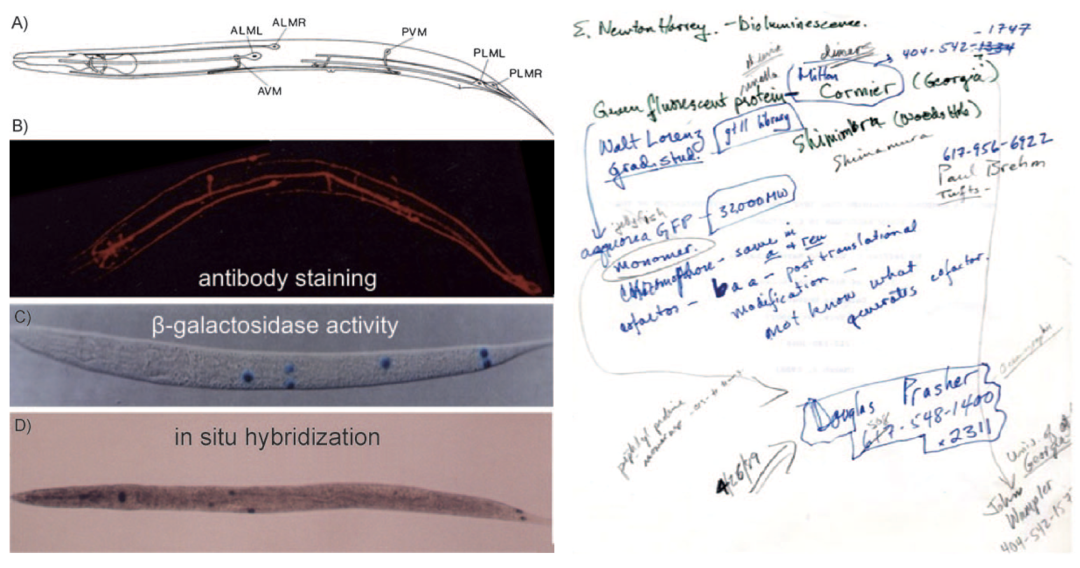
图17:全身透明的秀丽线虫适合研究动物发育过程的细胞分化和功能。GFP技术之前的几种基因表达定位法都需要样品制备,而无法用于直接观测活体线虫。查尔菲从布莱姆的讲座了解到GFP的发光特性后,通过一整天的辗转电话咨询与普瑞舍取得联络。来源:Chalfie, M. (2008) Nobel Lecture。
查尔菲与普瑞舍在电话中谈得很投机,两人对GFP的应用前景想法相似,但他们的合作必须要等普瑞舍拿到GFP完整的cDNA克隆之后才能开始。考虑到之前用细菌质粒构建的水母基因文库平均片段不够大,普瑞舍决定改用λ噬菌体来构建新的cDNA文库,两年后筛选得到包含了编码238个氨基酸完整序列的λGFP10克隆 (图18)。可惜此时的普瑞舍已经没有心情来庆祝这个阶段性成功:(1) 美国癌症协会提供的科研经费已经用完,他最新递交的基金申请屡屡被拒;(2) 他把λGFP10转到大肠杆菌中表达,得到的GFP蛋白却没能在显微镜下发荧光,这动摇了他之前认为GFP无需辅因子或者转化酶就能发光的想法;(3) WHOI的同事们对他克隆基因工作缺乏兴趣,拿不到新经费的他已看不到通过终身教职评审的希望。普瑞舍决定先公布GFP的cDNA序列,但论文从投稿开始也不太顺利,用了近一年的时间才于1992年2月正式发表。

图18 来源:Prasher, D.C., et al (1992) Gene 111: 229 - 233
普瑞舍在论文发表前后试图通过电话与查尔菲联系,很不凑巧的是,查尔菲由于新婚而正在他夫人所在的犹他大学实验室学术休假。就在普瑞舍由于联系不上查尔菲而无法展开合作计划的时候,GFP故事的最后一位主角钱永健教授 (Roger Tsien) 在1992年5月读到了普瑞舍的新论文。钱教授从研究生时代开始就希望通过荧光共振能量转移 (Fluorescence Resonance Energy Transfer, FRET) 来研究蛋白之间的相互作用,几年来他一直想获得编码荧光蛋白的基因。将标记基因导入要研究的细胞要比标记蛋白容易许多,同样是有心人的钱教授一眼就能看出普瑞舍手上这个cDNA克隆的价值。普瑞舍在电话里告诉钱教授:由于申请经费的困难,他将很快离开WHOI而前往美国农业部就职,并从此告别GFP的研究。普瑞舍愿意马上分享GFP基因的克隆,可惜钱教授的实验室里虽然化学高手众多,但还无人掌握分子生物学的技术,他需要等1992年10月新招的博士后海姆 (Roger Heim) 报到之后才能接收处理普瑞舍寄来的样品。这五个月的延迟反转了查尔菲几乎与GFP擦肩而过的“剧情”。
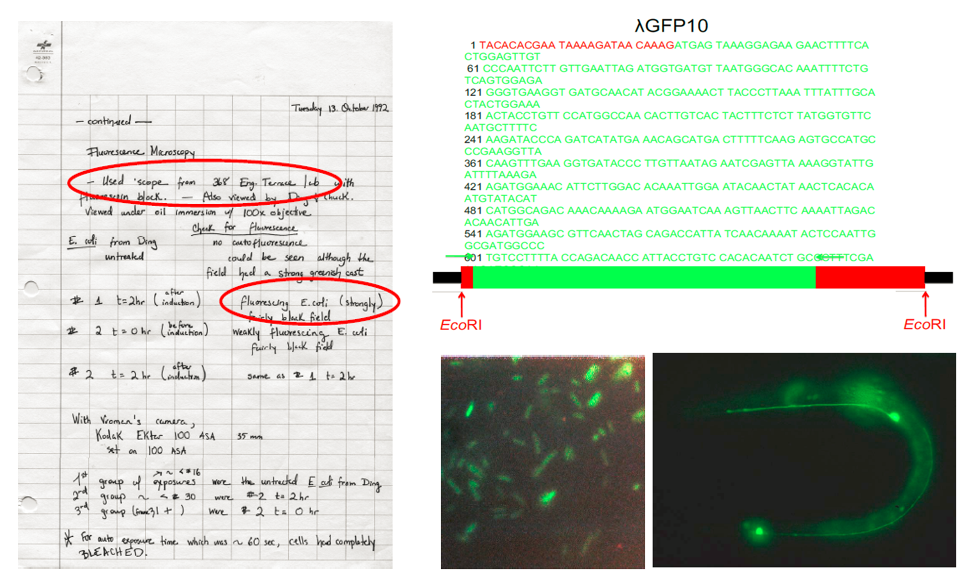
图19 来源:Chalfie, M. (2008) Nobel Lecture
查尔菲在1992年秋季开学前回到哥伦比亚大学。9月初,一年级博士生吉娅 (Ghia Euskirchen) 希望来查尔菲的实验室做第一个轮转。查尔菲听说吉娅刚在本校工程学院完成的硕士论文与荧光有关,不由感叹普瑞舍三年来一直没有音讯,只能和她通过电脑文献检索寻找与GFP有关的课题设计思路。查尔菲看到普瑞舍年初发表的完整GFP基因序列后喜出望外,立刻通过电话联系重启计划中的合作。拿到普瑞舍的GFP克隆后,查尔菲注意到由于分子克隆过程中只用限制性内切酶而未用PCR技术 (1992年前后,包括WHOI在内的很多美国科研院校都还没有PCR仪器。即使在哈佛等常春藤院校,也需要同一楼层的多家实验室共用一台),λGFP10在GFP编码序列的两端都有来自水母基因组的多余非编码DNA序列,其中5’端起始密码子的上游多了25个碱基对 (图19右上,红色标注)。查尔菲的分子生物学直觉告诉他,两端多余的序列可能会干扰GFP在大肠杆菌中的表达,于是他指导首次上手分子克隆实验的吉娅在高年级博士生薛定的帮助下,利用PCR只把GFP编码序列转到表达质粒中。
几周后,吉娅获得了许多包含GFP表达质粒的菌落。她想既然查尔菲认为GFP的蛋白产物可能直接发出荧光,不妨拿着培养皿回到熟悉的工程学院,直接用那里的荧光显微镜碰碰运气。1992年10月13日,吉娅的实验笔记本 (图19左) 完整记录了这一出乎意料的“尤里卡时刻” (Eureka moment):多个大肠杆菌菌落在显微镜下发出漂亮的绿色荧光!查尔菲看到后自然激动不已,他连续几天拿着吉娅拍摄的显微镜照片四处炫耀 (图19右下)。实验结果清楚证明:GFP蛋白无需来自水母的任何辅因子或者转化酶就能自发在另外一个物种的细胞中发出绿色荧光。
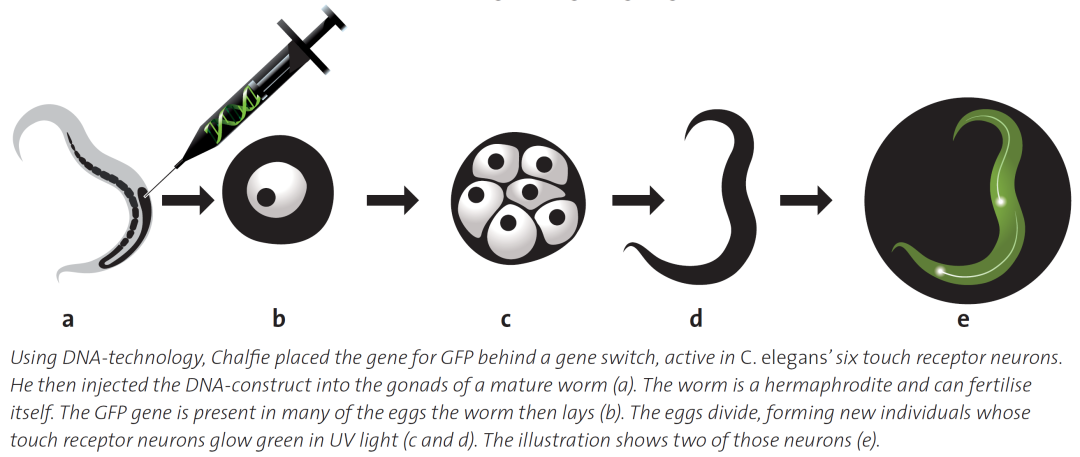
图20:查尔菲实验室运用重组DNA技术将水母GFP基因与秀丽线虫的触觉感受神经元转录启动子相连,成功展示GFP的绿色荧光可以用来特异性标记单个细胞。来源:
吉娅在完成这一实验后很快去另一个实验室轮转,查尔菲让技术员尝试一个新的实验:先将GFP基因与秀丽线虫触觉感受神经元的特异启动子 (promoter) 相连,然后用显微注射把新构建的质粒转入成熟线虫的性腺。只要GFP的表达成功,雌雄同体的线虫产生的下一代幼虫中的触觉感受神经元就会被绿色荧光在显微镜下点亮 (图20)。这一成功的突破性实验最终以Science杂志封面论文的形式载入科学史册 (图21)。
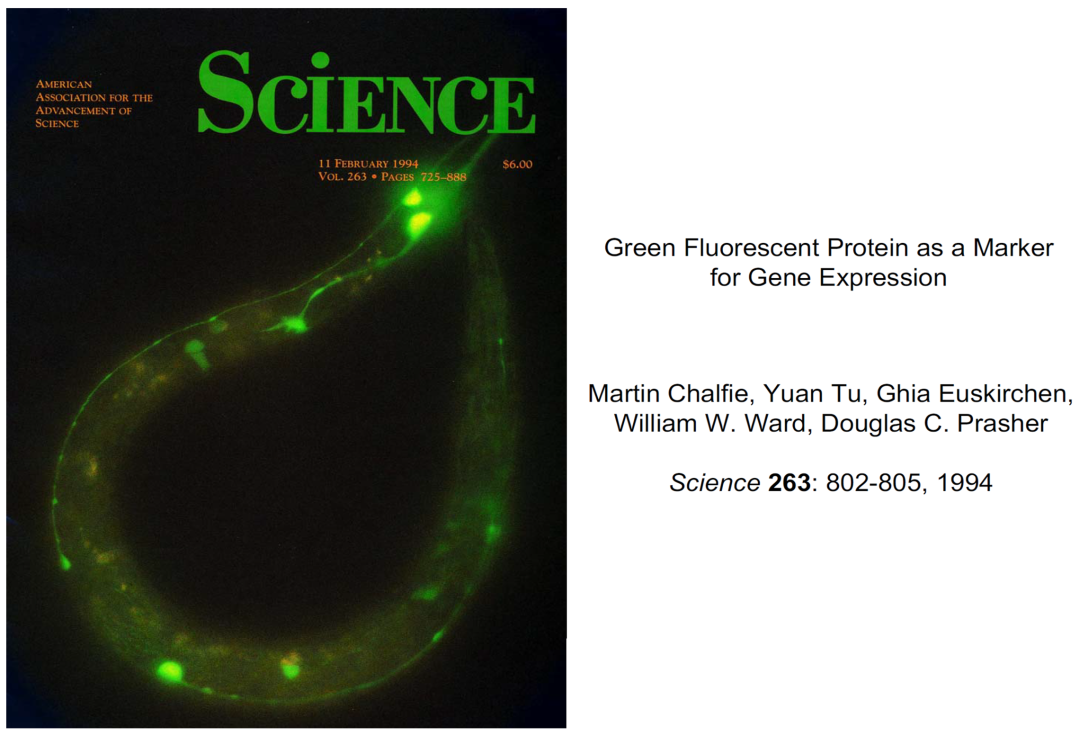
图21 来源:Chalfie, M. (2008) Nobel Lecture
多年以后再回首,吉娅的“尤里卡时刻”原本可以属于普瑞舍,而让他失之交臂的“罪魁祸首”很可能就是λGFP10的5’端多出的那25个碱基对!作为单细胞原核生物的大肠杆菌,其基因转录调控相对简单,只需要启动子加上一段调控序列(regulatory sequence) 就能达到开关的效果。而水母作为多细胞真核生物的转录调控机制就要复杂许多,需要启动子与近程和远程的多种增强子 (enhancer) 和调控序列相互作用 (图22)。当来自水母的5’端调控序列被携带进入大肠杆菌的质粒,它们就可能打乱细菌的启动子“上下文”,从而干扰目标基因的正常表达。普瑞舍在1991年若能通过寻找合作者而用上PCR技术,那么GFP研究的历史就会被改写。中学语文课本中曾收入叶圣陶先生著名的短篇小说《多收了三五斗》,而我们在此可以通过模仿的标题来概括普瑞舍与诺贝尔奖擦肩而过的悲壮:多克隆了25个碱基对。
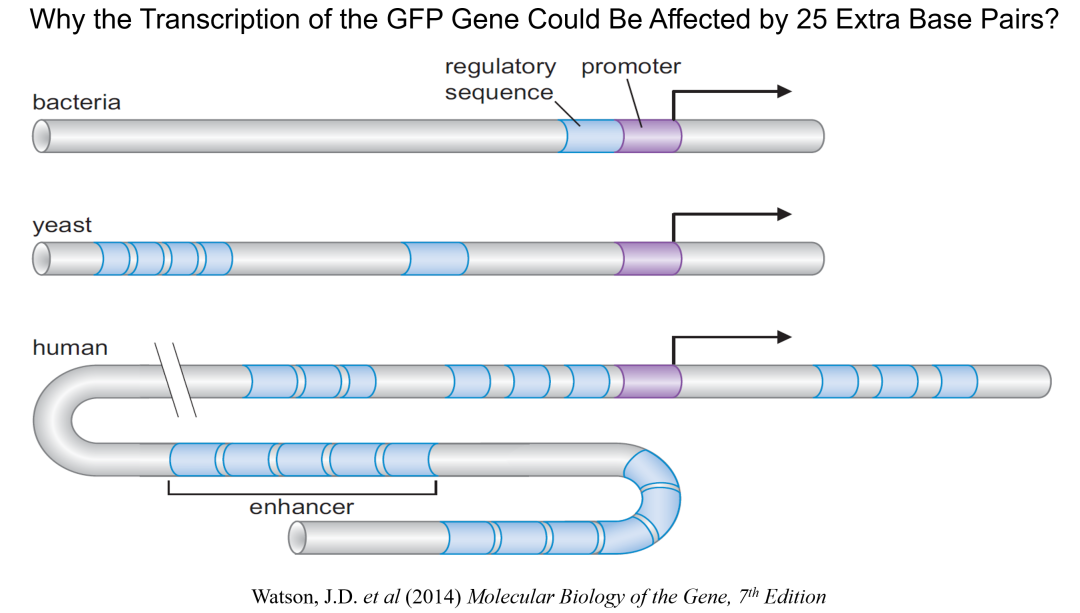
图22:普瑞舍多克隆的25个碱基对干扰GFP在大肠杆菌中表达的潜在分子生物学机理。
钱永健在海姆抵达后马上又和普瑞舍通了电话,普瑞舍在如约寄出GFP基因克隆的同时告知:查尔菲实验室已在一个月前收到了这个克隆。钱永健在起跑已经落后的情况下决定与查尔菲开始良性竞争,双方互通信息,主动避开对方的研究方向。得知查尔菲证明GFP在其它生物中能够独自发光虽然让钱教授对其应用前景充满希望,但以他深厚的有机化学功底,依然不能理解Ser65-Tyr66-Gly67这三个氨基酸侧链如何自发环化形成沃德和普瑞舍阐明的生色团,尤其是那一步碳碳单键脱氢成为双键,这在没有酶催化的情况下很难发生 (图23)。钱教授能够想象的化学途径只有两种:(1) 两个氢原子结合成为氢气而被释放,这在生物化学环境里发生的可能性极低;(2) 需要一种氧化剂把两个氢原子带走,而实验者可以直接操控的氧化剂只有空气中的氧气。钱教授建议海姆在严格绝氧的恒温摇床里培养含有GFP表达质粒的大肠杆菌,他们惊喜地发现此时在电泳胶上虽然可以看到分子量正常的GFP蛋白,但这些细菌却不能发出荧光。当把细菌培养液放回有氧环境两小时后,就又能看到绿色荧光。钱教授据此给出了GFP自发形成生色团的详细化学机理,其中会生成过氧化氢的理论推断要等到2006年才被其它实验室证实 (图23,右上)。
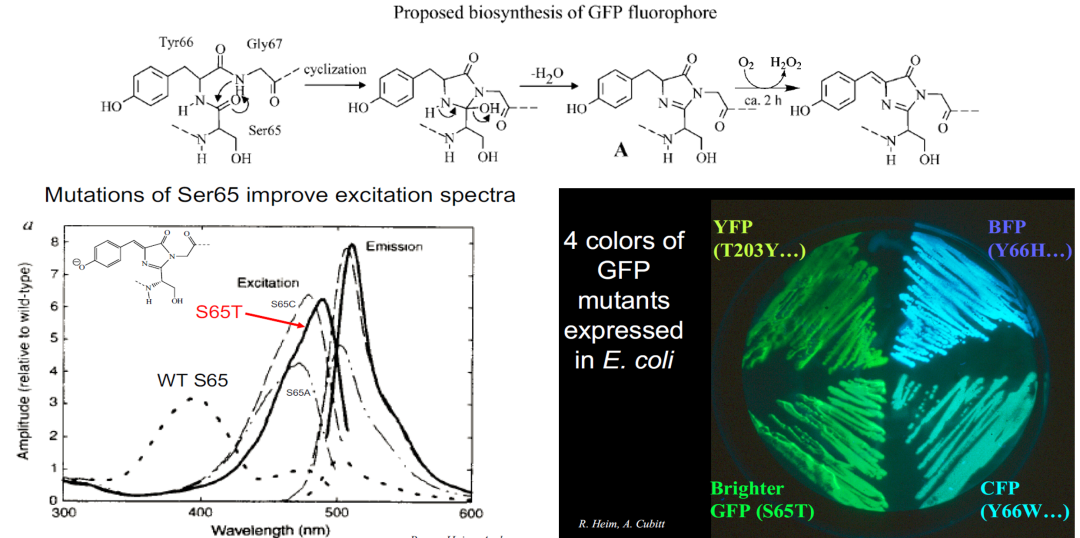
图23 来源:Tsien, R.Y. (2008) Nobel Lecture
钱教授对野生型GFP的激发光谱有高低双峰也颇感困惑,紫外线比蓝光更能有效地激发GFP的荧光 (图23,左下)。他根据自己的有机化学直觉推断,丝氨酸65 (Ser65, S65) 这个侧链可能是导致双峰的关键。分子生物学高手海姆在讨论时提醒钱教授,可以用定点诱变的方法将丝氨酸65替换成其它氨基酸来验证这个假设。当丝氨酸被换成苏氨酸 (S65T) 后,紫外激发峰居然消失,而蓝光对这种GFP的荧光激发效率是野生型GFP的8倍 (图23,左下和右下)!定点诱变法为钱永健实验室全面改良GFP打开了洪水闸门,他们先后推出的蓝色荧光蛋白(BFP),青色荧光蛋白 (CFP),黄色荧光蛋白 (YFP), …… 为实验生物学家们的“调色板”增添了五颜六色 (图23,右下)。
2008年度的诺贝尔化学奖最终由下村修、查尔菲和钱永健三人分享。已离开学术界多年的普瑞舍,在经历了命运的颠沛流离和曲折离奇后,由于诺奖的人数限制也未被委员会青睐。更令人唏嘘的是,星期五港附近的海域由于持续遭受石油开采造成的环境污染,发光水母从1990年代中期开始彻底消失了踪影。
推荐阅读
[1] Pieribone, V. & Gruber, D.F. (2005) Aglow in the Dark: The Revolutionary Science of Biofluorescence, Belknap Harvard.
[2] Shimomura, O. et al (2017) Luminous Pursuit: Jellyfish, GFP, and the Unforeseen Path to the Nobel Prize, World Scientific.
【GFP发现史讲座视频】
链接1:
链接2:
本文经授权转载自微信公众号“药时代”,《返朴》发表时作者有二次修订。
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 