为什么我们长得左右差不多对称,身体里的器官却不对称?
撰文 | Catherine Offord
编译 | 继省
蓦然回“手”——意外进入细胞手性研究领域
时钟拨回到2009年的一天。科学家万群(Leo Wan)正在用显微镜观察他培养的小鼠细胞。看着看着,他发现这些小鼠细胞不太对劲儿,像是长“拧劲儿”了。这批细胞的名字是成肌肉细胞(myoblast),顾名思义可以生成肌肉,是肌肉细胞的前身。他所培养的数百个成肌肉细胞长在了一个微型芯片上。向芯片上接种细胞时,万群使用的是一种微观图案技术(micropatterning):经由此技术处理的细胞,会附着在培养表面上,并依照研究者事先设计的某种高度规则的模式或图案生长。(译注:此技术可用于探究细胞的形态控制和迁移行为等重要生理过程。)

图1. 肿瘤细胞在不同宽度的线性区域内生长丨图源
万群在哥伦比亚开展博士后研究期间,就有一部分精力是放在对这一技术的完善上。他原本以为,这些狭长的细胞会自己顺着芯片(译注:此处所用的芯片为矩形)的长边排布。但他告诉TheScientist杂志,当时这些细胞看起来像是被往左拉偏了一点儿。
据万群回忆,最初他以为这只是一次偶然现象。然而在那之后,这个现象反复出现,并且细胞几乎总是偏向同一个方向(译注:即总是向左偏)。他和导师生物工程专家Gordana Vunjak-Novakovic讨论后,一致决定,调整他的课题方向,专攻他所看到的这一特殊现象。
万群把成肌肉细胞接种到了两种芯片——矩形芯片和环形芯片上,并测量细胞在两种芯片上时的倾斜扭转数据。细胞长在环形芯片上时,会沿着圆圈方向持续生长。他猜测他可能捕捉到了细胞的某种内在偏向,即细胞会沿着某个特定方向排列,而不是其他方向。尽管细胞偶尔会向右偏转(即顺时针),或是没有明显的偏向,但超过80%的时间细胞都会向左偏(逆时针)。
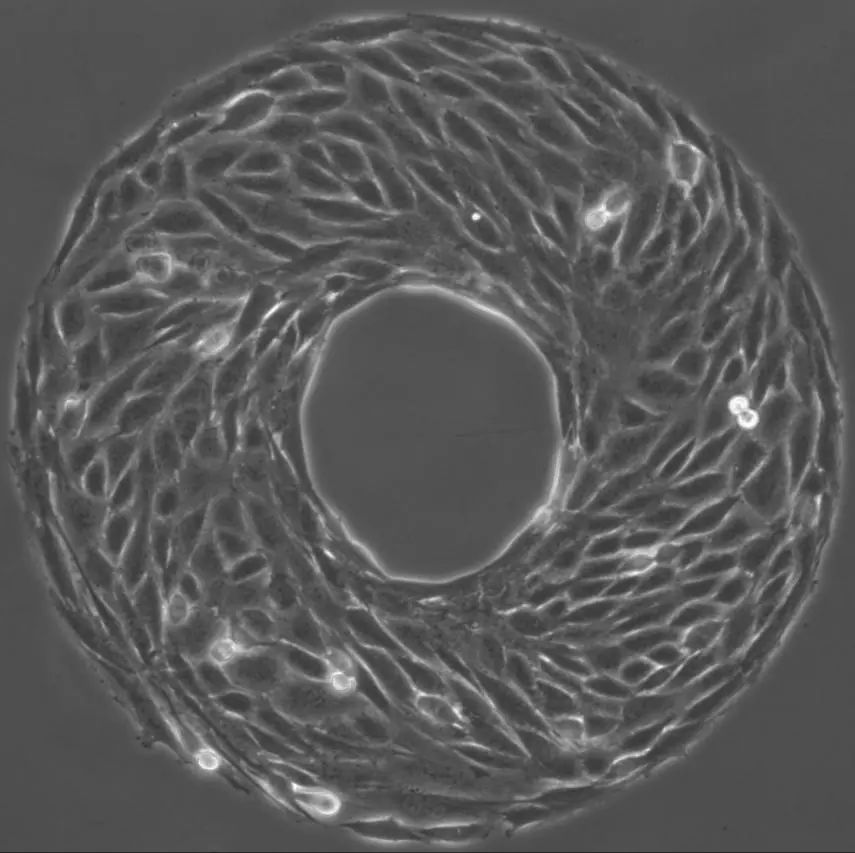
图2. 细胞“甜甜圈”:小鼠肌肉细胞长出了一个圆环图案,显示了逆时针旋转的手性(万群供图)
当他进一步研究发现,这种内在偏向似乎因细胞而异,“有些细胞顺时针,而有些是逆时针的”,他对这个猜测更加笃定。比如,人类肌肉细胞与小鼠成肌肉细胞相似,存在逆时针的偏向。他所在的团队于2011年在《美国国家科学院院刊》(PNAS)[1]上发文报道了这一现象。在这一篇文章中他们还提到,包括皮肤、心脏、骨骼细胞的很多细胞,是倾向于顺时针偏转的;皮肤癌细胞则是个例外,倾向于逆时针偏转,与尚未癌变的正常皮肤细胞正好相反。万群现在在纽约的伦斯勒理工学院开展研究工作。对当时的他来说,这一发现将他引入了动物生物学的一个冷僻方向——细胞手性(cell chirality)。这是一个鲜少为人理解的现象。过去几十年间,在各种细胞上记录这一现象的研究者屈指可数。
手性——现象常见但原因未明
从广义上讲,手性是在空间不对称物体的一种特性——当物体无论如何旋转,都无法和它的镜像完全叠加重合时,我们就称这一物体具有手性。据此观点,不对称的物体就可以分为右手的或左手的,分别对应着顺时针旋转或逆时针旋转。尽管有时候手性很难清晰描述出来,但这个特征在生物学中极为常见——小到一个分子,大到整个生物体都可能存在手性。例如,DNA等生物聚合物形成的螺旋天然就具有手性结构(译注:DNA螺旋主要是右手螺旋);氨基酸在组成复杂的三维结构时也可能有左右手之别。研究者现在知道,分子的手性对其功能有至关重要的决定性作用。而且,生物体在选择手性形式时还很挑剔:尽管很多分子的左右手性形式可以同时存在,但几乎所有生物在其合成和代谢过程中,都毫无例外地选择左手性的氨基酸和右手性的糖类。
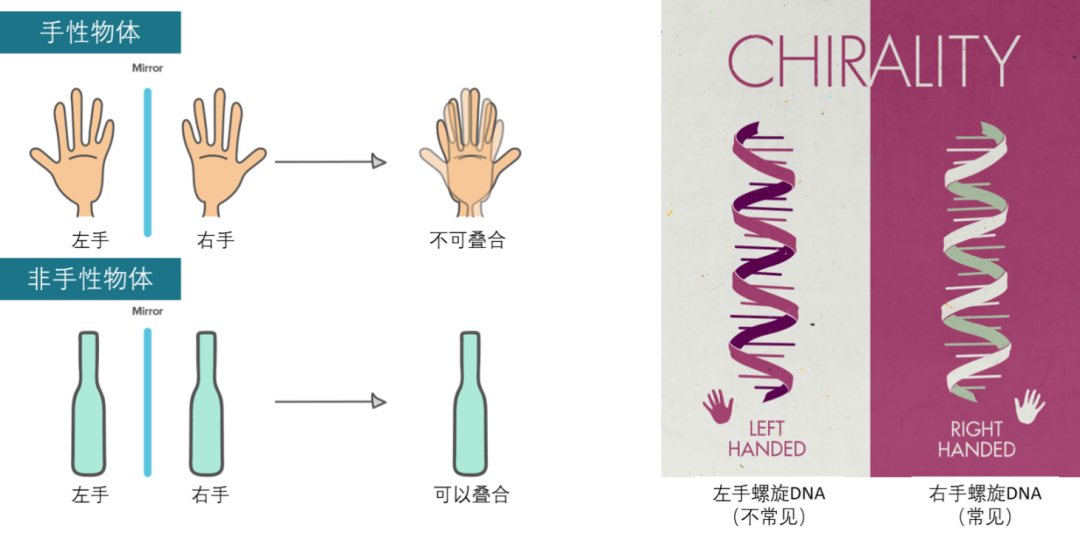
图3. 左:手性和非手性物体示意图(修改自可汗学院网络课程插图)右:DNA双螺旋手性示意图。
手性在宏观尺度上也很常见。在动物的身体平面上,即使外表看起来对称的生物也存在手性。拿人类来说,从头到脚,从后往前,这两个体轴方向上很明显是不对称的;而在第三体轴即从左到右的体轴上,人类的身体也同样不对称。正常人体发育中,主要脏器多数最后会定位在身体中轴线的某一侧——比如肝脏在右侧,胃部总在左侧,心脏略微偏左。手性也可见于器官本身:例如心脏从结构上就是左右不对称的,在另两个体轴上也同样不对称。这些不对称模式在人体发育过程中一旦发生错误,便会导致左右对称异常。
例如,有一些人的脏器左右位置和正常人完全相反,正常在右侧的器官会出现在左侧,反之亦然。当全部器官都处在正常位置的相反一侧,我们把这一现象称为全内脏反位(situs inversus totalis)(图4)。这种情况在人群中出现的概率大约为万分之一。由于器官之间的相对位置关系没有改变,这一情况并不一定对身体有害。然而,如果只是个别器官异位,例如左位心(levocardia,除了心脏其他器官均对侧异位)、右位心(dextrocardia,只有心脏出现在对侧),或是内脏异位(situs ambiguus,有异位和没有异位的器官混在一起),病人往往会出现心脏病等医学症状,原因便是异位器官无法与其他器官正确协作。
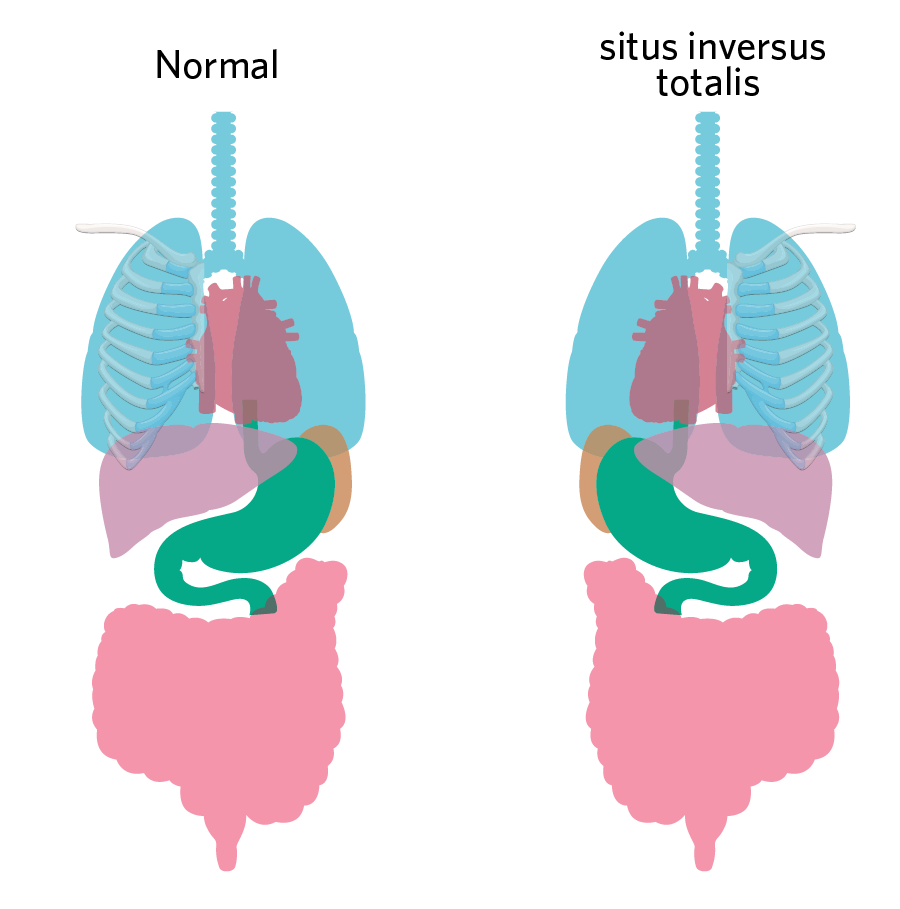
图4. 正常器官(左)与全内脏反位(右)丨修改自图源:
动物界也有类似的不对称异常的发育情况。例如,过去几年间,诺丁汉大学的研究者对大池塘蜗牛(Lymnaea stagnalis)的壳螺旋方向进行跟踪记录,他们发现,尽管大多数时候这种蜗牛的螺壳都是右手螺旋,但也能发现个别的左手螺旋。他们正在研究这一现象背后的遗传基础[2]。
塔夫茨大学的Michael Levin是万群2011年论文的编辑。Levin提到,身体层面的不对称性如何形成,是动物发育领域由来已久的谜题,其中又以左右体轴最难以理解和研究。上下和前后两轴都有明确的现实意义,比如要跟随重力,或者要为动物或有极性的细胞指示运动迁移的方向;但左右轴相比之下并没有明显的意义。Levin说,“如果你试图向一个外星人解释,你说,‘好,我的左手……’;那么问题来了, ‘左’究竟是什么意思?这个问题委实难以回答。”
单个细胞同样具有手性:除了表现为上下和前后的不对称性之外,细胞在左右轴方向上也是不对称的。对于万群等人来说,单个细胞层面上的手性,是解开动物身体不对称性谜题的重要一环。如今,单细胞手性这个现象已经广为阐释。例如,我们熟知的一种纤毛虫——草履虫——在游动时就倾向于向左螺旋;类中性粒细胞——一种用来研究免疫细胞迁移的细胞系,与中性粒细胞类似——也呈现出了运动中向左的偏向。万群认为,“在具有手性偏向的细胞中,存在某种共性”。他和Levin等同行认为,这一现象揭示了分子不对称性与器官或组织不对称性之间存在某种机制上的联系,而这一联系可能之前被忽略了。
“对我来说,从对大型生物体的单侧化行为探索,比如人惯用右手,很自然地就过渡到了对单个细胞的单侧化行为的探索”。从20世纪90年代起,Levin就一直在酝酿关于细胞手性和身体不对称性的假说。他的想法经常会与发育生物学领域里已有的一些“科学共识”相矛盾。但他认为,细胞手性和身体不对称性,只是同一件事情发生在不同的尺度而已。
争鸣——多家课题组探索细胞手性建立机制
在万群开始研究左偏细胞(译注:即前文所提的向左偏向生长的成肌肉细胞)没多久,在世界的另一边,新加坡国立大学力学生物学研究所Alexander Bershadsky实验室里,博士后Yee Han Tee开始应用另外一种微观图案技术,来研究细胞形成内部结构的方式。她所研究的内部结构叫微丝蛋白骨架,是细胞生长、运动和细胞内运输的重要媒介。Tee将单个的成纤维细胞铺在有粘性的微型“小岛”材料上,这样可以“强行”让本来伸长生长的细胞长成圆形。在接下来的几个小时里,她用显微镜记录下了每个细胞内部细胞骨架形成的过程。Alexander Bershadsky回忆道,“有一天,Tee找到我,告诉我说这些细胞表现得非常有趣,具体说就是,它们的内部在旋转”。
他们利用荧光标记技术跟踪单个微丝纤维的运动,发现有两组纤维似乎在细胞内建立一种逆时针涡旋的运动方式[3]。第一类是所谓的辐射纤维(radial fiber),从细胞边缘向内生长到细胞中心,形成了类似自行车轮上辐条的图案。另一类是横贯纤维(traverse fiber),它们在多个点上链接到辐射纤维,并随着后者向细胞中心移动,逐渐形成了同心圆结构。这些纤维最开始以辐射对称的模式规则排列,但在铺下细胞三个小时刚过不久,“辐条”便开始倾斜,导致整个结构开始围绕细胞中心涡旋运动。最后,在11小时附近,纤维停止涡旋并伸展开来,或多或少看上去和细胞的直径方向是平行的。
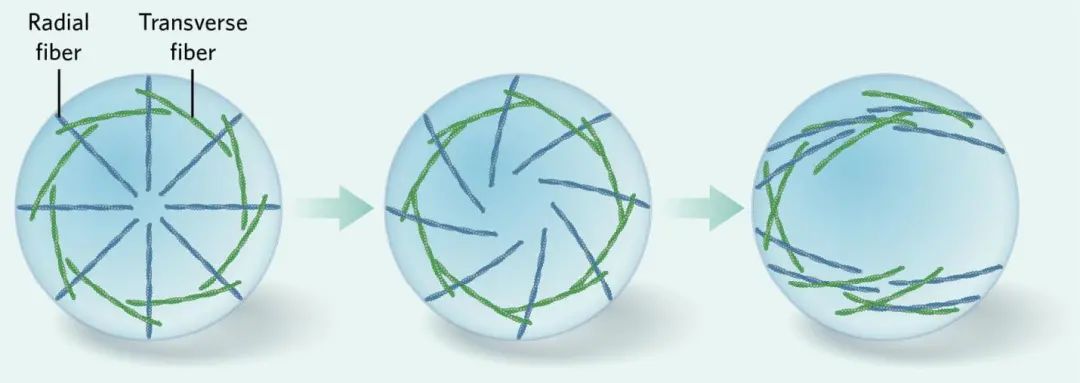
图5. 细胞骨架形成过程中的旋转现象。手性在细胞内得以建立,可能的方式之一便是构成细胞骨架的这些微丝纤维有自发的组织排列。在细胞骨架建立的最初几个小时里,这两类纤维组成辐射对称的模式(图5左),但从三个小时之后,辐射纤维开始倾斜,拉拽得横贯纤维偏离轨迹,引发涡旋模式(图5中),11小时左右,涡旋模式打破为线性模式,纤维沿着细胞主轴排布(图5右)。ILLUSTRATION BY © SCOTT LEIGHTON; DATA FROM NAT CELL BIOL, 17:445–57, 2015.
虽然细胞骨架带有手性算不上新发现,但Bershadsky和Tee等人在2015年发表的这篇研究论文[3]里以实验手段提供了细胞内分子自发形成手性的早期可视化证据,还使用电脑模拟重现了细胞骨架的涡旋模式。为了深入挖掘个中机制,他们还用小分子药物抑制微丝相关蛋白,发现药物处理会导致细胞骨架失去原有的手性偏向,甚至开始向反方向涡旋。其他研究组也在探究这一机制。数年前,来自日本的研究斑马鱼黑色素细胞的科学家们,报道了用微丝组装的抑制剂可以阻断细胞在培养条件下逆时针旋转的趋势[4]。
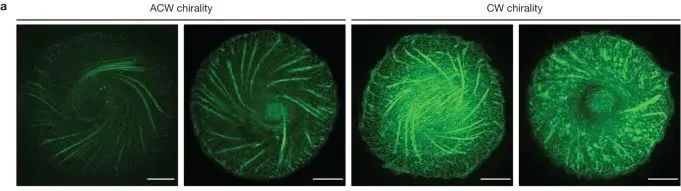
图6 细胞骨架涡旋的两种状态——逆时针(左图)和顺时针(右图)。来自参考文献[3]
微丝本身就是具有手性的分子,它们会形成右手螺旋。Bershadsky和Levin等人因此怀疑,微丝的分子结构在细胞不对称性的建立上有核心地位。Bershadsky说,“我们的观点是,微丝纤维和它的螺旋不对称性就是形成手性的因素。”他同时补充道,目前这个机制如何发挥作用仍然不清楚,有可能微丝的分子结构影响了微丝纤维对机械力的响应,以及与其他细胞内蛋白的相互作用。
实际上,微丝并不是细胞骨架的唯一成分,细胞骨架的组成部分还有微管(译注:此外还有中间纤维)。有一些实验室也在研究微管的作用。微管相比微丝更硬更厚,在囊泡运输等特定细胞内过程中发挥着更大作用。在早期一项关于细胞手性的研究中,研究者使用干扰微管组装的药物处理类中性粒细胞,随即发现:尽管这些细胞依然可以迁移,但不再呈现向左偏的运动模式[5]。几年之后,Levin和同事们发现了类似现象:当敲除掉类中性粒细胞里的微管蛋白(即组成微管的蛋白),细胞的不对称性彻底消失了。
然而,关于微丝和微管在建立细胞手性上的重要性,也有研究者持不同意见。Bershadsky提到,他们在实验中的确观察到微管沿着微丝纤维涡旋,但是破坏微管功能并不能阻断涡旋过程,也不影响涡旋方向。研究黑色素细胞的日本研究组也提到,微管抑制剂反而会让细胞旋转加剧。Levin的课题组除了微管之外也研究微丝相关蛋白,他则认为,微丝和微管可能都参与了细胞手性的建立,“两者都有确凿证据,没有必要非得二选一”。
为了更好地了解不同因子在生物体宏观尺度上如何驱动手性,研究人员尝试了更能模拟自然条件的实验设置来观察细胞手性。例如,万群等人开发了一项三维的微型图案技术(万群也是细胞手性研究领域中与微型图案技术相关的专利的发明人之一),可以更好地复刻胚胎发育环境,进而检测上皮细胞所形成的微球体的旋转行为[6]。研究团队发现,绝大部分微球体按逆时针方向旋转,但当有药物阻断微丝组装时,大部分微球体开始顺时针旋转,就像按下了某个转换开关一样。
万群的团队还开发出从视觉特征上鉴定细胞手性的方法,比如分析细胞内细胞器的分布——他们想以此为动物体内观察实验铺平道路。在近期的一篇论文[7]中,他们推出了一项基于细胞核和中心体相对位置的新手段:由于在移动的细胞中,细胞核倾向留在移动方向的后端,而中心体(译注:中心体是细胞分裂时内部活动的中心,位于细胞核外的细胞质中)常常靠近前端,他们就在细胞核和中心体之间画一条虚拟线,然后记录细胞的重心相对这条虚线的位置。利用这一新观测手段,他们观测到内皮细胞的重心倾向于出现在前后轴线的右侧,而此前已知内皮细胞有向右偏转(顺时针偏转)的倾向,说明观测结果与已知手性吻合。这提示,他们开发的策略可以粗略地测定细胞手性。
万群等人还研究了多个手性细胞聚集后的行为。例如在胚胎中,一些迁移型细胞会聚成一群或同时涡旋以形成特定的器官。这类研究可以帮助科学家确定细胞手性在动物发育中的重要性,解决相关的争议。
由小见大——手性在动物身体不对称性中的作用
到了21世纪早期,脊椎动物胚胎发育中左右不对称性谜题的重要一环被解开:在头尾轴和背腹轴(译注:即前文提到的上下和前后体轴)建立之后,沿着胚胎的腹部一侧,一些细胞在其边缘集结了名为纤毛(cilia)的细小绒毛结构,这些绒毛通过摆动制造了向左的液体流动。这种液体流动引发了细胞在左右轴相对位置上的不对称性基因表达,并最终将身体分为左右两侧。基因敲除(译注:即通过基因工程手段把基因移除)实验表明,当敲除纤毛组装所必需的蛋白(例如驱动蛋白kinesin,这类蛋白沿着微管运输纤毛组装所需要的原料)后,小鼠胚胎中的液体流动会被干扰甚至反转,导致动物体内器官的错位(定位缺陷)。对具有器官对称定位缺陷的小鼠进行基因筛查的结果显示,有数十个纤毛相关基因发生了突变,并且这些突变与小鼠的发育缺陷显著关联[8]。看起来,纤毛便是打破神秘第三体轴对称性的关键。
这一观点出现至今,仍主导了研究者对动物发育的认知。但是,Levin指出,多数研究都忽略了一个关键事实,即敲除纤毛相关蛋白后,细胞骨架和多种胞内进程也一样会受影响(译注:换言之,敲除纤毛相关蛋白后所观察到的器官对称定位缺陷,不能简单地归因为依赖于纤毛的胚胎液体流动,细胞骨架组装等过程同样有可能参与)。此外,左右不对称在鸡、猪和蛔虫等动物中一样存在,而这些动物的胚胎中并没有带纤毛的细胞来引导液体流动[9, 10]。即便在青蛙这种有纤毛的动物中,早在纤毛完成组装和开始摆动之前,就已经能检测到RNA等重要的发育相关分子的不对称分布。敲除微管蛋白会干扰偏侧性发育(译注:即发育过程中的两侧不对称)的现象不仅存在于动物,在植物中一样如此。这反而提示,在建立不对称性时可能存在某种通用的机制,它依赖于微管蛋白,但不是纤毛。
“说纤毛引发了不对称性是完全不合理的……最公平的说法是你可以认为纤毛参与了这一通路的某个中间环节”。Levin认为,也许纤毛放大了由细胞内机制建成的左右不对称性的差异。
尽管一系列证据提示,存在某种不依赖于纤毛的机制来建立组织和身体层面上的不对称性,但个中作用细节远未明晰。研究细胞手性需要解决以下两个问题:
第一,细胞如何提供组织水平上的方向信息?即怎样算左,又怎样算向右?
第二,相比第一点也更有挑战,细胞如何编码具体位置信息?即细胞如何知道胚胎中线在何处,又怎么知道自己在哪一侧?
科学家们现已分头投入了对这两个问题的解析中。
关于第一个问题,很多研究组已经在体外实验中证实,当细胞彼此排列对齐时,细胞手性在群体层面上控制细胞的偏转方向。与万群所用的左偏型小鼠细胞类似,Tee用的成纤维细胞在排列和迁移时亦展示出群体行为模式,而这种模式可以被微丝破坏型药物清除或反转,相关结果已经发在2021年4月的预印本平台BioRxiv上[11]。另有研究者报道,细胞的这类群体行为可以在整个组织和器官的层面上产生影响。Kenji Matsuno是日本Osaka大学的果蝇研究者,他一直在研究果蝇胚胎后肠(译注:一般称胚胎消化系统的末端为后肠)的不对称性。果蝇的后肠在胚胎发育中会有90度的左转,而组成后肠管道的上皮细胞本身就有不对称的形状[12]。Matsuno和他的团队发现,干扰微丝相关蛋白后,既可以翻转上皮细胞的手性(译注:即左旋变右旋),也可以调转后肠的旋转方向(图6)[13]。Matsuno团队在近期的一篇论文[14]中提出,细胞层面上的手性是驱动后肠旋转现象的充分必要条件。
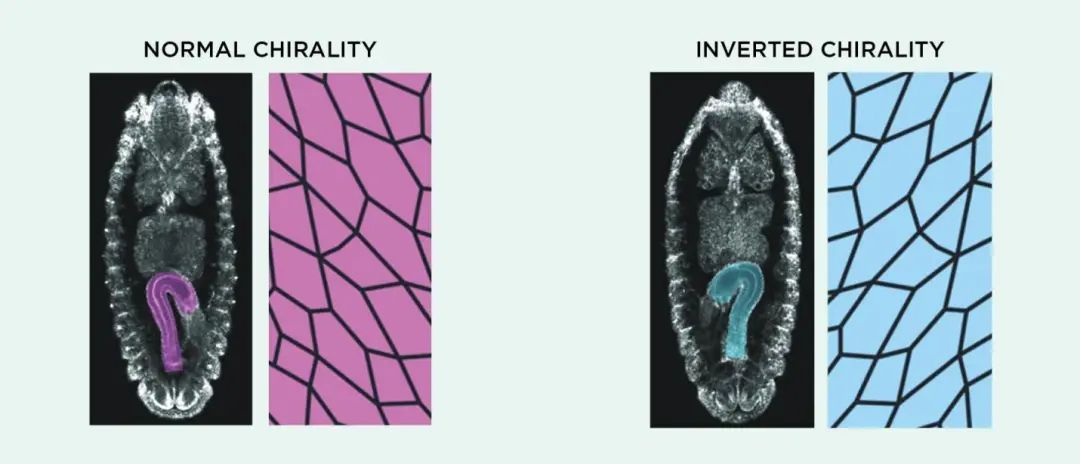
图7. 果蝇肠胃反转:正常果蝇发育过程中,后肠会经历逆时针旋转,最后向右弯曲(左)。研究者敲除掉参与细胞骨架功能的蛋白后,扭转了后肠的旋转方向,得到了指向左侧的后肠(右)。丨来源:M. INAKI ET AL., FRONT CELL DEV BIOL, 6:34, 2018.
万群也在研究鸟类的心脏发育。心脏属于胚胎发育中首批打破体轴对称性的器官——这一过程起于一群特殊的细胞,它们通常会形成向右偏转的环路。万群团队报道[15]说,从鸡胚胎心脏分离出的细胞表现出内在的右手偏向,在培养条件下,可以通过药物处理来翻转手性偏向。可用的药物一般是一些已知的破坏微丝细胞骨架手性和胞内结构的药物。用这些药物处理鸡胚胎后,导致大量胚胎发育出向左转的心脏。万群说,“这给我们提供了某种证据,说明细胞手性很可能起到了某种作用”。他补充说,他的团队还曾偶遇一枚天然发育出向左旋转的心脏的鸡胚。在这一枚特殊鸡胚中,心脏细胞是逆时针的,就像被小分子药物处理过一样。他和同行们将这一工作拓展开,研究手性对人类健康和疾病的潜在意义,包括心脏发育、内皮细胞屏障的通透性[16],以及癌症细胞与正常细胞的竞争[17]等。
然而,尽管上述机制为不对称器官的发育提供了部分解释,在动物身体平面的更高水平上,这些机制如何起效仍不明确。研究者普遍认为,在发育的某个中间时间点(具体节点可能因物种而异),在胚胎的中线形成了某种分子屏障,这一屏障阻隔了身体两侧生长因子的自由扩散,加剧了基因表达产物的不对称性积累。但是Levin也指出,对侧模式异常个体的存在,比如一半雄性一半雌性的雌雄嵌体(如下图的雌雄嵌体蝴蝶),暗示着在胚胎发育的更早期就已经形成了基本的左右分离模式。

图8. 雌雄嵌体动物。尽管大部分雌雄嵌合体出现在昆虫和蛛形纲动物中,但在一些相对高等的动物,包括甲壳类、北美红雀、鸡等之中也会出现。丨图片来自新浪图片站#p=1
“这些遗传紊乱如果发生在胚胎发育晚期,绝不会像现在这样,雌雄特征分居左右、泾渭分明。”Levin发表了用以描述细胞手性的模型[18],并特别指出,特定胞内蛋白沿着细胞骨架上的偏向运输,可以通过在胚胎中建立电压或pH值梯度,来帮助胚胎形成左右不对称”。当然,他现在也认为,真正的机制仍然不明,“完全是个迷”。
道阻且长——细胞手性待解之谜
不论细胞手性在动物发育中起何作用,接受采访的科学家都承认,仍有一些关键的基础问题需要解答。首先,我们仍不清楚,为何有些细胞表现出顺时针偏向,而另一些细胞却是逆时针的?换句话说,这种差异是如何形成的?万群提到,他的同事曾指出肌肉细胞比其他细胞含有更多的微丝蛋白,这可能可以解释为何哺乳动物肌肉细胞向左偏,而其他细胞向右偏或根本没有多少偏向。另外,内皮细胞和上皮细胞通常有相反的手性,这一现象他很有兴趣作进一步研究。
由于细胞和细胞群体在倾斜的方向上不是百分百一致,一些研究者认为这是细胞手性领域的局限之处,这意味着相关研究要依赖于统计手段来鉴定手性偏向。毕竟在万群2011年的论文中,仅有80%的肌肉细胞表现了逆时针旋转偏向,这个比例远少于人体内氨基酸左旋的比例,或是脊椎动物胚胎心脏形成右手偏转的比例,后两者都接近100%。对单个细胞的研究中也有同样的局限:大多数细胞表现了某一方向上的手性,但总有一些细胞向反方向倾斜。
复旦大学的分子工程师丁建东和同事们最近在多篇论文中呼吁,细胞手性研究的一致性较低屡见不鲜,大家应该谨慎分析结果[19, 20]。但这种不一致究竟是来源于实验的人为误差等因素,还是反映了细胞的真实差异,现在仍不好定论。
万群认为,细胞手性非常重要,使用细胞骨架干扰型药物改变细胞和整个器官的手性的研究就有很好的重复性。即便有部分细胞的手性不统一,但细胞群体可能依然足以驱动组织水平上的行为,尤其是细胞手性有可能只是发育过程中参与建立和放大不对称性的众多机制中的一员。
Matsuno补充说,一些研究者渐渐开始改变旧有的、二元的手性观念,转而认为这是一个在左右两个方向上存在强弱不同程度偏好的多元组合。“细胞手性可能不是一个0或1的开关。我现在相信这是个非常复杂的现象。”
Bershadsky认为,细胞手性领域未来发展的研究议题中,必定会包含对这些谜题的解答。他正在和万群合作组织2022年7月份世界生物力学大会上关于细胞手性和打破对称性主题的讨论单元[21]。“这一领域仍然是个新鲜话题,这也是我们喜欢它的原因”, Bershadsky说,“事实上绝大多数动物是两侧对称的,这也是我们不太容易理解的”,“对称性上的偏差,某种意义上是大自然更改了对称性的编码公式,错乱的编码造就了不对称之美。(我们所见的)不对称不是随机发生的,能够很好地遗传给后代,并精密地调控”。
参考文献
[1]
[2] (16)00056-7
[3]
[4]
[5]
[6]
[7]
[8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
[16]
[17]
[18]
[19]
[20]
[21]
本文经授权编译自TheScientist 2月刊封面特别文章 https://www.the-
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 