阅读:0
听报道
为什么在医学日新月异、各种治疗手段非常先进的现代社会,我们对付COVID-19这类传染病仍然如此捉襟见肘,狼狈不堪?当新冠来袭的时候,医药武器库里仍然拿不出能有效与病毒对抗的武器?
当人们从最初的惊慌中镇定下来,瑞德西韦(Remdesivir)走入了人们的视线。这款抗病毒新药从2020年初在武汉光速启动临床测试,到当年10月22日FDA正式批准用于新冠治疗,历经曲折而终成正果。已有许多媒体报道了它在抗新冠病毒中的临床研发历程。
今天的文章讲述了“人民的希望”背后的故事。读完后,也许你会得出自己的答案。
撰文 | 志言
2020年伊始,新型的致命肺炎席卷全球,病人接连死去。面对全新的病毒,医生、科学家一时束手无策。
1月,美国第一例正式记录的新冠病例接受瑞德西韦“同情用药”,病情好转。
同时,武汉启动瑞徳西韦治疗新冠的随机双盲三期临床试验。
5月,FDA批准瑞德西韦紧急使用授权(EUA)。
10月,FDA批准瑞德西韦,用于治疗COVID-19。
在现代药物开发历史中,可以说没有任何药物像瑞德西韦这样,以如此快的速度大规模接受临床测试,在数月之内得到FDA紧急授权以及正式批准——这是前所未有的。
诞生之地:吉利德科学
故事从瑞德西韦的诞生之地 “吉利德科学” (Gilead Sciences)说起。
“吉利德科学” 由Michael Riordan博士于1987年创立。与许多具有传奇性的人物一样,吉利德科学也是一个传奇的公司,在它的成长过程中,充满了各种阴差阳错与机缘巧合。
Michael Riordan本科就读于圣路易斯华盛顿大学,获生物学与化学工程双学位。他的祖父母在日本相识,因此他对亚洲产生了兴趣。大学毕业时,Michael申请了一项去东亚地区(日本与菲律宾)工作的奖学金。在菲律宾的一年时间里,他在一个类似于饥民救济站的地方工作,染上了登革热(Dengue)病毒,几乎丧命。游学结束后回到美国,他决定去学医,考入约翰·霍普金斯医学院,毕业后又对医疗公共政策感兴趣,就去哈佛商学院读了个MBA,然后又想赚钱,去了加州的投资公司Menlo。后来,在公司同事的帮助下,Michael融资两百万美元,创立了一个名叫Oligogen的公司,想要利用当时方兴未艾的反义多聚核苷(anti-sense oligonucleotide, ASO)理论与技术来调节细胞内mRNA的含量,以治疗疾病。
什么是反义多聚核苷理论?
这个听起来炫酷的名词与生命的中心法则密切相关。中心法则是指遗传物质由DNA转录到mRNA(信使RNA),再由mRNA翻译成为蛋白质,发挥各种功能。当错误的或不需要的蛋白质累积过多,就会导致许多疾病,如癌症和其他遗传性疾病。如果从mRNA入手来调节这些蛋白质的含量,就能从根本上治疗这类疾病。而mRNA是单链多聚核苷酸,人们就设想,如果设计另外一条与之配对的反义链,就能够特异性地结合单链mRNA,阻止其翻译成为蛋白质,从而降低目标蛋白质的含量。这个设想就叫反义多聚核苷理论。
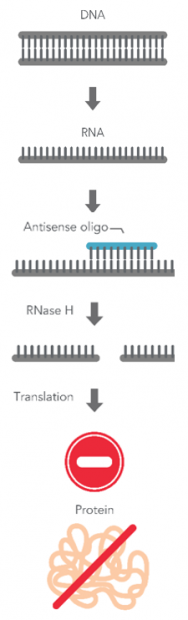
反义多聚核苷(ASO)原理:用反义链结合mRNA,致使其不能翻译成蛋白质。
来源:(图片经修改)
反义多聚核苷理论自提出以来,技术发展并不算十分成功,但却催生了核糖核酸干扰(RNAi)技术:美国科学家Craig Mello 以及 Andy Fire 偶然发现双链RNA干扰现象以及细胞内部的天然RNAi 通路与一系列调节分子,获得了2006年诺贝尔生理学或医学奖。接下来发现的microRNA现象与机制也足以获颁另外一个诺奖。不过这都是题外话,暂且不表。
理想是丰满的,现实是骨感的。Michael Riordan 博士寄予厚望的反义核苷(酸)药物开发遇到了一个几乎不可逾越的障碍:药物输送。若想达到调节目标mRNA的特异性,反义多聚核苷ASO的碱基数要达到20个,分子量太大,且水溶性强,不容易透过脂溶性的细胞膜。除此以外,药物的体内稳定性也成问题,许多设想与药物开发项目在初始阶段举步维艰。
几年后,Michael 将公司改名为“吉利德科学”(Gilead Sciences,以下简称“吉利德”。这个名字来源于圣经上的一个叫Gilead的地名,在今天的约旦国,出产一种沉香膏,可以治疗疾病) ,并将其在ASO方面的知识产权和在研药物全部转让给了加州的另外的一家公司伊西丝制药(ISIS pharmaceuticals)。多年后,因与突然壮大的伊斯兰极端组织重名,公司不得不更名为伊奥尼斯制药(Ionis pharmaceuticals)。Isis/Ionis 对ASO技术不离不弃,对ASO药物进行了大量的化学修饰及改造,后来也有收获,做出了几款上市药物。
前体药物:新药开发史上的经典
也许是由于在菲律宾患不幸罹患过登革热,Michael一直对抗病毒药物的研发耿耿于怀,一直将这一领域作为公司的主要研发方向。恰逢上世纪80年代后期到90年代初期,科学界将分子生物学技术应用于病毒学领域,极大促进了对病毒的分子与基因学本质的认识。其中非常重要的进展是逐渐了解了HIV(艾滋病病毒)与HCV (丙型肝炎病毒)两种病毒的编码基因、相关蛋白质的功能,以及它们的生命周期。人们认识到,HIV与HCV都是RNA病毒,它们都需要一个病毒基因本身编码的“RNA 依赖性的RNA聚合酶”(如HCV)或者DNA 聚合酶 (如HIV)来进行自我复制与繁殖。而我们体内没有这些聚合酶,因此很容易筛选出对这些酶有特异性抑制作用的化合物,达到药物开发过程中对于靶点蛋白的选择性,并且达到足够的治疗窗口。
因此,制药业开展了大量的筛选工作,寻找针对这些酶的小分子抑制剂。无独有偶,之前吉利德公司积累了大量ASO药物开发过程中的核苷类化合物,正好成为这类聚合酶抑制剂的重要开发基础。因为这些聚合酶的底物就是以四个碱基(我们通常所说的ATGC)为不同基团的三磷酸核苷,而科学家们发现的许多核苷类抑制剂,其工作原理其实是与天然的核苷酸竞争聚合酶上的催化位点,或者以假乱真,导致错误的反义链生成。
可惜,药物输送仍是个绕不过去的难题。以上发现都是在体外试管反应中的发现,当实验进入细胞模型中的时候,问题来了:这些化合物往往水溶性太大,无法进入细胞内。这时候,科学家们想出一个办法,合成出这些磷酸核苷类化合物的前体药物,加入了一个脂溶性基团,当药物进入细胞内后,利用细胞内的相关催化酶去掉这些脂溶性基团,代谢成为目标药物。
可是这个问题解决后,新问题又来了:这样的药物往往无法口服,因为口服后要经过肠细胞吸收,在肠细胞代谢成为目标药物后,无法再次进入全身循环。科学家们又想出了新的办法:开发肝细胞特异性的前体药物,因为肝细胞内药物代谢酶(如羧酸酯酶Carboxylesterase和氨基磷酸酯酶Phosphoramidase)的高表达可以让一些前体药物只有进入肝细胞后才能够高效生成目标药物[8, 9]。
这些药物研发的思路与实践极大促进了现代抗丙肝病毒HCV药物的诞生。这其中既有关键科学家的智慧、勇气与坚持,也有科学发现上的偶然与运气。
如上所述,丙肝病毒HCV复制与繁殖依赖于RNA依赖性的RNA聚合酶。大家发现了核苷类似物的抑制作用,也产生了“前体药物”的想法。在前人工作的基础上,Pharmasset 公司(法莫赛特公司)的化学家Michael Sofia 在抗HCV药物研发中做出了重要突破。Sofia及同事利用前体药物的思路,最终开发出了抗HCV的药物索非布韦(sofosbuvir),商品名索华迪(Sovaldi) [9]。Michael Sofia 也因此获得了2016年的拉斯克临床医学奖(相当于美国的诺贝尔医学奖,化学家获得此奖比较少见)。索华迪可以口服,耐受性良好,临床上疗效显著,一个疗程在大部分病人(>90%) 上可以达到功能上的治愈(疗程结束6个月之内仍然无法检出病毒RNA),成为抗HCV核苷类前体药物开发的里程碑。(详见《肝神在上:谁能拯救七千万慢性丙肝病患?》)
2014年,当索华迪在FDA待批的时候,吉利德公司孤注一掷,以114亿美元的高价收购了法莫赛特公司。不出意外,索华迪获得FDA批准上市,吉利德在美国推出了一个疗程定价8.4万美元的丙肝治疗方案,2015年全年销售额就达到了191亿美元。此后,由于病人数量(主要是美国)直线减少,索华迪销售额也逐年下降,但这次收购仍然为吉利德带来了大约500亿美元的销售额(当然这里面大部分都是利润)。
与许多其它抗感染类药物的命运一样,索华迪治愈了丙肝,但同时也失去了病人与生意。到了2019年,吉利德丙肝业务销售收入从峰值的191亿美元降到29亿美元,幸亏有HIV药物销售勉力维持(需要长期甚至终生服用),整个公司的销售业绩才不至于一落千丈。但资本是势利的,公司股价一路下滑,虽然用大把现金持续回购股票,仍然难挽颓势。这也迫使吉利德不断选择另外的生长点,包括oncology (肿瘤)、NASH(非酒精性脂肪肝)、CART (细胞疗法)的研发等。
有意栽花,无心插柳
不过,抗病毒一直是Gilead的主业。公司一直保持着抗新发病毒的研究项目,但总是走走停停,一时也看不出明显的业绩。2014年,非洲埃博拉(Ebola)疫情暴发,吉利德成立一个小组与美国NIH(国立卫生研究院)合作,开发抗埃博拉病毒的小分子化合物。
与丙肝病毒HCV一样,埃博拉也是RNA病毒,需要依赖 RNA聚合酶进行复制,因此一个明显的药物开发策略就是抑制这种酶的活性。吉利德在这方面轻车熟路,历年积累起一个专门的、以核苷类药物为主体的化合物库,因此很容易就筛选到了瑞德西韦(Remdesivir) [10]。不出意外,瑞德西韦也是一个前体药物,它进入细胞后代谢成为单磷酸核苷类似物,然后利用细胞内的磷酸激酶(kinase)变成三磷酸核苷类似物,从而发挥作用(图2)[11]。
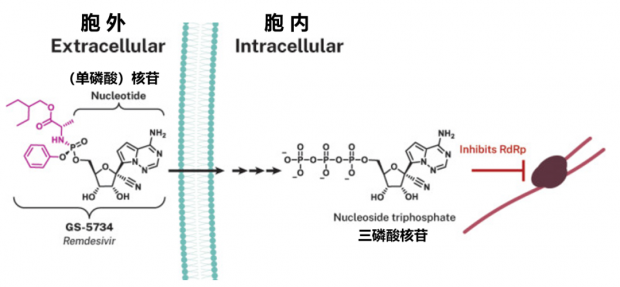
图2. 瑞德西韦以及其细胞内的活性产物。丨来源:参考文献[11]
瑞德西韦的作用也是“以假乱真”。我们可以把病毒RNA复制想象成是拉拉链:RNA聚合酶如同拉链头,以一条链为模版,将不同的核苷酸像拉链中的一个个小粒子加到被合成的另外一条链上,而瑞德西韦假冒成ATP,被加入到合成链中,但它接下来会与RNA聚合酶结合,如同在一个正常转动的齿轮上别了杠子,使得拉链头无法继续前行,合成终止(图3) [12]。
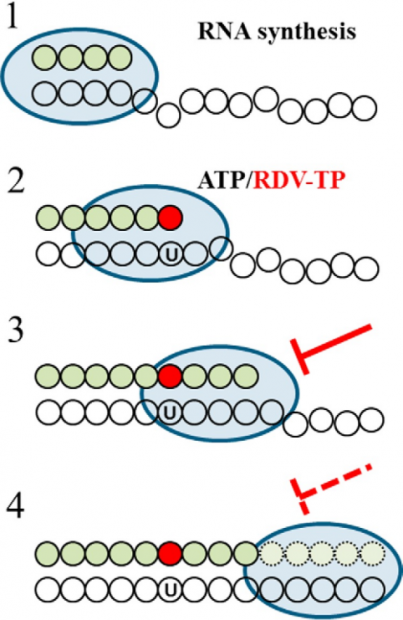
图3. 瑞德西韦抑制RNA聚合酶的原理丨来源:参考文献[12]
瑞德西韦的研发在临床前一切顺利,并且在以猴子为模型的埃博拉感染中表现出显著疗效[4],也显示出优良的安全性[5]。如前所述,它无法口服,因为经过肠细胞/肝细胞,成为活性物质后无法自由进入全身循环系统,因此只能静脉滴注。不过,埃博拉致死率很高,相比之下,给药方式已经算不上是大的问题。
不幸的是,瑞德西韦在埃博拉二期临床试验中表现不佳[5]。项目启动五年后,也就是2019年,吉利德停止了瑞德西韦用于治疗埃博拉感染的开发。虽然疗效未达预期,但有研究者认为这可能是因为给药时间太晚,毕竟与历史数据相比,也出现了有效的趋势,他们也探讨了改变试验方案继续试验的可能性。不过,因为埃博拉没有后续暴发,特别是在发达国家没有暴发,这一项目就被搁置了。
瑞德西韦问世之后,因其在埃博拉病毒临床前动物模型中表现优良,其他学者也开始注意到它的广谱抗病毒活性,希望将其用于其他抗病毒研究项目。
2014-2018年间,美国北卡来罗纳大学(UNC)、范德堡大学(Vanderbilt University)、阿拉巴马大学(University of Alabama )等机构的研究者在美国NIH的支持下,组建了一个研究冠状病毒(MERS 与 SARS)与治疗手段的联合项目,将瑞德西韦作为工具药物(图4)。

来源:
2016-2018年间,NIH的研究者测试了瑞德西韦在MERS(中东呼吸窘迫综合征)猴子感染模型中的有效性,取得了阳性(有效)结果。虽然由于种种原因(主要是疫情传播地区有限),没有启动对MERS的临床研究,但是这些相关研究的临床前成果得以发表,让人们了解到了瑞德西韦在抑制冠状病毒复制方面的药理活性[2, 3]。
2020年初,新型冠状病毒引发的疫情在全球迅速蔓延。这是一个全新的病毒,又是经呼吸传播,能够引起威胁生命的肺部炎症及多器官衰竭,而人类没有做好相应的准备,一时陷入了恐慌。
当人们镇定下来寻找对付这个病毒的武器时,早先用于抗埃博拉病毒的瑞德西韦进入人们的视线。与埃博拉病毒相似,新冠病毒SARS-CoV2也是RNA病毒,其复制与繁殖也依赖于同类RNA聚合酶,而新冠病毒的RNA聚合酶与埃博拉病毒的聚合酶高度同源。
更为重要的是,瑞德西韦也能够强效抑制SARS以及MERS病毒的RNA聚合酶[2, 3],而后两者与SARS-CoV2的RNA聚合酶几乎一模一样。
因此,从理论上推测,瑞德西韦应该对SARS-CoV2的复制与增殖也有高度抑制作用。
2020年1月19日,美国正式记录到第一例新冠肺炎的确诊病例,在华盛顿州,病人有武汉旅行史,入院数天后情况急剧恶化。主治医生Dr. George Diaz在与CDC讨论中得知了瑞德西韦这个在研药物,他查阅文献并与相关研究者联系,获知了瑞德西韦的临床前与临床研究数据,特别是对SARS/MERS/Ebola的药理学动物试验数据,认为值得一试,便联系了吉利德与FDA,快速申请了同情用药许可。
经FDA连夜紧急批准,吉利德当天将药物寄达医院,于1月27日开始给病人用药,第二天即见到明显疗效。随后,这一病例迅速发表于新英格兰医学杂志(NEJM)[6]。这是瑞德西韦第一次用于临床新冠病人,虽说孤证不立,但是也引起了全球瞩目,中国媒体一度称之为“人民的希望”。
与此同时,北京中日友好医院的曹彬教授团队也在文献中看到了瑞德西韦的治疗潜力,联系到吉利德的中国部门,在武汉传染病医院光速启动了随机双盲安慰剂对照的三期临床实验。接下来发生的一切已载入史册,无需赘述。
虽然由于种种原因,中国的临床试验未能证实瑞德西韦在受试病人中的有效性,但该试验本身设计严谨,结论可靠,也提供了非常有用的信息——那就是瑞德西韦治疗严重的Covid-19晚期病人疗效有限[13]。
这一结果与药物的作用原理也是一致的:一方面,瑞德西韦在细胞内积聚一定的浓度需要时间,另一方面,它的作用是抑制病毒的复制与繁殖,但无法清除已经存在的病毒(体内的病毒需要病人的免疫系统来清除)。另外,该药的作用是抗病毒,而对病毒已经导致的身体病理变化(如肺部的炎症与多器官衰竭等)无能为力,因此在一定时间内无法阻止病情的恶化,所以用药越早越好,对后期病人效果可能不佳。如同一座失火的房子,早期起火原因可能是汽油或者电线短路,当后期已经引燃了房子的建筑材料,再干预起火原因已无济于事。
5月22日,新英格兰医学杂志发表了《瑞德西韦用于治疗Covid-19的初步报告》[7],最终确认了瑞德西韦的疗效。文章全面系统地报道了有1063名住院新冠病人(需要非创伤性吸氧支持)参与的多中心随机对照双盲试验,试验主要结果表明,接受瑞德西韦治疗的病人比安慰剂对照组恢复时间缩短四天,治疗组与安慰剂组的死亡率分别为7.1%与11.9%,显示了瑞德西韦能够一定程度上降低死亡率,也就是说,每治疗1000个这类病人,会挽救大约48个人,副作用方面两组没有差异。
试验结果有力地证明了瑞德西韦治疗新冠病人的安全与有效性。FDA根据这一结果批准了瑞德西韦应用于新冠的紧急治疗。稍后,吉利德也公布了瑞德西韦治疗轻度或中度住院病人(有肺炎症状,但是不需要吸氧)的初步结果,结果显示瑞德西韦可以改善病情,防止病情进展,降低死亡率[14] 。10月22日,FDA正式批准瑞德西韦用于新冠治疗,商品名Veklury。值得一提的是,在十月份发表的一项由WHO主持的、关于瑞德西韦应用于住院病人的大规模三期临床试验(SOLIDARITY)揭示,虽然与安慰剂组相比,用药组显示出死亡率降低的趋势,但差异并不显著[15]。这虽然令人失望,但是如上所述,这可能与入组病人的严重程度或者异质化太大有关,后期抗病毒已经不是主要矛盾,作为单纯的抗病毒药物,瑞德西韦无力回天。而抗炎药如地塞米松(Dexamethasone),Baricitinib (JAK-1 inhibitor) 在后期的治疗中则可以起到更好的作用。这写数据并不能否定瑞德西韦的临床作用,而是帮助我们更好地理解这个药物,根据病人具体情况来考虑用药时间。
瑞德西韦与吉利德:历史的选择
为什么在医学日新月异,各种治疗手段非常先进的现代社会里,我们对付COVID-19这类传染病仍然如此捉襟见肘,狼狈不堪?与1918年一样,人类的武器库里仍然拿不出足够与病毒对抗的武器?
表面上看,这是因为新冠病毒突然出现、突然袭击,传染性很强,而人类却对它知之甚少。
但这背后还潜藏着深层的原因。
自二战结束以来,以青霉素为代表的抗生素的出现成为现代文明最为重要的标志之一。抗生素的出现让人类彻底告别了惧怕细菌感染的年代,将人类的平均预期寿命提高了20年以上,同时也为一些制药公司注入了新的活力,发展出新的增长点。今天的一些大型制药公司如默克(Merck)、 辉瑞(Pfizer)、礼来( Eli Lilly)、施贵宝(BMS)等无一不曾受惠于抗生素发展的黄金时代。但是,由于细菌感染病程短,抗生素领域竞争越来越激烈,许多制药公司便将重金投向利润更高的慢性疾病领域,如胃病、心血管疾病、代谢性疾病、癌症等。不过,在上世纪末,这些公司往往还保留着“抗感染性疾病”这一研究部门,其中一半做细菌,一半做病毒。但是,进入本世纪后,事情发生了变化。
大约2001年,施贵宝研发部门重组,大幅削减了感染病部门。2004年到2005年间,礼来裁减感染病部门,将一款很有前景的抗HCV药物拱手送给了福泰制药(Vertex),这款药物就是后来的丙肝药物特拉匹韦(telaprevir/Incivek)。2000至2010年间,辉瑞先后合并Warner-Lambert (2000年)、法玛西亚(Pharmacia,2003年)、惠氏(Wyeth,2009年),并且逐渐将所有这些公司以及自己的感染病部门全部裁撤。
罗氏(Roche)也是抗病毒小分子研究的先驱,许多小分子抗HCV核苷类药物都是罗氏首创,但在2009年合并基因泰克(Genentech)后,罗氏关闭了许多部门,包括在新泽西的一个主要研发总部,小分子研发受到重创。诺华(Novartis)也于近十年间逐渐将感染病部门全部关掉。其余大型制药公司,包括默克 (Merck)、艾伯维(Abbvie)、赛诺菲(Sanofi)等也是关停并转。
因此,等到2020年的时候,放眼望去,研发新型抗生素的大型制药公司几乎绝迹,研究抗病毒的公司也只有吉利德了,可谓是千顷地里一颗独苗。正所谓天下熙熙皆为利来,天下攘攘皆为利往,感染性疾病疗程短,发达国家病人少(得益于公共卫生的改善与疫苗的普及),研发相关药物无法获得足够的回报,而可以赚钱的抗病毒方向,要么错过,要么是难啃的硬骨头,最终的结局就是大家普遍认为做抗感染药物不赚钱,或者投入产出不成比例,而无一例外地放弃了对这一领域的药物开发。
与历史上许多伟大药物的发现过程一样,瑞德西韦用于新冠治疗也是纯属偶然:如同《我不是药神》中的格列卫(Glivec)与大放异彩的免疫检查点抑制剂Keytruda 一样,都是被从垃圾桶里捡回,开发之初都是来自不同的适用症 (格列卫最初只是泛泛的蛋白激酶抑制剂,Keytruda来源于对自身免疫性疾病的药物开发,此处不再展开)。无论如何,在本次新冠疫情中,我们还是应该庆幸瑞德西韦的存在——如果用药得当,“人民的希望”是无愧于“新冠治疗的一缕曙光”的称号的。
毋庸置疑,本次新冠大流行为当今世界带来了一场巨大的灾难。同时也带给我们许多思考,应对这样的公共卫生危机,传统的商业药物开发模式没有起到作用。吉利德开发瑞德西韦治疗埃博拉,主要也不是出于商业目的,而是丙肝药物暴利后对抗病毒药物不计成本的全面投入。同样的道理,如果这次政府管控瑞德西韦,导致吉利德公司赚不到钱(现在看来确实如此),也会打击制药界开发抗病毒药物的积极性,等下一次疫情来临,人类还将面临无药可用的处境。
《诗经》云:“迨天之未阴雨,彻彼桑土,绸缪牖户。”防患于未然永远是上上之策。放在药物研发上来说,我们的理想境界是药等病,而非病等药。但是,做生意是要赚钱的,如何平衡这两方面的矛盾,应该是公共政策制定方与业界共同考虑的问题。
另外一方面,要对付新冠这种危害极大的感染性疾病,最为有效的手段还是“治未病”——即安全有效的疫苗。现在,瑞德西韦与其它药物的联合使用,以及新冠病毒的高效单克隆抗体也已经应用于临床[16]。2020年12月,由BioNTech/Pfizer与Moderna研制的mRNA疫苗也被FDA批准紧急使用(两款疫苗在数万人参加的三期临床试验中均取得了近95%的保护效力,并没有出现严重的无法耐受的副作用)。正所谓,沉舟侧畔千帆过,病树前头万木春,我们正利用科学知识来逐渐获得与掌握对付新冠病毒的利器,最终彻底消除Covid-19,让我们的生活回归正常。
参考文献
[1] Tchesnokov EP, Feng JY, Porter DP, Gotte M. Mechanism of Inhibition of Ebola Virus RNA-Dependent RNA Polymerase by Remdesivir. Viruses 2019;11.
[2] Agostini ML, Andres EL, Sims AC, Graham RL, Sheahan TP, Lu X, Smith EC, et al. Coronavirus Susceptibility to the Antiviral Remdesivir (GS-5734) Is Mediated by the Viral Polymerase and the Proofreading Exoribonuclease. mBio 2018;9.
[3] Sheahan TP, Sims AC, Graham RL, Menachery VD, Gralinski LE, Case JB, Leist SR, et al. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses. Sci Transl Med 2017;9.
[4] Warren TK, Jordan R, Lo MK, Ray AS, Mackman RL, Soloveva V, Siegel D, et al. Therapeutic efficacy of the small molecule GS-5734 against Ebola virus in rhesus monkeys. Nature 2016;531:381-385.
[5] Mulangu S, Dodd LE, Davey RT, Jr., Tshiani Mbaya O, Proschan M, Mukadi D, Lusakibanza Manzo M, et al. A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics. N Engl J Med 2019;381:2293-2303.
[6] Holshue ML, DeBolt C, Lindquist S, Lofy KH, Wiesman J, Bruce H, Spitters C, et al. First Case of 2019 Novel Coronavirus in the United States. N Engl J Med 2020;382:929-936.
[7] Beigel JH, Tomashek KM, Dodd LE, Mehta AK, Zingman BS, Kalil AC, Hohmann E, et al. Remdesivir for the Treatment of Covid-19 - Preliminary Report. N Engl J Med 2020.
[8] Coats SJ, Garnier-Amblard EC, Amblard F, Ehteshami M, Amiralaei S, Zhang H, Zhou L, et al. Chutes and ladders in hepatitis C nucleoside drug development. Antiviral Res 2014;102:119-147.
[9] Sofia MJ. Nucleotide prodrugs for HCV therapy. Antivir Chem Chemother 2011;22:23-49.
[10] Siegel D, Hui HC, Doerffler E, Clarke MO, Chun K, Zhang L, Neville S, et al. Discovery and Synthesis of a Phosphoramidate Prodrug of a Pyrrolo[2,1-f][triazin-4-amino] Adenine C-Nucleoside (GS-5734) for the Treatment of Ebola and Emerging Viruses. J Med Chem 2017;60:1648-1661.
[11] Eastman RT, Roth JS, Brimacombe KR, Simeonov A, Shen M, Patnaik S, Hall MD. Remdesivir: A Review of Its Discovery and Development Leading to Emergency Use Authorization for Treatment of COVID-19. ACS Cent Sci 2020;6:672-683.
[12] Gordon CJ, Tchesnokov EP, Woolner E, Perry JK, Feng JY, Porter DP, Gotte M. Remdesivir is a direct-acting antiviral that inhibits RNA-dependent RNA polymerase from severe acute respiratory syndrome coronavirus 2 with high potency. J Biol Chem 2020;295:6785-6797.
[13] Wang Y, Zhang D, Du G, Du R, Zhao J, Jin Y, Fu S, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet 2020;395:1569-1578.
[14]
[15]
[16]
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 