1882年3月24日,德国微生物学家科赫(Robert Koch)宣布发现了结核病的病原体:结核分枝杆菌。1921年6月,法国细菌学家卡尔梅特(Albert Calmette)与其助手介兰(Camille Guérin)培养牛分枝杆菌而研发的结核疫苗第一次应用于人体,这便是以两人名字命名的“卡介苗”(Bacille Calmette-Guérin vaccine,简称BCG)。
如今,卡介苗问世已过百年,仍是目前唯一被批准用来抗击结核病的疫苗。但结核这个恶魔却从来没有被彻底打败过。几十年来,科学家一直在努力开发更好的选择。在试验了几十种方法,经历了多次临床失败后,研究人员表示,第二种肺结核疫苗有望上市。丰富的渠道,大量的候选疫苗,让战胜结核充满了希望。
撰文 | Anthony King
编译 | 咸姐、Idobon
1921年7月18日,一名婴儿在巴黎呱呱坠地。他的母亲分娩不久便死于结核分枝杆菌(Mycobacterium tuberculosis,Mtb)的感染,照顾他的祖母也患有结核病(tuberculosis ,TB)。为了保护这名新生儿,医生为他接种了一剂活的牛分枝杆菌,这便是人类历史上第一名接种卡介苗的婴儿。
如今,全球每年有1亿多新生儿接种卡介苗,主要集中在发展中国家。这一举措可以挽救数万人的生命。但是,卡介苗提供的保护仍然是不完全的,结核病仍然是这个星球上的头号传染病杀手。据估计,在过去的200年里,结核夺走了约10亿人的生命,仅2019年就有140万人命丧于此。现在,医生们拥有可以治疗结核病的抗生素,却也使得这个“巨大的负担”变得更加不幸——因为我们似乎开始忘记,结核病是一种瘟疫。
卡介苗的缺点
儿童感染结核常见于肺部以外,可能以粟粒性结核和结核性脑膜炎的形式出现。前者会影响多个器官,若不及时上抗生素治疗几乎就是致命的;后者则是因为大脑和脊髓周围的膜受到了感染。卡介苗最大的优点就是可以预防这些感染。新生儿接种卡介苗,能够可靠地预防结核杆菌在儿童间的传播。
而超过90%的结核病例则是青少年和成年人,表现为我们熟知的肺结核。这是一种严重的肺部疾病,可引起胸痛或咳血。卡介苗为肺部提供了更多样化的保护,但出于某些原因,比起其它结核,卡介苗预防肺结核的效果却差一些。
奇怪的是,卡介苗对青少年和成年人的保护力度存在地域差异:在斯堪的纳维亚和其他高纬度地区,卡介苗有很好的效果,但对靠近赤道的人群保护力却较弱。一个最受认可的解释是,赤道地区有一些不同种类的分枝杆菌,它们可以触发人体产生免疫记忆,从而使身体能够识别出卡介苗,并减少卡介苗的复制。这种解释有一个有力的流行病学证据:世界上卡介苗效果不佳的地区,人们接触非结核分枝杆菌的几率往往也是最高的。
更复杂的是,结核分枝杆菌可以在人体内潜伏数十年。全球大约有20亿人可能感染了这种病菌,当时机一到,例如免疫系统受到抑制时(艾滋病患者中很常见的情况),结核杆菌就会激活,使人生病,并很容易通过空气传播感染其他人。
理解这些动态过程的关键在于了解免疫反应。结核分枝杆菌与人类已共存了数千年,它已经进化出了一套“分子把戏”来逃避我们的免疫雷达,甚至在被检测到时还能够减弱免疫反应以求自保。伴随着人们的呼吸,空气中的结核杆菌进入肺部,吸引了在肺里“巡逻”的免疫细胞:肺泡巨噬细胞。
结核分枝杆菌有一层蜡状的厚层霉菌酸构成的囊状结构,不易被免疫系统识别。当巨噬细胞认出并吞噬了结核杆菌,躲在“蜡囊”中的结核杆菌可以阻止吞噬溶酶体成熟,这样它们就不会被杀灭,甚至还能复制。同时,结核杆菌还会干扰抗原递呈,使“前线”的免疫细胞无法向辅助T细胞传递结核杆菌的信息,推迟保护性T细胞做出反应,并限制T细胞启动后的效应。
可以说,巨噬细胞无意中为结核杆菌提供了它们所渴望的“庇护所”——在巨噬细胞内,结核杆菌正好可以免受抗体的袭击。
至此,人体最终将结核分枝杆菌隔离在一种叫做“肉芽肿”的免疫细胞群中,犹如一颗“定时炸弹”,等待你的防御系统崩溃的那个最佳时机。
当然,并非所有情况都很严重。大多数感染了结核杆菌的人都不会发病,只有5%-15%的人会患上结核病。毕竟结核与人类之间经历了如此长时间的斗争和博弈,已经建立了输赢的平衡。
徒劳的探寻:结核免疫的指标究竟是什么?
卡介苗虽然已经用了一百年,但其实科学家并没有完全弄清楚它究竟是怎样调动免疫系统保护孩子们的,也没有弄清楚成年人到底要产生什么样的免疫反应,才算接种成功。与大多数疫苗一样,卡介苗在刺激抗体产生这方面比激发强大的T细胞反应这方面要强得多。几乎所有的疫苗都是通过产生中和抗体来起作用的,但是对于结核而言,中和抗体的作用似乎远远不够。
保护性关联值(correlates of protection,CoP)是评估疫苗效力的一组指标。只有当数千人规模的安慰剂对照试验(即临床3期)取得成功时,才可能挖掘、制定出这些指标。然而,在结核病患者的血液中,却找不出任何指标能表明“这位患者已经打过疫苗、受到疫苗保护”。
多年来,科学家们一直认为,卡介苗所引发的T细胞的强烈反应是抵抗结核病的关键,它能消灭感染了结核杆菌的细胞。大量研究也显示,CD4+ T细胞(也叫TH1细胞)对控制感染、预防传播性疾病是必不可少的。然而,CD4+ T细胞越多,却未必等于抗结核病的能力越强,因此难以将它的丰度作为评估疫苗效力的指标。另外,近年来,人们认为产生促炎细胞因子的辅助性T细胞17(也称Th17细胞)也可以保护人体。
为了研制一种能够有效招募并激活T细胞的疫苗,牛津大学的Helen McShane团队利用一种改良的安卡拉牛痘病毒(MVA)作为载体来传递结核抗原,命名为“MVA85A疫苗”。据McShane回忆,在早期临床试验中,MVA85A疫苗激发了理想中正确的免疫反应——CD4+ T细胞被诱导了出来,分泌了干扰素γ、肿瘤坏死因子和白细胞介素-2。然而,南非的一项婴儿试验缺表明,加种MVA85A疫苗并没有显示出比仅接种卡介苗更有效的抗结核效果。这可能意味着,研究人员搞错了方向、找错了CoP指标。最终,McShane团队总结道, MVA85A疫苗诱导的T细胞反应水平不足以增强卡介苗接种后的保护作用。
伦敦卫生与热带医学学院的免疫学家Hazel Dockrell认为,我们不应忽略结核病首先是一种呼吸道感染,然而现在的研究却几乎总是盯着血液中发生了什么。这并不能帮助我们了解肺里发生了什么。也许肺里存在着可能对抗结核的关键特殊细胞呢。
卡介苗
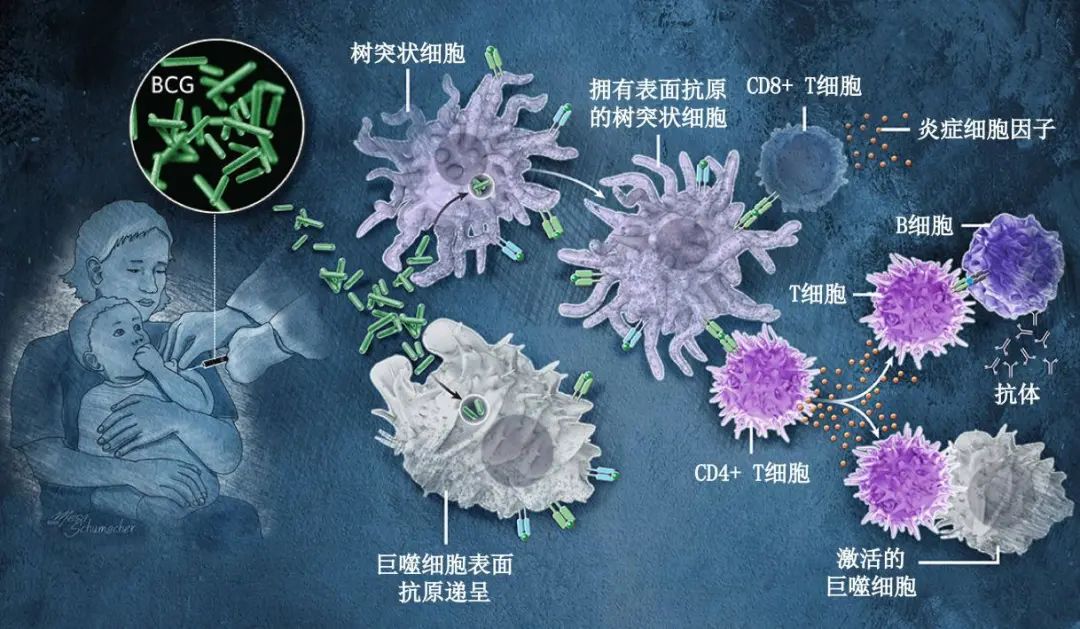
已有百年历史的卡介苗是一种活的、但是弱化了的牛分枝杆菌,与结核分枝杆菌(Mtb)相关。接种卡介苗会将“前线”免疫细胞吸引至注射部位,树突状细胞和其他抗原递呈细胞会在它们的表面呈现卡介苗中细菌的部分,从而驱动T细胞作出反应,以对抗未来病原体的感染,同时促使B细胞产生抗体。卡介苗和结核分枝杆菌都会进入被称为吞噬体的囊泡,不同的是,卡介苗最终会降解,而结核杆菌则能在巨噬细胞内长期存活。
正在研发中的结核疫苗
目前已有十几种结核病疫苗正在进行临床试验,虽然新的结核疫苗可能还无法防止感染,但有些疫苗已经可以阻止带菌者发展为结核病。必须承认的是,阻止感染一直是疫苗成功的“圣杯”,但这其实是个非常非常高的标准,因此,将标准稍微变通一下也未尝不可——比如,阻止感染者发展为结核病,就可以作为一个评判疫苗标准。毕竟,在几乎所有的结核病疫苗试验中,受试者都接种过卡介苗,并感染了潜伏的结核病。
领跑的在研疫苗
目前有两种候选疫苗正在进行临床3期试验,还有八种疫苗紧随其后,处于临床2期试验阶段。再往前,有三种疫苗处于1期试验阶段(未显示),还有少数临床前候选疫苗正在争取进入人体试验阶段。
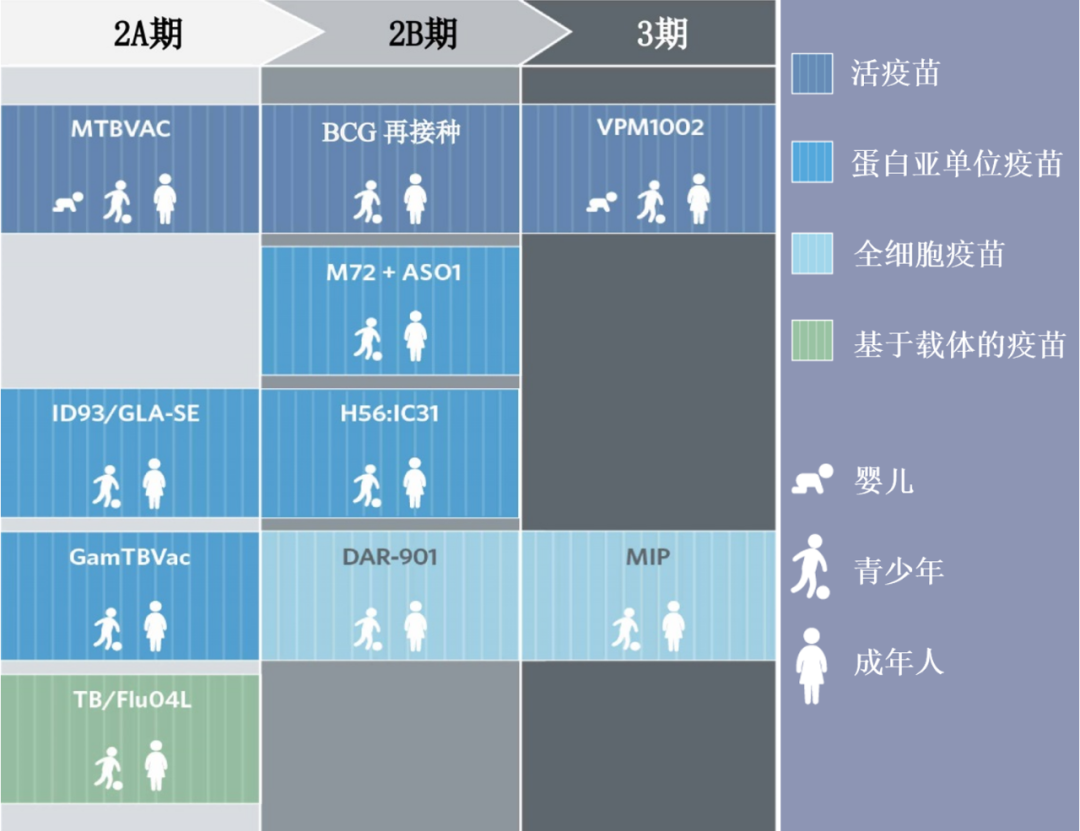
活疫苗
VPM1002:活的减毒卡介苗,含有另一种细菌的成孔蛋白,可使抗原和分枝杆菌DNA从吞噬体进入细胞质
BCG再接种:再注射一针卡介苗
MTBVAC:带有毒性基因突变的、活的、遗传上减弱的结核分枝杆菌(是此类疫苗中第一个也是唯一一个进入临床试验的)
蛋白亚单位疫苗
M72 + ASO1:由两种结核分枝杆菌抗原和一种佐剂组成的重组融合蛋白
H56:IC31:由两种早期分泌蛋白、一种潜伏蛋白以及一种佐剂组成的蛋白质疫苗
ID93/GLA-SE:四种结核分枝杆菌毒性抗原与一种佐剂的融合
GamTBVac:融合两种结核分枝杆菌抗原和一种佐剂的亚单位疫苗
全细胞疫苗
DAR-901:布氏杆菌(Mycobacterium obuense)的灭活制剂,不引发疾病
MIP:由分枝杆菌 M. indicus pranii组成的灭活疫苗,该菌生长迅速,不会引起疾病
基于载体的疫苗TB/Flu04L:经鼻给药、含有结核分枝杆菌两种抗原、减毒、活流感病毒
大多数结核病候选疫苗都是在青少年和成年人中进行试验。不过有两种疫苗值得关注,那就是处于2A期临床的MTBVAC疫苗和处于3期临床的VPM1002疫苗。它们可以同时在成年人以及婴儿、新生儿中进行试验,并且可能对免疫缺陷的艾滋病儿童特别有用。当然,如果我们能够阻止青少年和成年人感染结核病,就不用担心儿童对结核疫苗的需求了。
目前,几乎人人都在谈论的候选疫苗是葛兰素史克(GSK)正在研发的蛋白质亚单位疫苗——M72疫苗。该疫苗包含来自结核分枝杆菌的两种蛋白的融合,采用了一种名为AS01的佐剂(GSK曾将这种佐剂用于轰动一时的带状疱疹疫苗和处于行业领先的疟疾候选疫苗)。尽管M72疫苗在非人灵长类动物身上的作用看起来并不乐观,但在最近的一次涉及肯尼亚、南非和赞比亚3000多名成年人的试验中,它在3年内将肺结核的发病率降低了54%。
卡介苗是一种活的、可复制的载体,类似于自然感染结核杆菌的“缓慢进程版”。虽然卡介苗在青少年时期的保护作用减弱了,但毕竟在整个儿童时期都能有效抵御结核病。而M72疫苗的成分主要是一些蛋白质,所以早期遭到了一些学者的怀疑。他们认为,像卡介苗这种可提供足够长的免疫期以避免自然感染的疫苗才是最合适的结核疫苗。但M72疫苗提供了持续3年的保护,证明了这种想法的局限性。
华盛顿大学传染病科学家Thomas Hawn虽然没有参与M72疫苗的研发,但他认为M72疫苗的效果归功于疫苗的佐剂。AS01佐剂可以触发一种名为toll样受体4(TLR4)的先天免疫受体,从而产生强大的免疫反应,除了产生抗体的B细胞外,还会召唤T细胞。“从前,我们还没有那么高效力的佐剂。如今,有了新的佐剂,我们以更微妙的方式触发不同免疫反应的能力大大提升了。”
M72蛋白亚基疫苗
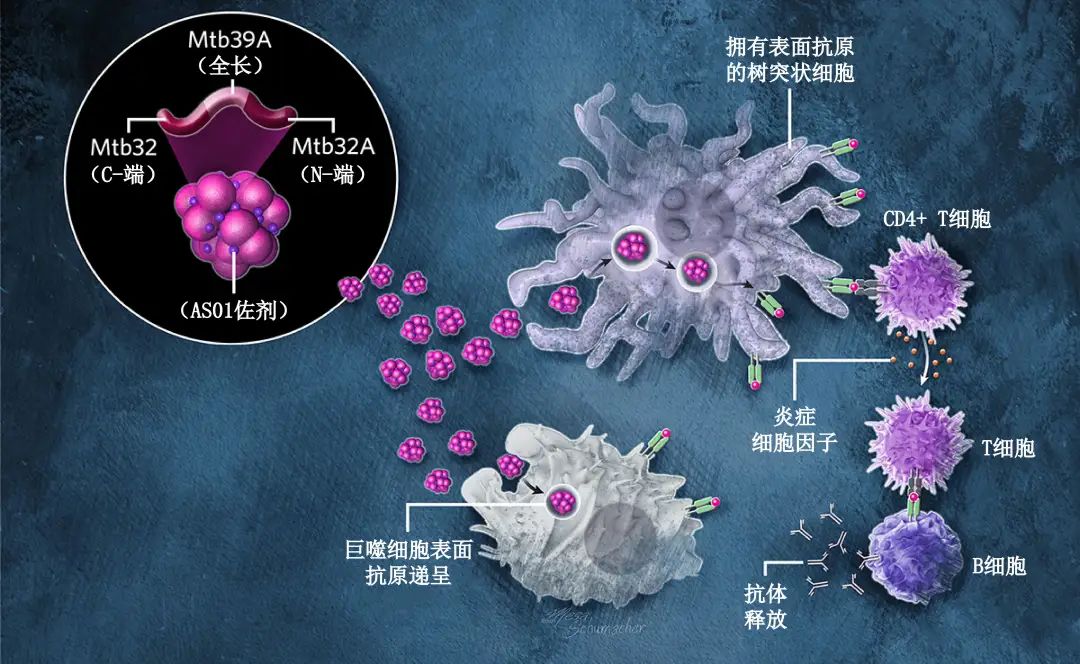
构成卡介苗的两种分枝杆菌重组蛋白融合在一起进行注射,融合蛋白被免疫细胞识别,然后显示在其表面,从而触发针对抗原的免疫反应,而葛兰素史克的一种专利佐剂(AS01)则增强了免疫反应。
但不容忽视的是,M72目前的试验规模很小,安慰剂组仅含有26例结核患者,疫苗组也只有13例结核患者。毫无疑问,想要寻求监管机构的紧急使用授权,必须先进行万人规模的试验。
与此同时,丹麦国立血清研究所正在开发两种亚单位疫苗,其主要候选疫苗H56(由三种抗原和一种新型佐剂组成)正在坦桑尼亚和南非进行2B期临床试验。另一种名为H107的亚单位疫苗,含有8种结核分枝杆菌的特异性抗原,由于这些抗原不是卡介苗所共有的,因此H107疫苗不会与卡介苗发生交叉反应,这就意味着二者可以联合使用。
但是,也有不少含佐剂的蛋白质亚单位疫苗半路夭折。它们在早期和中期试验中显得很有潜力,却最终失败了。一些科学家因此对亚单位疫苗失去了兴趣。澳大利亚昆士兰詹姆斯·库克大学的疫苗学家Andreas Kupz就是其中之一,他转而认为采用原始卡介苗的方法制作的活疫苗更具有潜力。例如,比尔和梅琳达·盖茨医学研究院正在进行一项试验,为南非10-18岁的人注射增强剂量的卡介苗。一开始,大家认为这种方法肯定无效,但试验结果却表明,在南非青少年中,此法可以预防45%的人感染继发性结核,且即使感染了6个月内也可痊愈。值得一提的是,这种方法并不能阻止感染结核杆菌(血检呈阳性),但有更多的人最终结核转阴了,感染最终被清除了。
也有一些新的活疫苗正在研发中,其中走在最前列的是VPM1002疫苗。这是一种转基因卡介苗,目前正在进行3期临床试验,由柏林马克斯·普朗克感染生物学研究所的Stefan Kaufmann牵头。Kaufmann表示,他们并不认为卡介苗很糟糕,但是希望可以改善新生儿卡介苗,使其最好也能用于成年人和青少年。他们为疫苗添加了李斯特菌产生的一种致孔蛋白(李斯特菌溶血素O)的基因。一旦结核杆菌被“前线”免疫细胞(如巨噬细胞)吞噬,它就会被隔离到吞噬小体中,而李斯特菌溶血素O则能穿透吞噬小体膜,泄露VPM1002来源的分子泄漏。这些分子出现在细胞表面,诱导CD8+ T细胞攻击感染细胞,并使DNA逃逸,触发促炎途径。
VPM1002全细胞疫苗
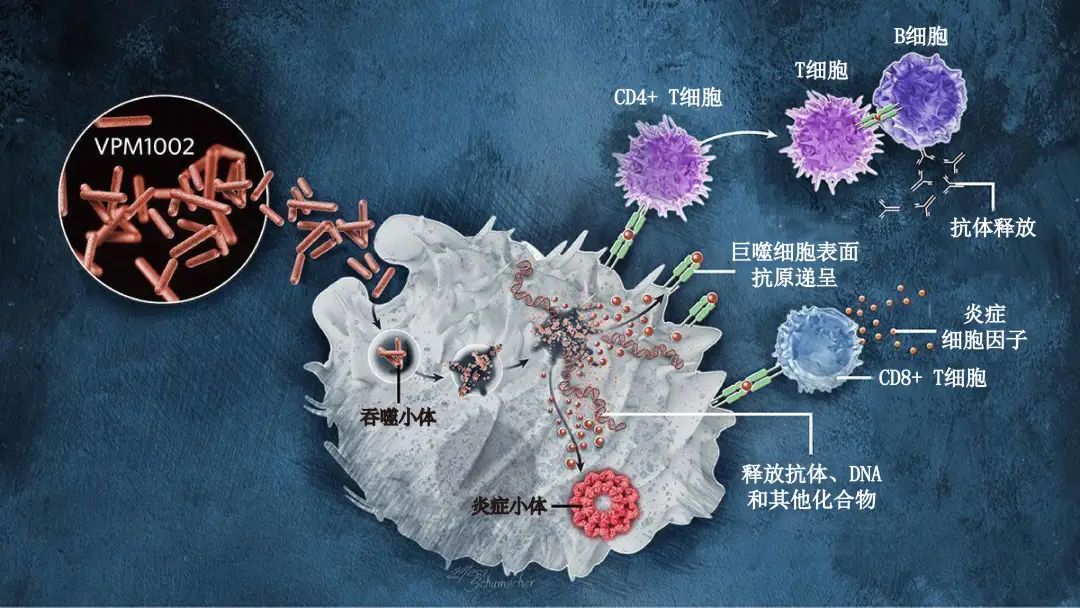
与卡介苗不同,这是一种转基因卡介苗。注射后,巨噬细胞会将其带入吞噬小体,在那里产生一种酶,以使吞噬小体的膜上形成孔隙,令抗原泄漏到细胞质中,并以类似于结核杆菌的方式激活炎症小体。
另一种候选活疫苗与卡介苗的区别更大,因为它使用的是结核分枝杆菌本身。有一种观点认为,更直接地模拟自然感染可能是疫苗的成功之路。西班牙萨拉戈萨大学的研究人员删除了结核分枝杆菌的两个致病基因以使其更安全,从而研发了改良版的MTBVAC疫苗, 现在正处于2a期试验中。MTBVAC所模拟的过程可能比卡介苗更接近于真实的结核感染,并能诱导更加相似的记忆免疫反应,从而起到更好的保护作用。
还记得本文开头提到的卡介苗的保护作用有地域差别的现象吗?上文提到,目前最有利的证据是:赤道附近的分枝杆菌数量越多,似乎就越容易降低卡介苗对成年人的效力。这意味着,同样的现象很可能会在这些新的活分枝杆菌疫苗中重演。确实,已有证据表明,对环境中的分枝杆菌的免疫反应会干扰卡介苗的效率,那么现在要关心的就是,这一点在多大程度上会成为MTBVAC和VPM1002的问题?将这些疫苗接种给终生接触分枝杆菌的老年人会发生什么不一样的事情吗?如果分枝杆菌之间的交叉反应确实会影响疫苗效力,那么蛋白亚单位疫苗或基于载体的疫苗(如McShane团队目前正在研究的疫苗)可能是更好的选择,毕竟“不要把鸡蛋都放在一个篮子里”。
消灭结核病
要想重振结核疫苗,研究人员必须考虑到,卡介苗不只可以预防结核病,还能激发免疫系统,抵御更广泛的呼吸道疾病,乃至败血症。当然,研究人员在卡介苗广泛应用后不久就观察到了这种非特异性保护作用:当时卡介苗接种不仅减少了儿童的结核死亡,还减少了其他原因造成的死亡。目前,卡介苗还被用于早期膀胱癌的免疫疗法:将其直接注入膀胱,可以触发患者的免疫系统攻击肿瘤。相应地,VPM1002疫苗在临床试验中也显示出治疗膀胱癌的潜力。
在过去十年中,研究人员逐渐揭示了这些非特异性效应的机制,发现它涉及先天免疫细胞的基因重组,这种现象称为训练免疫(trained immunity)。从本质上来说,卡介苗会给细胞留下表观遗传学印记,以便它们对随后的其他感染做出反应。一些科学家甚至推测,这种免疫防御的通用机制足以(基本)解释卡介苗为什么能对抗结核。虽然目前大多数正在研发的结核疫苗都是专门针对肺结核进行试验的,但是默多克儿童研究所及墨尔本大学的结核疫苗研究员Nigel Curtis正在领导一项跨国试验,调查接种过卡介苗的医务人员,看看卡介苗是不是也能影响新冠病毒感染。
疫苗接种
20世纪20年代,卡介苗是口服的;很快,医生们就开始皮下注射(这已经成为近一个世纪以来的标准做法)。不过现在,研究人员正在考虑新的接种方式,比如直接送入肺部和静脉注射。
牛津大学的疫苗研发人员Helen McShane表示,他们正在努力尝试将疫苗送入肺部,因为这是结核进入身体的渠道。一些动物实验数据表明,入肺是最好的保护方式,当结核疫苗通过气雾剂接种时,肺部和血液中的免疫反应更为强烈。澳大利亚昆士兰詹姆斯·库克大学的疫苗科学家Andreas Kupz也表示,当卡介苗通过鼻腔或喷雾直接进入肺部时,驻留的记忆细胞将被激活——局部记忆T细胞,也可能是记忆B细胞,时刻准备着应对特定病原体的再次出现。这些细胞似乎也受到卡介苗静脉注射的刺激,Nature杂志最近的一项研究报告指出,与接受鼻腔和皮内给药的猴子相比,静脉接种卡介苗的恒河猴的CD4+和CD8+ T细胞的应答更佳。McShane认为,静脉注射卡介苗可以让我们更多地了解那些免疫反应是必需的,这样我们就能有针对性地设计疫苗来诱导这些反应。
目前,结核疫苗的开发因新冠疫情而变得复杂。接受Science杂志采访的专家指出,一些结核疫苗试验已经推迟或放缓。如果不是新冠疫情暴发,M72疫苗的试验应该已经完成。此外,在大流行期间,很可能存在结核病例没有上报、甚至治疗滞后的情况。针对新冠病毒的全球封锁破坏了“终止结核”的计划。
事实上,根据非政府组织“遏制结核病伙伴关系”(Stop TB Partnership)的数据,结核病例最多的国家中,有9个在2020年结核病感染的诊断和治疗方面出现了数量大幅下降,降幅从16%到41%不等。该组织估计,新冠暴发12个月,抵消了全球抗击结核 12年所取得的进展。由于新冠疫情的干扰,2020年结核病的官方病例数和死亡人数可能会下降,但是2020年结核病死亡人数可能会超过新冠,因为那些未确诊的结核病患者将无法得到应有的治疗。
全球95%以上的结核病死亡发生在低收入至中等收入国家,伦敦卫生与热带医学学院的一项研究估计,基本的社会支持可以将结核病负担减少85%。人类已经适应了结核的存在,但恶劣的生活条件、贫困、过度拥挤、艾滋病毒导致的免疫功能低下,都会导致更多的疾病。世界卫生组织表示,要实施现有的结核干预措施,还存在33亿美元的资金缺口。
毫无疑问,疫苗可以成为防治结核全球战略的关键部分。倘若我们有一种疫苗能够阻止接种者因感染结核杆菌而发展成结核病,甚至,能完全阻止感染,那一定是了不起的成就。
虽然新冠疫情暂时阻碍了结核疫苗的研发,但是,新冠疫苗的研发工作中也有望出现一些“化学反应”。例如,一些研究人员就认为,对免疫系统具有强烈刺激作用的mRNA疫苗不仅非常灵活,而且具有极高的免疫原性,正适用于靶向结核病。
面对传染病中的“头号杀手”,我们需要一种更好的结核疫苗。然而,无论答案在哪里,研究人员都一定会找到它,并勇往直前,推进临床项目的进行。
本文经授权编译自TheScientist 在线杂志,链接地址:
https://www.the-
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 