1954年,人类发现第一个具有抗抑郁效果的化合物,离古希腊时代关于抑郁的医学记录已过去二十几个世纪。仅仅隔了34年,1988年,第二代抗抑郁药“百忧解”就获批上市,帮助了不计其数的抑郁症患者,但仍不能满足所有治疗需求。还需要多久,我们才能研发出第三代抗抑郁药?
撰文 | 徐亦迅
远在两千五百年前,古希腊医学之父希波克拉底 (Hippocrates of Kos) 和其著名后辈盖伦 (Galen of Pergamon) 分别倡导了影响西方医学界近两千年的四体液学说 (The Four Humors Theory)。希波克拉底认为人有四种体液:血液 (sanguine) 、黄胆汁 (choleric) 、黑胆汁 (melancholic) 和黏液 (phlegmatic),健康是各种体液相互谐调的结果,如果体液混合错误就会生病,而治疗要领就是要使体液恢复和谐的状态 (图1)。
盖伦进一步将四体液学说应用到临床,将人的脾气体质分为四类:黄胆质者勇敢精力充沛、黑胆质者固执忧郁、多血质者热情果断、黏液质者愚笨懒惰。盖伦将炎症也分为四种:来自血液之蜂窝组织炎、来自黄胆汁之丹毒、来自黏液之水肿、来自黑胆汁之癌瘤。他甚至将该学说用于发烧的分类:属血的持续热、属黄胆汁的三日热、属黏液的每日热、属黑胆汁的四日热。
图1. 希波克拉底《人的本质》一书中关于四体液学说的段落。丨来源:Jones, W.H.S.(1931) Hippocrates, Volume IV: Nature of Man。
盖伦可说是希腊医学发展的高峰,此后的医家顶多只能注释或编纂盖伦及古代医学的学说而已。与《黄帝内经》和《伤寒杂病论》主导和束缚中医的发展相类似,西洋医学在接下来的两千年里再也没有创出新机。
盖伦和希波克拉底得自临床与实验的医学假说竟成为取代事实的绝对真理,直到文艺复兴之后,才由新解剖学和细胞学说取代了早已过时的四体液学说。如今的西方医学界虽已不再谈及体液学说,但是我们在医学教科书中仍可看到“melancholia”这条术语,这无疑是四体液学说的遗迹。
希腊词根melan表“黑色”,cholia表“胆汁”,melancholia (也可拼写成melancholy或melencolia) 指因黑胆汁过多而造成的疾病 (图2),它描述的其实就是困扰当今世界近15%人群的抑郁症。
图2. 德国艺术家丢勒创作于1514年的人物版画名作:《忧郁的我》(Melencolia I)
抑郁症是一种心理障碍,又称情感性精神障碍或情感性精神病,是一组以显著的心境低落为主要特征的情绪病症,常伴有相应的思维和行为改变。抑郁症患者有痛苦的内心体验,是“非常消极悲伤的人”。美国精神医学会提出的抑郁症诊断标准,要求在同一个两周时段内,病人几乎每天都在九种常见症状中至少表现出五种:
(1) 情绪忧郁;
(2) 对几乎所有的日常活动丧失兴趣;
(3) 体重明显下降或增加;
(4) 异常失眠或嗜睡;
(5) 精神运动性阻滞或焦虑不安;
(6) 疲惫和精力不济;
(7) 思维消极和全面否定自我;
(8) 脑功能下降或异常犹豫不决;
(9) 反复产生自杀的念头。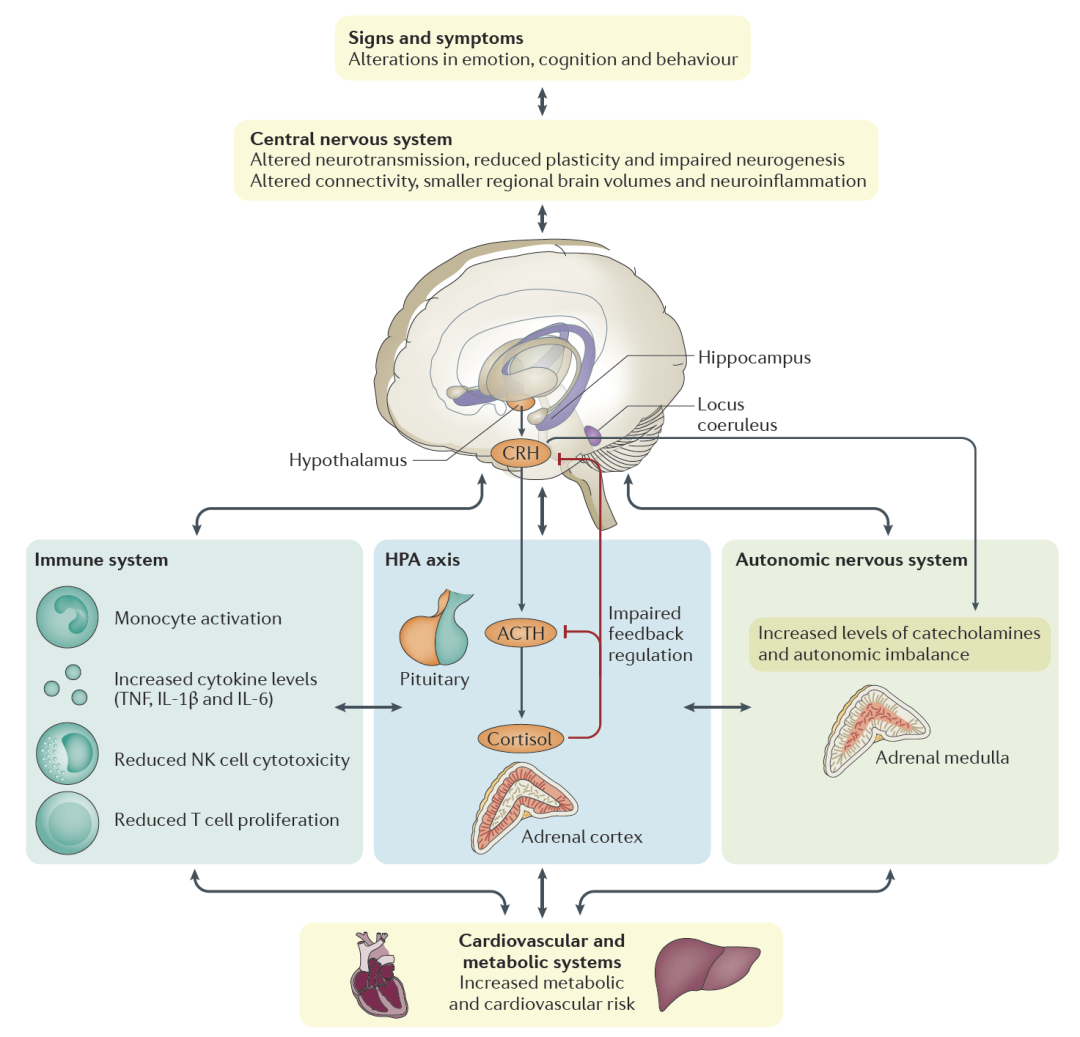 图3. 抑郁症的病理生理学与人体的多个系统有关。[1]抑郁症虽然是中枢神经系统的情绪病症,但是它的病理生理学也牵涉了人体其他几个生理系统,其中包括免疫系统、参与应激反应的神经内分泌系统 (主要是下丘脑—垂体—肾上腺轴) 、外周的自主神经系统、以及心血管和代谢系统 (图3) 。由于各种抑郁症动物模型的局限性,神经生物学研究至今都未阐明发病过程中这些系统之间相互作用的机理。
图3. 抑郁症的病理生理学与人体的多个系统有关。[1]抑郁症虽然是中枢神经系统的情绪病症,但是它的病理生理学也牵涉了人体其他几个生理系统,其中包括免疫系统、参与应激反应的神经内分泌系统 (主要是下丘脑—垂体—肾上腺轴) 、外周的自主神经系统、以及心血管和代谢系统 (图3) 。由于各种抑郁症动物模型的局限性,神经生物学研究至今都未阐明发病过程中这些系统之间相互作用的机理。
巧合与启发:第一代抗抑郁剂
虽说抑郁症对人类健康的危害在古希腊时代就有记载,但直到晚近,现代医学对付精神类疾病的手段仍旧非常有限。第一个具有抗抑郁效果的化合物Iproniazid直到1954年才由几位肺病临床医生意外发现。这种单胺氧化酶 (monoamine oxidase,MAO) 抑制剂 (MAOI) 最初被用来尝试治疗肺结核,临床试验没有看到疗效,却意外发现Iproniazid有提升病人精力的“副作用”。
可惜在抗抑郁临床试验成功和广泛用于抑郁症病人后没多久,Iproniazid 就因为发现具有肝脏毒性而被迫停止使用。值得庆幸的是,按照MAOI思路研制的第二个抗抑郁药物Imipramine很快在1957年取得成功,这是一个具有三环结构的化合物 (图4)。Imipramine对60%到70%的抑郁症病人有效,至今依然是精神科医生的治疗手段之一。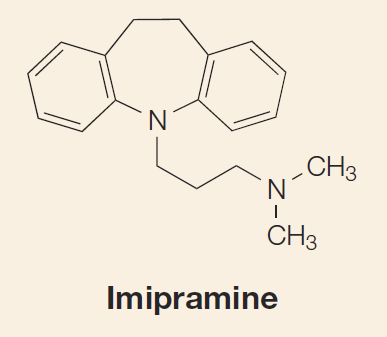
图4. 三环抗抑郁剂的原型:Imipramine制药业的传统经验告诉我们,许多靠机缘巧合发现的药物通常因为作用机制比较复杂而有多种毒副作用。服用第一代抗抑郁药的病人在临床上通常伴随心跳急速而不规则、口干舌燥、便秘、体位性低血压、昏昏欲睡等不良副作用。
有鉴于此,科学家又不断合成和筛选了各种Iproniazid及Imipramine的类似物,以期减弱这些副作用。同时,基础医学研究人员也在深入探索这些药物的作用机理。
自1950年代后期开始,大量与抑郁症有关的神经化学研究工作可谓硕果累累,先后引领了去甲肾上腺素 (Norepinephrine) 和多巴胺 (Dopamine) 两种单胺类神经递质 (图5) 的新发现,其中的代表科学家阿克塞尔罗德 (Julius Axelrod) 和冯·奥伊勒 (Ulf von Euler) 在1970年、卡尔森 (Arvid Carlsson) 在2000年先后荣获诺贝尔生理学或医学奖。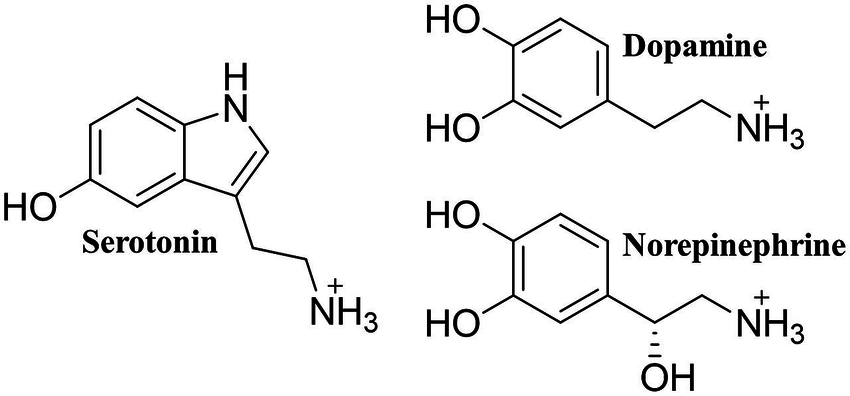
图5. 三种最重要的单胺类神经递质:5-羟色胺,多巴胺,去甲肾上腺素
正常生理情况下,为了使突触后神经元能够连续不断地感应来自突触前神经元的动作电位,已从突触前神经元释放的神经递质在完成信号传导后,必须及时高效地从突触间隙被清除。由于神经递质通过扩散离开突触间隙的速度较慢,神经系统还有两种快速清除神经递质的机制,要么动用突触间隙中的特异性代谢酶来原位降解 (例如MAO就是负责降解单胺类神经递质的氧化酶),要么通过突触前神经元或者神经胶质细胞质膜上的特异转运蛋白来回收 (图6)。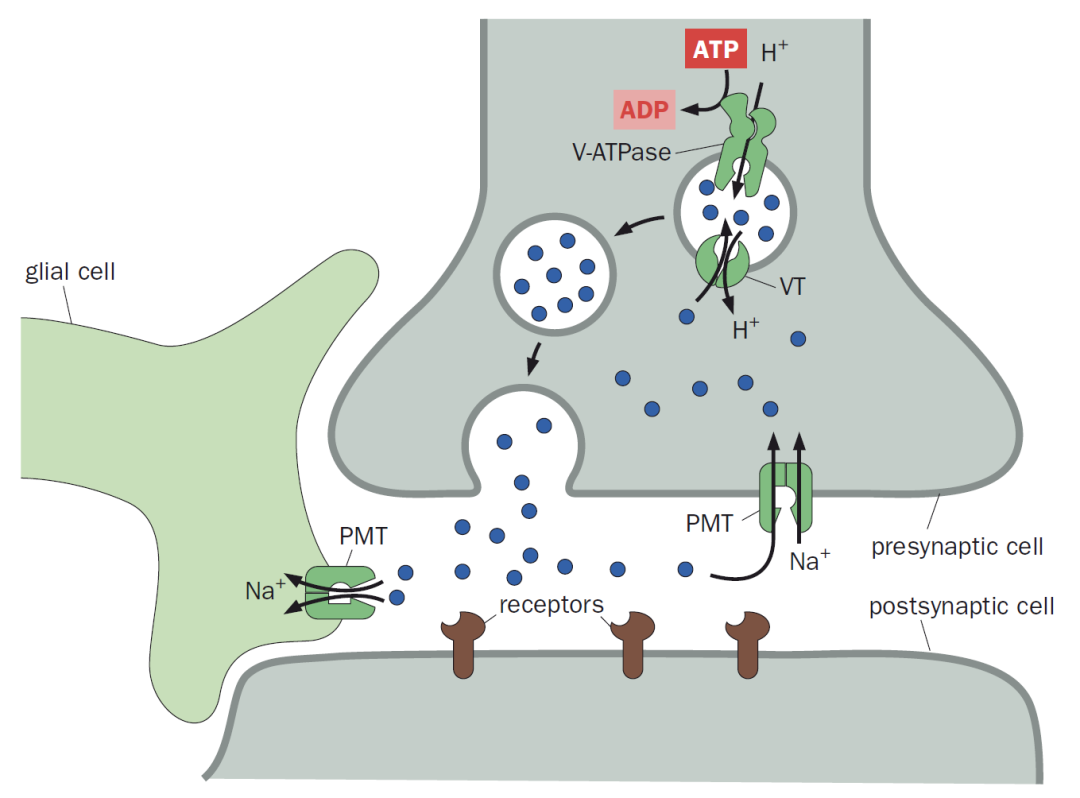 图6.突触前神经元和神经胶质细胞从突触间隙回收过量的神经递质。丨来源:Luo, L.(2020) Principles of Neurobiology, 2nd Edition。
图6.突触前神经元和神经胶质细胞从突触间隙回收过量的神经递质。丨来源:Luo, L.(2020) Principles of Neurobiology, 2nd Edition。
在抑郁症的病理条件下,与调控情绪有关的神经递质对突触后神经元的信号传导效率很可能偏低,也许没有必要把它们从突触间隙快速清除。沿着这条思路的后续研究果然发现,MAOI和三环抗抑郁剂 (tricyclic antidepressants, TCA) 都能提高单胺类神经递质在突触间隙的有效浓度。
MAOI能抑制负责降解突触间隙单胺类神经递质的MAO酶活性,而TCA则抑制神经系统对去甲肾上腺素和5-羟色胺 (5-HT,别名Serotonin) 的回收。这使得科学家们相信,抑郁症的一个主要致病机理是病人大脑中可有效利用的单胺类神经递质浓度明显下降,该理论被称为“抑郁症的单胺假说”。
艰难出世:第二代抗抑郁剂
抑郁症单胺假说在1970年代初期成功地促进了第二代抗抑郁剂的诞生。当时关于Imipramine和另外两个含叔胺基团 (tertiary amine) 的TCA药物Amitriptyline及Chlomipramine的实验表明,它们对5-羟色胺回收的抑制程度要比对去甲肾上腺素回收的抑制高一个数量级以上。
而含仲胺基团 (secondary amine) 的TCA药物,如Desipramine, Nortriptyline,和Desmethylchlomipramine等则有相反的选择性,则能更有效地抑制神经系统对去甲肾上腺素的回收。卡尔森实验室因此提出了一个细分TCA药效的假说,他们认为,对5-羟色胺回收的抑制能够提升病人的情绪 (图7),而对去甲肾上腺素回收的抑制则可提升病人对日常活动的兴趣和动力 (图8)。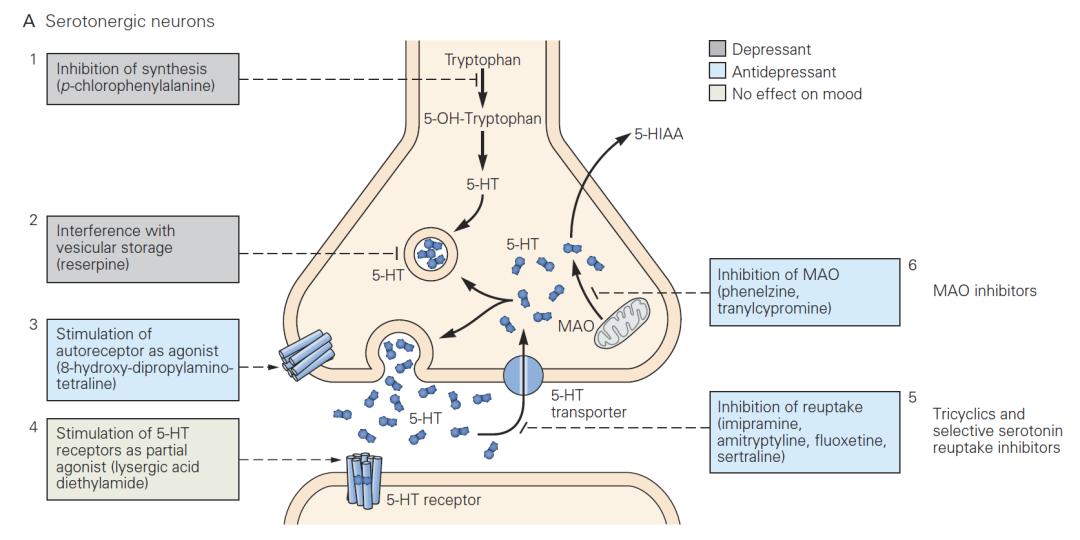 图7. 5-羟色胺回收抑制剂的抗抑郁作用机理。来源:Kandel, E.R. et al (2021) Principles of Neural Science, 6th Edition。
图7. 5-羟色胺回收抑制剂的抗抑郁作用机理。来源:Kandel, E.R. et al (2021) Principles of Neural Science, 6th Edition。
从1971年开始,美国礼来制药公司 (Eli Lilly) 的研究人员开始致力于研制比TCA类药物更具特异性的选择性神经递质回收抑制剂 (selective reuptake inhibitors, SRI) ,通过区分不同的单胺递质系统而增强抗抑郁药物的安全性能和病人对药物的耐受力。他们先合成了一种名为Nisoxetine (LY94939) 的仲胺化合物,在体外细胞生化实验中,它能高选择性地抑制去甲肾上腺素的回收。
1972年,他们又对Nisoxetine的两个苯环之一进行了化学修饰,惊奇地发现:在对位引入三氟甲基后,新产生的仲胺化合物Fluoxetine是很强的5-羟色胺选择性回收抑制剂 (selective serotonin reuptake inhibitor, SSRI) !这说明在TCA中发现的“叔胺规则”并不适用于这类双苯环化合物,而且三氟甲基是关键基团,若换成甲基、甲氧基、或简单的卤素,都会降低抑制5-羟色胺回收的效果。而若把三氟甲基挪到邻位或间位,则除了抑制5-羟色胺回收的有效性下降之外,对去甲肾上腺素回收的抑制效果却有所增高。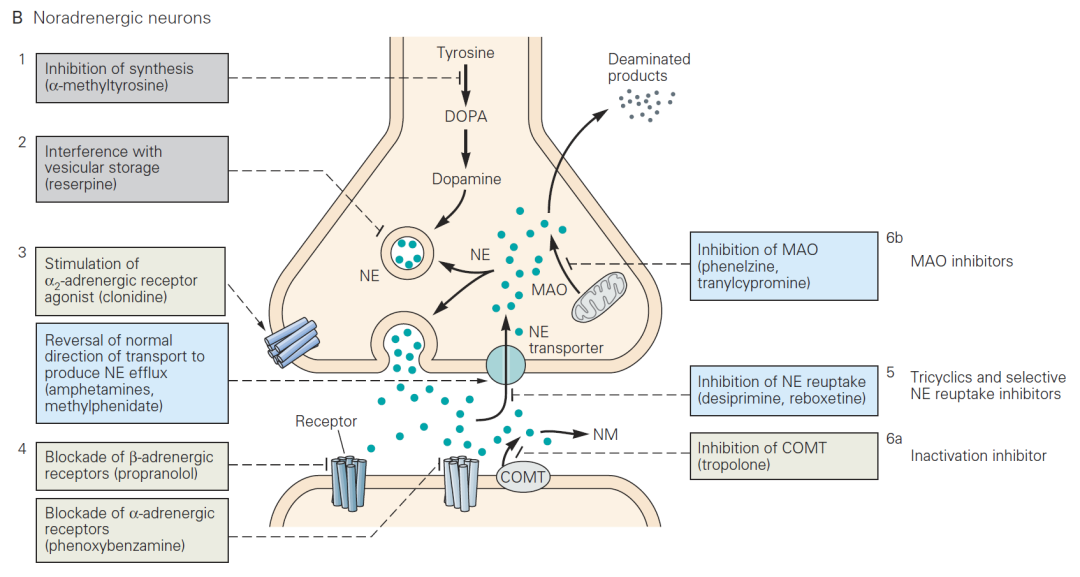 图8. 去甲肾上腺素回收抑制剂的抗抑郁作用机理。丨来源:Kandel, E.R. et al (2021) Principles of Neural Science, 6th Edition。
图8. 去甲肾上腺素回收抑制剂的抗抑郁作用机理。丨来源:Kandel, E.R. et al (2021) Principles of Neural Science, 6th Edition。
随后,动物药理学实验证实了Fluoxetine对5-羟色胺回收的特异性抑制,于是在1974年,礼来公司的研究人员决定先将这些实验结果在文献中发表,Fluoxetine成为首个正式报导的SSRI (图9)。他们认为,Fluoxetine不仅是一个研究5-羟色胺神经元生理和内分泌过程的有用试剂,而且很可能会成为一种新型的抗抑郁剂。
这一观点引起了学术界一些专家的怀疑和批评,因为当时Fluoxetine在常用的抑郁症动物模型 (例如小鼠强迫游泳实验) 中并没有表现出类似TCA药物的明显效果。专家们同时认为,对去甲肾上腺素回收的抑制在治疗抑郁症中更为重要,他们无法想象一种几乎专一的5-羟色胺回收抑制剂能作为临床上的抗抑郁剂。更有观点偏激者认为,增强5-羟色胺的神经信号传递甚至有可能加深病人的抑郁症状。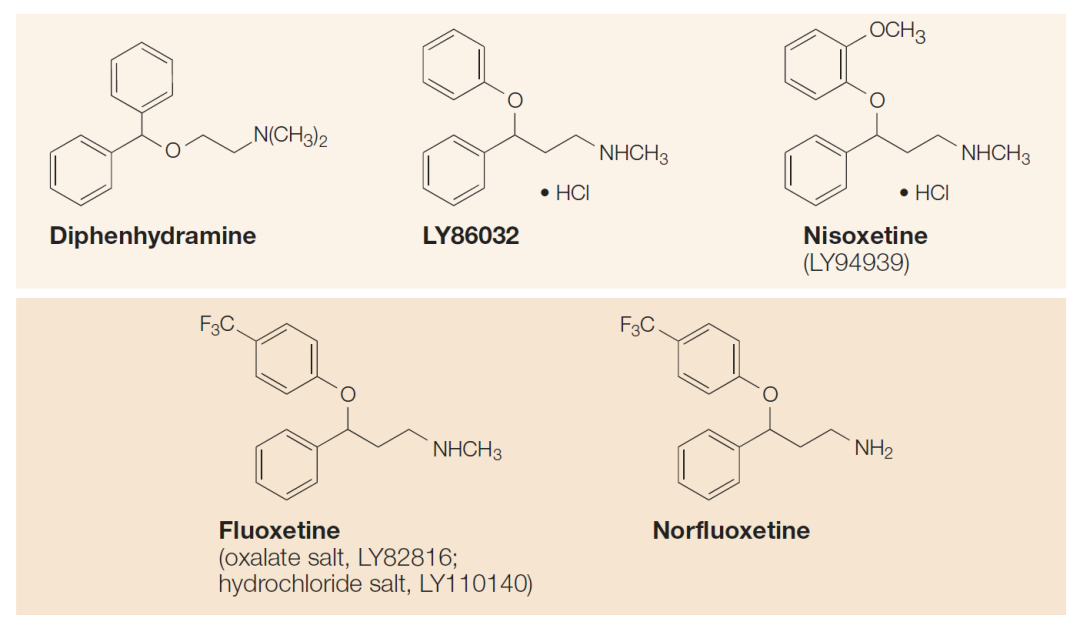 图9. 礼来公司通过药物化学的逐步优化研制出新药Fluoxetine,就是如今鼎鼎大名的百忧解。[5]
图9. 礼来公司通过药物化学的逐步优化研制出新药Fluoxetine,就是如今鼎鼎大名的百忧解。[5]
好在1970年代初期的礼来公司领导层颇具开拓和冒险精神,他们还是批准成立了Fluoxetine的产品开发项目。公司首先要用大鼠和狗做毒理测试,结果很快发现动物用药后表现出如今毒理学界已司空见惯的细胞内磷脂积累 (phospholipidosis) 。当年的毒理学家们对磷脂积累可能预示的毒性判断还处于未知状态,于是礼来公司的团队被迫将Fluoxetine项目暂停以商量对策。
九个月后,礼来公司科学家们前往美国FDA的神经药理学部咨询有关专家的意见,了解到许多双亲性正离子分子 (cationic amphiphilic molecules) 都能导致可逆的磷脂积累。对礼来公司开发项目的一个利好消息是,当时不少已经被批准上市的药物在动物身上都能引起磷脂积累,而用于人体后却没有不良毒副作用。于是Fluoxetine开发项目得以重新启动,并从1976年开始进行关于药物安全性能的一期临床试验,病人对Fluoxetine的耐受剂量范围令人满意。
但是,有关Fluoxetine对抑郁症疗效的二期临床试验却遇到了很大的麻烦。当时Fluoxetine并非礼来公司的重点项目,因此志愿病人数量不够,而且公司在精神疾病类药物开发领域缺乏一位有丰富临床经验的领导者。结果Fluoxetine用于一个小规模抑郁症病人群体时没有明显疗效。礼来科学家们在深感挫败之余,仔细征询了一些专家的意见,发现这批病人中有不少对第一代抗抑郁剂也没有反应。
于是,礼来团队决定不言放弃,在接下来的两年多时间里换一批病人重新进行代价昂贵的二期临床试验。这也是整个Fluoxetine项目的最后一次机会,成败在此一试。“苦心人,天不负”,这一次试验取得了满意的临床效果,从而印证了临床测试前用统计学引导合理实验设计的重要性。礼来团队很快乘胜追击,大规模检验疗效的三期临床试验再传捷报。
同时发现,Fluoxetine和TCA类药物相比,临床副作用大为降低,病人的口干、眼晕、便秘、和昏睡等不良副反应程度较轻。1983年,100多卷、每卷厚达两英寸的临床试验数据终于从礼来公司在美国印第安那州的总部运往首都华盛顿的FDA新药审批部,这已是Fluoxetine首例人体试验之后的第七年,开发一个新药的艰巨性由此可见一斑。
四年之后的圣诞节长假,也就是1987年12月29日,礼来团队成员终于在电视新闻里得知了Fluoxetine被FDA批准的好消息。经过了十几年的艰苦奋战,大家在激动之余也有一种被“平反昭雪”的感觉。
在很长时间里,礼来公司的这个项目不被人看好,甚至被某些业内人士耻笑。1988年1月,Fluoxetine以“百忧解” (Prozac) 为商品名在美国上市,市场占有率很快后来居上,压倒TCA类抗抑郁剂。1992年,百忧解仅在美国市场的销售额就突破了十亿美元大关。作为第一个上市的SSRI类抗抑郁剂,百忧解所取得的巨大成功吸引了其它制药公司沿着类似的思路争相效法,辉瑞公司的左洛复 (Zoloft) 在1992年成为第二个上市的SSRI。
很快各类新型SSRI不断涌现,成为至今仍然主导市场的第二代抗抑郁剂。1999年,SSRI类药物的“首席代表”百忧解荣膺美国《财富》杂志“世纪产品”。第二代抗抑郁剂所取得的成功是以TCA类为代表的第一代药物所无法比拟的。
漫漫征程:研发第三代抗抑郁剂的新方向
随着第二代抗抑郁剂越来越广泛的使用,其局限性和新问题也开始引起临床医生的广泛重视。大约20%到30%的抑郁症患者在经过至少两次不同的抗抑郁药治疗后仍然没有疗效,他们被归类为难治性抑郁症 (treatment-resistant depression, TRD),比一般患者的住院率和自杀风险都要高出许多。还有一些病人在SSRI药物取得疗效后会复发。
另外,以百忧解为代表的SSRI类抗抑郁药还有一个未解之谜:虽然病人在服药几小时内血液中的5-羟色胺浓度就显著上升,但却需要连续服药几周甚至几个月后才见抑郁症状的缓解。
疗效的延迟暗示着SSRI的抗抑郁机理十分复杂,并非仅靠提升突触间隙的5-羟色胺浓度。从1990年代开始,抑郁症单胺假说的局限性逐渐浮出水面。一些科学家开始推论:抑郁症的病理可能还涉及大脑皮层和边缘系统的内在神经回路,而这些回路中的神经元主要释放谷氨酸 (glutamate,常用简写是Glu) 和γ-氨基丁酸 (γ-aminobutyric acid, GABA) 这两种神经递质。
谷氨酸是大脑中浓度最高的兴奋性神经递质,对信息处理、学习记忆以及神经可塑性都至关重要。突触前神经元通过囊泡释放谷氨酸的过程可以经由激发抑制性递质GABA的受体 (GABAR) 来进行负调控 (图10)。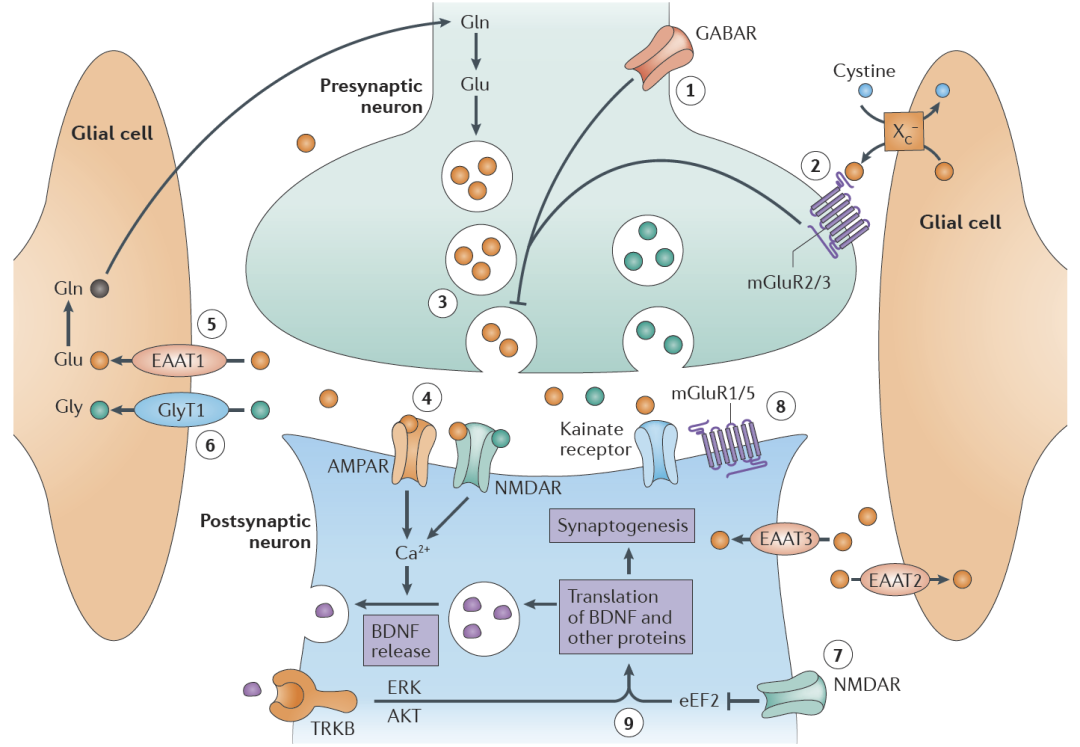 图10. 正常生理条件下的谷氨酸和GABA递质信号传导[6]
图10. 正常生理条件下的谷氨酸和GABA递质信号传导[6]
谷氨酸递质的受体系统比较复杂,可以分为两大类型:(1)离子型受体 (ionotropic receptors),主要包括NMDA受体 (NMDAR)、AMPA受体 (AMPAR)、红藻氨酸受体 (kainate receptor);(2)代谢型受体 (metabotropic receptors,mGluRs)。1990年代末,已有研究显示了NMDA受体拮抗剂在动物模型中的抗抑郁效果。而早在1970年就被FDA批准使用的麻醉剂氯胺酮 (Ketamine),其实就是一个高效的NMDA受体拮抗剂。
虽然氯胺酮容易被滥用,留下了毒品“K粉” (Special K) 的恶名,耶鲁大学的科学家们依然决定对亚麻醉剂量的氯胺酮在7位抑郁症病人中展开双盲临床试验。出人意料的是,这些患者在静脉注射后几个小时内就明显缓解了负面情绪,而且疗效可以持续好几天 (图11)。六年后,美国国家心理健康研究院的学者们进一步发现,单剂量注射的氯胺酮对难治性抑郁症病人同样有快速而可持续的疗效。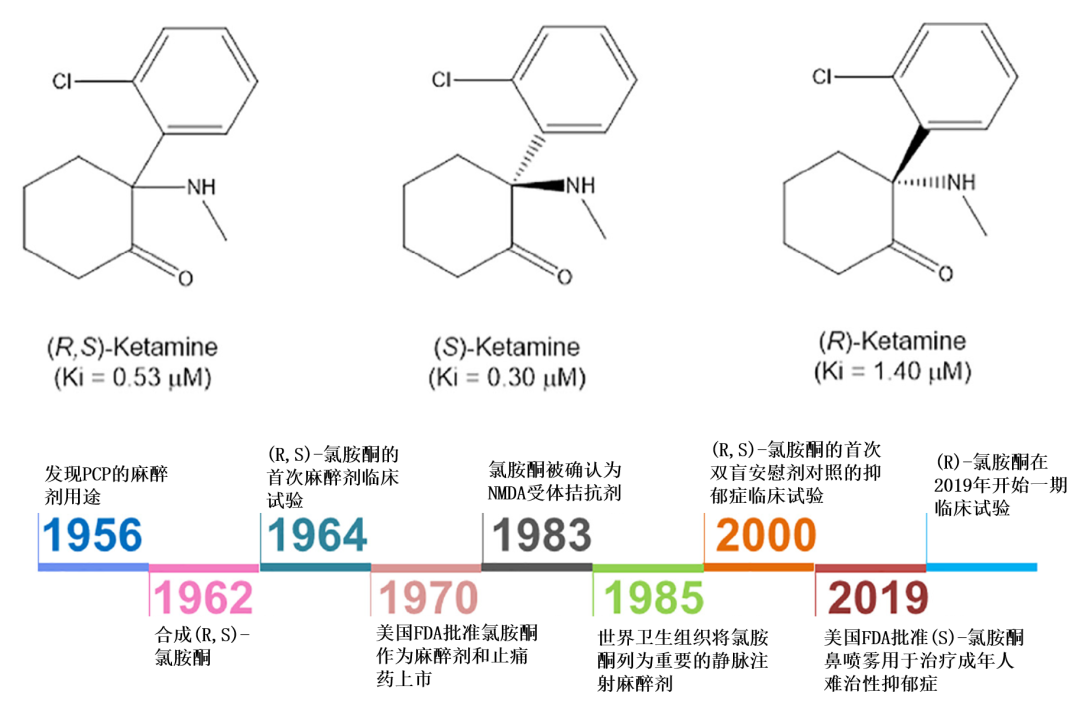 图11.氯胺酮从麻醉剂到抗抑郁剂的历史发展脉络[7]为了把这个容易被当作毒品滥用的麻醉剂研发成可以造福难治性抑郁症病人的新药,强生公司付出了艰巨的努力,先后以鼻喷雾剂型的氯胺酮(S)对映体 (艾氯胺酮,Esketamine) 进行了19个一期临床、4个二期临床、和5个三期临床试验。2019年3月,FDA专家委员会面对3个三期试验成功、2个三期试验失败的结果,考虑到过去三十多年里没有出现新机制的抗抑郁药,最后以14票支持、2票反对、1票弃权的压倒性优势支持艾氯胺酮上市,商品名定为Spravato (图11)。
图11.氯胺酮从麻醉剂到抗抑郁剂的历史发展脉络[7]为了把这个容易被当作毒品滥用的麻醉剂研发成可以造福难治性抑郁症病人的新药,强生公司付出了艰巨的努力,先后以鼻喷雾剂型的氯胺酮(S)对映体 (艾氯胺酮,Esketamine) 进行了19个一期临床、4个二期临床、和5个三期临床试验。2019年3月,FDA专家委员会面对3个三期试验成功、2个三期试验失败的结果,考虑到过去三十多年里没有出现新机制的抗抑郁药,最后以14票支持、2票反对、1票弃权的压倒性优势支持艾氯胺酮上市,商品名定为Spravato (图11)。
FDA规定,Spravato鼻喷雾必须与其它口服抗抑郁药物联用,限于治疗成年的难治性抑郁症病人。另外由于该产品有严重嗜睡、解离性幻觉、容易成瘾等副作用,需要通过特殊配送渠道 (Risk Evaluation and Mitigation Strategy,REMS)才能获得,并伴有相应的黑框警告。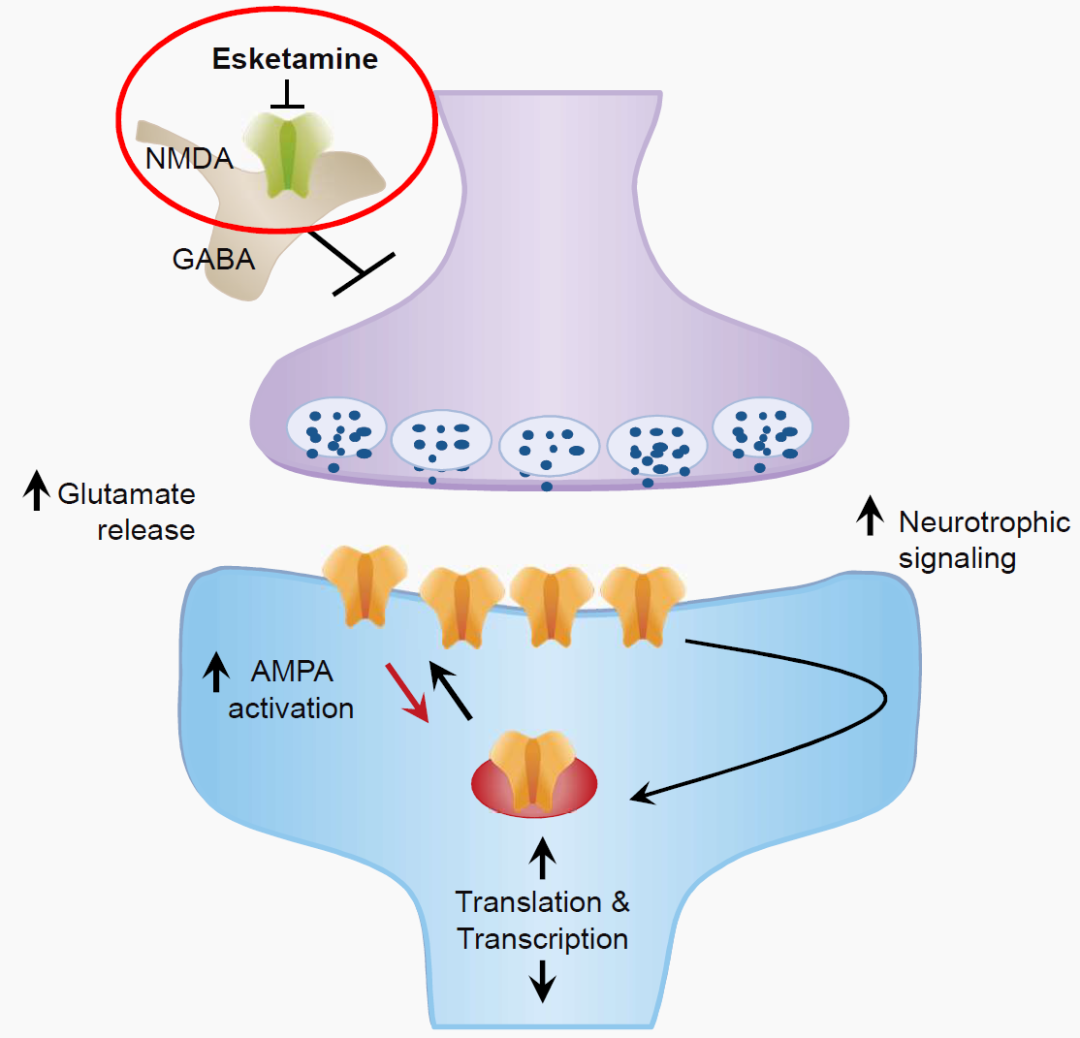 图12.氯胺酮和艾氯胺酮抗抑郁作用的粗略分子机制。丨来源:
图12.氯胺酮和艾氯胺酮抗抑郁作用的粗略分子机制。丨来源:
艾氯胺酮比较粗略的分子机制是:通过拮抗谷氨酸的NMDA受体,促进谷氨酸的释放,激活突触后神经元的AMPA受体。AMPA受体激活可以增强神经营养因子的信号传导,进而产生快速且可以持续的抗抑郁疗效 (图12)。
但这些初步认识离我们透彻理解氯胺酮的作用机理尚有距离。近年来很多科研团队都在深入探究,以求找到能消除艾氯胺酮不良性质的新药。目前至少有五种不同的假说,学术界在短期内很难达成全面共识。总之,与人类大脑健康休戚相关的抗抑郁药研发依然任重而道远。
参考文献
[1] Otte, C. et al. (2016) Nature Reviews Disease Primers 2: 16065.
[2] Wong, D.T., Bymaster, F.P. & Engleman, E.A. (1995) Life Sciences 57: 411-441.[3] Stokes, P.E. & Holtz, A. (1997) Clinical Therapeutics 19: 1135-1250.[4] Wong, M.L. & Licinio, J. (2004) Nature Reviews Drug Discovery 3: 137-151.[5] Wong, D.T., Perry, K.W. & Bymaster, F.P. (2005) Nature Reviews Drug Discovery 4: 764-774.[6] Murrough, J.W., Abdallah, C.G. & Mathew, S.J. (2017) Nature Reviews Drug Discovery 16: 472-486.[7] Wei, Y., Chang, L. & Hashimoto, K. (2020) Pharmacology, Biochemistry and Behavior 190: 172870[8] Yavi, M. et al. (2022) Discover Mental Health 2: 9
出品:科普中国-星空计划
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 