阅读:0
听报道
基因组研究发现了COVID-19的一些遗传风险因素——或为治疗方法指明方向。
原文作者 | Ewen Callaway
去年3月以来,世界各地的研究团队分析了逾10万名COVID-19患者的基因组,希望能找到一些遗传线索,用来预测哪些人最易在感染新冠病毒(SARS-CoV-2)后发展成重症。经过一番努力,这些团队于7月8日在《自然》上报道了十多个基因突变[1]——这些突变与个体感染COVID-19和发展成重症有很强的统计学关联。
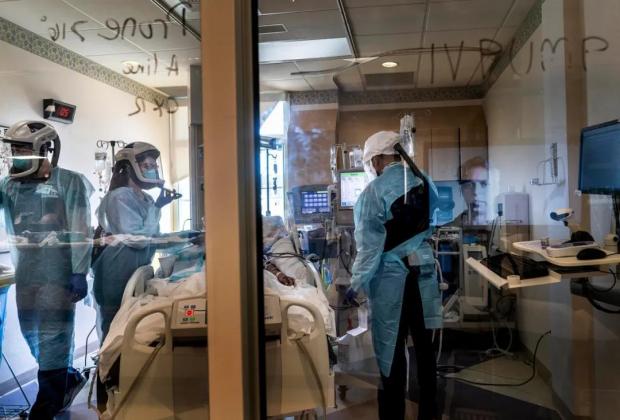
美国加州埃尔森特罗的COVID-19患者正在重症监护室接受治疗。丨来源:Melina Mara/The Washington Post/Getty
“居然有好几个常见的基因突变和COVID-19有很大的关系。”加拿大麦吉尔大学传染病医师、遗传流行病学家Guillaume Butler-Laporte说,“我们没想到会发现这么明确的关联。”
参与本次分析的多支团队既有科研实验室,也有私人公司,比如美国的23andMe和AncestryDNA,分析结果在过去一年里相继发布。整个项目被称为COVID-19“宿主遗传学计划”(Host Genetics Initiative,HGI),今年3月最先在medRxiv预印本服务器上发布了这篇荟萃分析——汇总了46项独立研究,开展分析时涵盖了近5万名COVID-19患者。
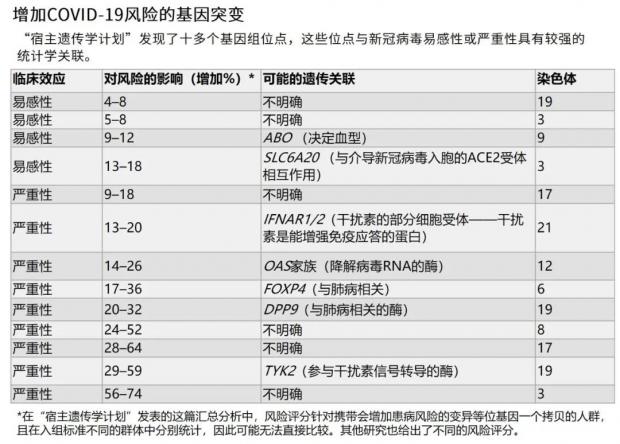
他们发现的遗传关联虽然只会让患病风险小幅上升,但有些程度堪比其他风险因素,如肥胖、糖尿病等基础疾病(见“增加COVID-19风险的基因突变”)。
不过,研究结果可以帮助阐释COVID-19的生物学机制,提示值得测试的药物,英国爱丁堡大学重症监护医师、遗传学家Kenneth Baillie说。和“宿主遗传学计划”鉴定出的常见突变不同,其他研究还发现了一些相对罕见的基因突变,或许也能指出重症的根源。
并非所有人都赞同这些遗传学研究能提出立竿见影的洞见。“我们正在获得一个很好的遗传图谱。”英国牛津大学的人类遗传学家Julian Knight说,“但从这里到确定可靠的药物靶点,或是认识疾病的个体差异 ,还需要迈出一大步。”他说,对于试图在基因组常见变异和人类复杂疾病风险之间寻找关联的研究,这是一个常见问题。
冰岛的deCODE Genetics公司的首席执行官、“宿主遗传学计划”成员Kári Stefánsson认为,这项寻找遗传学“靶点”的工作并非硕果累累——至少现在还没啥大收获。但Stefánsson仍表示,“我认为尽可能多地研究下去非常重要,说不定会发现十分关键的机制。”
虽然遗传学家现在还无法解答所有问题,但他们揭示COVID-19相关遗传因素的速度可谓风驰电掣,麦吉尔大学遗传学家、内分泌学家、“宿主遗传学计划”成员Brent Richards说,“整个人类遗传学领域今年就没睡好过。”
COVID-19的遗传靶点
“宿主遗传学计划”不是严格意义上为攻关一个问题而开展的合作,它更像一个集合作、支持、建议于一身的信息交换所。各个团队可以自己发表研究,也能为集体的研究出力。“其本意是要创造一个让大家感到自在、能互相合作的地方。”统计遗传学家Andrea Ganna说。Ganna和遗传学家Mark Daly是“宿主遗传学计划”的联合发起人,两人都供职于芬兰的赫尔辛基大学和美国的博德研究所。
Ganna是全基因组关联研究(GWAS)领域的专家,而GWAS是遗传流行病学研究的重要方法。这些研究会分析大量人群基因组中相对常见的单碱基 DNA差异,并观察这些差异是否会大量存在于有特定疾病或性状的人群中。将GWAS用于COVID-19是早晚的事,Ganna说。
Baillie团队鉴定出的一个基因组突变在“宿主遗传学计划”的其他研究中得到了验证,这个突变位于名为OAS(寡腺苷酸合成酶)的抗病毒基因家族附近。这种基因能激活会破坏病毒RNA的酶,“宿主遗传学计划”的研究[1, 2]显示,一个会导致肺部OAS1酶循环水平下降的突变会增加感染、住院和重症风险。大部分冠状病毒利用名为PDE(磷酸二酯酶)的蛋白来抵消这种保护作用,但新冠病毒无法产生PDE。“由此可见,这或许是它的要害。”Richards解释道。Richards知道许多医药公司都瞄准了这个靶点,但他拒绝透露细节。基于这种遗传关联,有人预测磷酸二酯酶12抑制剂可以增强人体天然抵御病毒的能力,Baillie说。
Baillie团队发现的另一个突变也在针对COVID-19的其他GWAS中得到了证实,该突变位于一个编码干扰素部分细胞受体的基因附近[1],众所周知,干扰素这种分子能增强人体对病毒的免疫应答。因具有抗病毒作用,一类干扰素分子虽然遗传关联还有待明确,但已经进入了临床试验。该分子也是世卫组织为寻找COVID-19疗法发起的“团结”(Solidarity)试验选入的首批药物,但并未显示出患者获益。Baillie认为,可能是遗传学预测错了,也可能是干扰素应在感染早期服用,或是采用不同于Solidarity试验对象采取的皮下或静脉注射方式给药。
Baillie还表示,其他遗传关联正用来筛选优势疗法。一个例子是英国备受好评的RECOVERY试验,该项目最知名的成果是证明了一种常见类固醇药物对于COVID-19重症患者的益处[3]。RECOVERY试验正在用遗传学数据筛选可进行测试的药物,包括类风湿关节炎药物巴瑞替尼(baricitinib)、银屑病和多发性硬化药物富马酸二甲酯,参与该试验的Baillie说。
巴瑞替尼能抑制TYK2基因编码的蛋白,该基因与危重症COVID-19有关[2]。虽然TYK2活性与重症COVID-19风险的关联在这些遗传学研究中并不清晰,“但却给这种观点提供了更多的支持。”Baillie说。富马酸二甲酯之所以被选入,主要是因为它能帮助抑制COVID-19重症涉及的一个炎症过程,但遗传关联为其进入RECOVERY试验提供了更多证据,Baillie说。
不过,GWAS也会得到让人摸不着头脑的结果。这在COVID-19中也出现了:基因突变与重症COVID-19之间的最强关联位于3号染色体这个研究并不充分的区域[1]。“整个学界仍不清楚为何这个区域如此关键。”Butler-Laporte说。3号染色体区域包含多个参与免疫信号转导、肺生物学和其他可能机制的基因。但尚不清楚其中哪个基因能解释与COVID-19的这种关联。
有这个基因突变的人因COVID-19住院的概率是其他人的两倍左右。Richards、Ganna和麦吉尔大学呼吸科医师Tomoko Nakanishi领导的一项研究[4]发现,该突变让 60岁或以下人群的COVID-19重症或死亡概率上升的程度与糖尿病、肥胖、慢性阻塞性肺病等风险因子相当,甚至更大。
风险评分
得到遗传关联后,一些研究人员开始分析GWAS发现的遗传关联是否能用来预测个体出现危重症COVID-19的风险。风险评分能汇总GWAS中发现的各种关联,已被用来预测个体罹患2型糖尿病、各类癌症和心血管疾病等疾病的风险。
不过,考虑到疫苗的普及性,尚不清楚这种方法是否适用于COVID-19——或是否有必要。6月,澳大利亚的Genetic Technologies公司推出了一款175美元的测试,可用来预测个体出现重症COVID-19的风险。但这也要看个人的年龄、性别、健康状况,这些因素能显著提升通过GWAS关联进行预测的能力[5]。
首席科学官Richards Allman表示,该公司的测试是利用英国生物银行(UK Biobank)数据库的数据开发和验证的,可能对中年人最有用。大部分中年人罹患重症COVID-19的风险相对较小,但这个测试或能发现危重症感染概率大幅提高(或显著降低)的罕见个体。该公司的测试目前只能通过美国新泽西州的Infinity BiologiX公司获得,并有专业医疗人士提供咨询。Allman说,Genetic Technologies正在和有意向员工提供该测试的公司洽谈,但Allman说他没有销售数据。
Nakanishi、Richards和Ganna认为,现在还不确定该测试是否已经被充分验证是有效的,但这不排除该测试能成为鼓励高风险人群接种疫苗的另一种手段。“它或许能让一些有顾虑的人转变态度。”Genetic Technologies的统计学家Gillian Dite说。
COVID-19和大部分其他疾病的遗传学研究一样,几乎清一色地针对欧洲裔人群。这很成问题,Knight说,因为COVID-19的全球负担以及英美等国少数族裔群体的患病率不断升高。“我们真的需要在这些人群中开展遗传学研究。”
遗传学研究的多样性不仅能帮助我们理解在欧洲人群中鉴定出的风险突变,还能在其他人群中发现新的风险突变。一项覆盖2000名日本COVID-19住院患者的GWAS[6]鉴定出了许多在欧洲人群中发现的突变,还有其他研究没有发现的一个参与干扰素产生的免疫基因DOCK2。会增加COVID-19风险的DOCK2突变在东亚人群中相对常见,但在欧洲、南亚、非洲裔人群中非常少见。“这告诉我们,丰富COVID-19宿主遗传学研究的多样性有多么重要。”该研究通讯作者、日本大阪大学统计遗传学家冈田随象(Yukinori Okada)说。
罕见突变
GWAS发现了让个体风险小幅上升的常见突变,但一些研究人员认为这种方法在效果上不如发现一些能解释为何身体健康的人会出现重症COVID-19的罕见突变。
这是纽约洛克菲勒大学遗传学家Jean-Laurent Casanova的观点。他参与领导的“COVID人类遗传学研究”(COVID Human Genetic Effort)在2020年9月报道了[7]COVID-19 重症患者体内发现的突变,这些突变能使参与1型干扰素免疫的基因失效,1型干扰素免疫是一种强效的抗病毒应答。(他们发现一个携带突变的基因是IFNAR2,该基因编码一个干扰素受体的亚基,也在多个GWAS中被发现。)Casanova团队发现的突变很罕见,但团队在一项随访研究[8]中发现,10%的COVID-19危重症患者能产生让1型干扰素失效的抗体——类似基因突变的作用。Casanova称其团队是在鉴定出这些遗传突变后才开始寻找它们的,他的方法也提示了新的研究路线。“本质上我们破解了COVID-19重症肺炎的机制。”他说。
会产生严重后果的罕见突变是用来阐明疾病机制的“一个超级火炬”, 美国耶鲁大学的免疫学家Akiko Iwasaki说。Iwasaki的团队正在研究“自身抗体”的作用,这些抗体会攻击COVID-19重症患者自身的免疫防御。GWAS中发现的常见突变的效应可能更加微妙,她补充道,但发现这些突变的无偏方法意味着这些突变能用来支持免疫学等其他学科的洞察。“它解释了我们看到的一些现象,这是我最喜欢的地方。”她说。
Richards所在的团队正在尝试重复Casanova的研究结果,但目前尚未取得成功。他和同事发现,13个1型干扰素基因中的突变在近2000名COVID-19患者中并不比在未感染的对照组中更加常见[9],这与纽约再生元生物技术公司研究人员的分析结果相一致,这些研究人员分析了英国生物银行逾50万名受试者的蛋白编码基因[10]。这并不表示1型干扰素通路不重要,Richards说,他也认为自身抗体的关联看起来很有希望。
意大利锡耶纳大学遗传学家、“宿主遗传学计划”早期成员Alessandra Renieri表示,想要完全理解COVID-19易感性并找到治疗方法,就需要将GWAS的研究结果结合罕见突变和其他形式遗传多样性的关联。她所在的团队已经向意大利监管当局申请许可,测试基于遗传学研究结果的疗法。
比如说,该团队希望在携带罕见突变的人群中测试一种佐剂(能唤醒免疫系统),这些罕见突变会让TLR7这种能检测病毒的基因失效,而这可能和COVID-19重症有关[11]。该团队在发现重症COVID-19与血液中循环的激素睾酮水平下降有关的基因突变具有相关性之后,打算进一步测试睾酮能否预防在编码睾酮受体的一个基因有一个常见突变的男性出现危重症COVID-19[12]。
研究人员认为,这类试验成功与否,都不应成为评判COVID-19遗传学研究是否有用的唯一标准。其他生物学家正在利用这些遗传学研究解释他们自己对新冠病毒开展的实验。类似3号染色体这种令人迷惑的关联或能带来重要见解,帮助我们治疗COVID-19以及下一个冠状病毒导致的疾病。
新的遗传学研究结果就像一块块拼图,Renieri说,“好几块拼图正在在拼凑成型。我相信整个版图会在不久的将来更加清晰。”
参考文献
1. COVID-19 Host Genetics Initiative. Nature (2021).
2. Pairo-Castineira, E. et al. Nature 591, 92–98 (2021).
3. The RECOVERY Collaborative Group N. Engl. J. Med. 384, 693–704 (2021).
4. Nakanishi, T. et al. Preprint at medRxiv (2021).
5. Dite, G. S., Murphy, N. M. & Allman, R. Preprint at medRxiv (2021).
6. Namkoong, H. et al. Preprint at medRxiv (2021).
7. Zhang, Q. et al. Science 370, eabd4570 (2020).
8. Bastard, P. et al. Science 370, eabd4585 (2020).
9. Povysil, G. et al. Preprint at medRxiv (2020).
10. Kosmicki, J. A. et al. Preprint at medRxiv (2021).
11. Fallerini, C. et al. eLife 10, e67569 (2021).
12. Baldassarri, M. et al. EBioMedicine 65, 103246 (2021).
本文经授权转载自微信公众号“Nature Portfolio”。原文以The quest to find genes that drive severe COVID标题发表在2021年7月8日的《自然》的新闻特写版块上。
原文链接:
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 