研究人员希望这位在移植转基因猪心脏后已经安全度过一周的患者,能为异种移植的可行性提供可观的数据。
撰文 | Sara Reardon
翻译 | 施普林格·自然上海办公室
上上周,马里兰巴尔的摩的一名男子成为首位接受转基因猪心脏移植的病人,目前状况稳定。器官移植医生希望这一进展能帮助他们在病人中实施更多的动物器官移植手术,但这方面仍存在许多伦理和技术上的障碍。“我们经过了漫长的努力才走到今天,看到有团队能做此尝试令人非常激动,”纽约哥伦比亚大学外科医生、免疫学家Megan Sykes说,“相信我们能收获很多有趣的知识。”
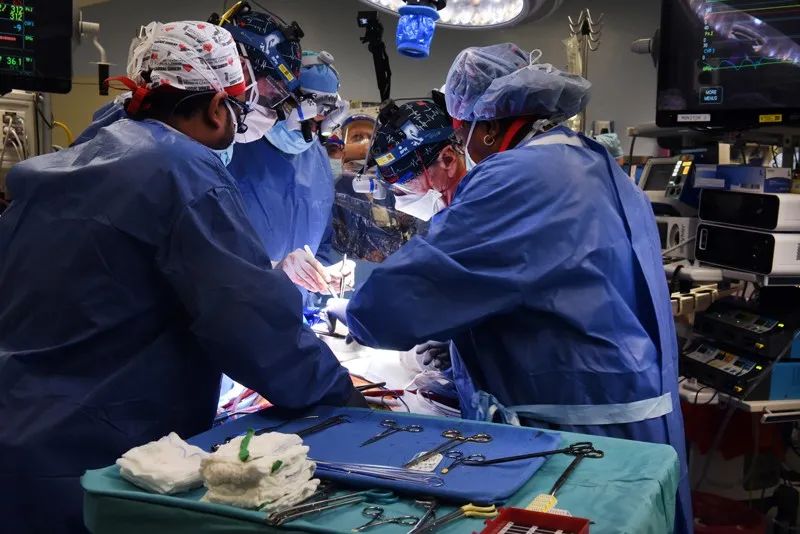
马里兰大学医学中心的外科医生将一个转基因猪心移植到了病人David Bennett的体内。来源:马里兰大学医学院几十年来,全世界的医生和科学家一直在向异种移植(xenotransplantation)的目标迈进,异种移植是指将动物器官移植到人体内。
非常机遇
上上周的手术标志着猪器官首次被移植到有机会存活并康复的病人体内。2021年,纽约大学朗格尼医学中心的外科医生曾将同系转基因猪的肾移植到已无可察觉脑功能、被判法定死亡的两名患者体内。移植的器官在这两位靠呼吸机维持的脑死亡病人体内没有发生排异反应,且能够正常工作。
除此之外,迄今为止的大部分研究都是在非人灵长类中开展的。但研究人员希望,1月7日的这例手术能进一步推动临床异种移植的进展,帮助克服临床异种移植面临的大量伦理和监管问题。“我们从4名病人身上学到了从40只猴子身上也学不到的知识,”波士顿麻省总院的器官移植医生David Cooper说,“是时候进入临床了,看看这些心和肾在病人体内会如何反应。”近年来,随着CRISPR–Cas9基因组编辑技术的出现,异种移植发展迅速,研究人员可以更轻松地获得不易被人类免疫系统攻击的猪器官。
最新的移植手术在马里兰大学医学中心(UMMC)开展,使用的猪进行了10处基因修改。研究人员曾向美国食品药品监督管理局(FDA)申请开展猪心脏移植人体的临床试验,但被拒绝了。马里兰大学的Muhammad Mohiuddin医生领导了这次移植手术背后的研究团队,他说,FDA曾要求手术使用的猪一定要来自医疗级养猪设施,并希望研究团队在移植到人体前先将猪心脏移植到10个狒狒体内。不过,57岁的David Bennett让Mohiuddin团队有机会直接跳到人体
Bennett近两个月来只能靠心脏支持系统维系生命,而且因为心律不齐无法使用机械心泵。由于他之前没有遵医嘱,所以也无法接受人体器官的移植。考虑到他只剩下“等死”一条路,研究团队征得了FDA的许可,可以为Bennett开展猪心脏移植手术。
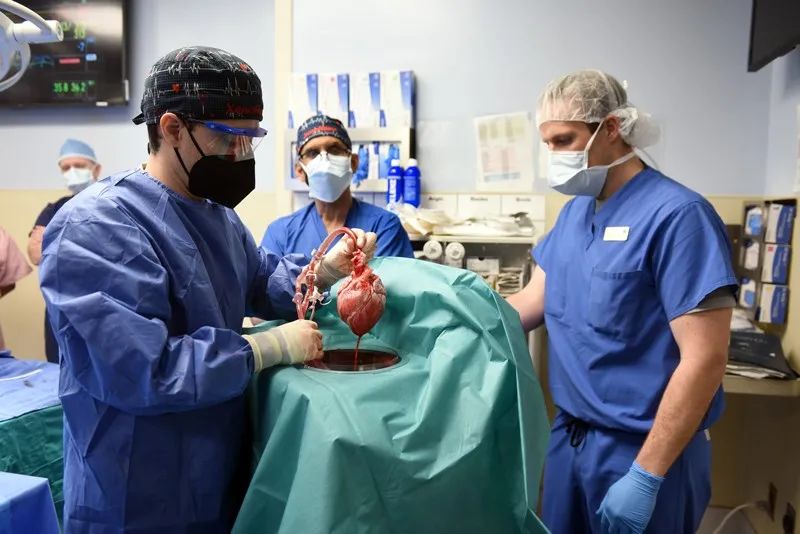
移植手术使用的心脏来自一头经过多次基因修改的猪,一些修改敲除了能激活人类免疫系统的基因。来源:马里兰大学医学院
Mohiuddin说,手术过程非常顺利,心脏功能看起来很好。他和他的团队将持续监测Bennett的免疫应答和他的心脏反应。临床对照试验仍是他们的目标,但Mohiuddin说,如果能遇到合适的患者,他们也许会申请开展更多的紧急手术。
悉尼大学已经退休的器官移植医生Jeremy Chapman说,如果Bennett的手术被证明是成功的,而且有更多的研究团队效仿,那么监管机构和伦理学家就需要定义哪些人才有资格接受猪器官的移植。等待器官的时间过长不是开展这项高度实验性、有潜在风险手术的充足理由。尤其是肾等器官,大部分等待肾移植的病人都可以先透析
Chapman将这个过程比作让那些有其他选择的患者使用实验性的癌症药物。他说,监管机构和伦理学家需要决定的是:怎样的获益才能超出患者在等待人体器官中面临的风险。
“疯狂而兴奋的一周”
目前为止,移植手术的开展主要局限于猪的供给和监管障碍。目前只有弗吉尼亚州的Revivicor公司(母公司为United Therapeutics)拥有适当的设备和达到临床等级的猪。
Revivicor公司首席执行官David Ayares说:“这是令人疯狂而兴奋的一周。” Revivicor利用阿拉巴马伯明翰附近的一家设施养猪,但Revivicor正在弗吉尼亚建造一个更大的设施,并希望这里以后每年能提供数百个器官。
Ayares从事猪的基因改造已经有20年了,他会测试不同的基因修改能如何减少人类和其他灵长类的排异反应。为了获得这次移植手术的猪心脏,Revivicor公司敲除了猪的3个基因——这些基因会诱导来自人体免疫系统的攻击,他们还加入了6个人类基因,帮助人体接受外来的猪器官。最后的一个修改是为了让猪心脏不会对生长激素产生反应,确保来自这些400公斤动物的器官能保持在人类器官的大小。虽然这次的人体-猪心组合看似成功了,但我们仍不清楚多少基因修改是必要的。“我们还要做很多研究,才能评估每一种基因修改的作用,”
Sykes说,这些修改可能对人体有害,所以我们需要掌握这方面的信息。Mohiuddin说,为狒狒开展一次移植手术的成本大约在50万美元左右,实验多种组合的成本可能会高得离谱。Cooper等人表示,异种移植的未来可能需要根据特定器官和移植受体进行定制化基因修改。比如Cooper自己的研究就发现,在接受猪肾移植的狒狒中,针对生长激素的基因修改会导致尿液输送的问题。但他说,他们团队希望很快能将猪肾植入人体,前提是他们能获得一个经过适当基因修改的猪。
无论发生什么情况,我们距离其他器官的临床使用可能还要一段时间。相比之下,病人肝移植的等待期要短很多,所以对人体进行猪肝移植更难获得认可。虽然等待肺移植的病人经常等不到器官就去世了,但Sykes指出猪肺很脆弱,已被证明很难移植到灵长类的体内,而且经常发生排异。
动物模型的局限
Cooper、Chapman和其他人都认为,我们一定要研究移植器官在人体内而不是在狒狒体内的反应。Chapman说,不同物种间的差异使我们无法沿用这个模型预测病人的临床转归。非人灵长类有一些人类没有的抗体,这些抗体会破坏猪器官上的蛋白,为此研究人员做了大量工作,让这些器官适应狒狒的身体,而不是人类的身体。此外,研究人员还需要研究猪心脏的生理机能,比如猪心脏是否和人类心脏的跳动频率一致,以及病人对移植器官的反应是否和健康的狒狒一样。
好几家公司都在针对实体器官移植,对猪进行不同的遗传修改,但这些公司不像United Therapeutics一样具备临床级设施。马萨诸塞州的eGenesis公司正在生产不会传播逆转录病毒的猪——这种病毒在所有猪的基因组中都存在。新西兰奥克兰的NZeno公司正在培育迷你猪,这些猪的肾无需针对生长激素进行基因修改就能保持人体器官的大小。
Chapman猜测还有很多机构都在生产转基因猪,只不过没有公开商业敏感信息。Ayares和United Therapeutics拒绝透露一头猪的生产成本,但他们承认这些动物“身价不菲”。随着更多公司的加入,Cooper认为成本会慢慢下降,而且FDA等监管机构也会放宽他们对洁净设施的一些要求。猪器官病原体造成的感染似乎还不成问题,但我们仍需对Bennett和今后的移植受体进行后续监测。
本文经授权转载自微信公众号“Nature Portfolio”。原文以First pig-to-human heart transplant: what can scientists learn?为标题发表在2022年1月14日《自然》的新闻版块上。
原文链接:
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 