在鲨鱼和骆驼的免疫系统里,存在着一种与传统抗体构造截然不同的神奇抗体,被称为“纳米抗体”,科学家们正在深入研究这种抗体,并试图利用它解决从新冠病毒到癌症的各种疾病。
撰文 | Hayley Bennett
编译 | 汪汪
美国药理学家Aaron LeBeau有个绰号叫“鲨鱼小子”。当你听到这个绰号,大概很难想象这人会是一名致力于研究癌症新疗法的科学家。刚刚入职美国威斯康星大学麦迪逊分校(University of Wisconsin–Madison)的头一年,LeBeau就在与学校达成的协议里提出,要在他的实验室里放一个30立方米的鲨鱼盐水水箱,现在这个水箱已经成为了四条小护士鲨的安居之处。
LeBeau喜欢他的绰号,他形容这个昵称是一个“众所周知的秘密”,当他第一次见到他的新邻居时,就被问道:你是那个每天在研究鲨鱼的人吗?鲨鱼小子并不仅仅研究鲨鱼。最近,LeBeau又开始研究起了另一种生物:骆驼。在旁人看来,鲨鱼和骆驼显然没有任何共同之处,但在科学家的眼里,这两种风马牛不相及的生物正被一种在进化过程中的奇特之处联系起来,而科学家们正在研究这种奇特之处,试图利用它解决从新冠病毒到癌症的各种问题。
故事要从上世纪80年代说起,当时,一群比利时的学者正在研究水牛昏睡症,在测试过程中,他们需要分析水牛的血液样本。项目中途,一位之前曾在研究组待过的学生提出想用同样的方法来分析骆驼的血液。项目的负责人,来自布鲁塞尔自由大学(Vrije Universiteit Brussel)的 Serge Muyldermans同意了这个请求。学生给研究组送来一些阿拉伯骆驼血液,但研究团队只取了很少一部分用于测试,剩余的血液样本都继续储存在冰箱里。不久之后,Muyldermans为一些生物学专业的学生设置了课程实践——对血液样本中的抗体进行分离。这时,冰箱里储存的骆驼血液终于发挥了作用。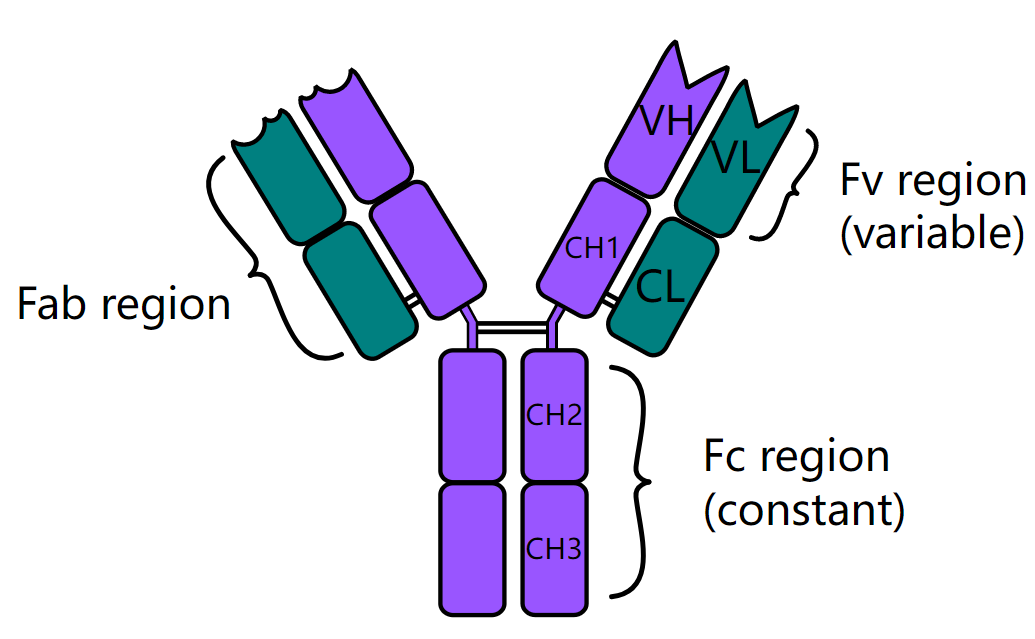
Y形抗体(https://www.antibodies-)
如果我们对免疫学有所了解的话,我们会知道,经典抗体分子一般被认为由两种类型的蛋白质链组成:即重链(heavy chain, Hc)和轻链(light chain, Lc)。两条重链与两条轻链配对形成一个免疫球蛋白分子(immunoglobulin G, IgG)——一种经典的 Y 形抗体(如图1,紫色为重链,绿色为轻链)。这个结构是如此的优雅而强大:两条重链构成了 Y 形双倍厚度的躯干,在顶部向两端展开,就像是伸出的双手;而轻链则像装备在盔甲上的臂板一样,附着在重链伸出的手臂上,和重链一起形成“抓手”,即Fab区,可以与抗原相结合。
按照实验设计,学生们需要首先使用化学还原剂将他们分离得到的 Y 形抗体进行还原拆分,再按分子量对抗体进行分离,就可以得到抗体分子的重链和轻链。但在对骆驼血液样本进行实验时,结果却并不符合预期。无论学生们如何重复实验,都只能得到重链的分子量,而轻链部分却不知所踪。这个实验结果令所有人意外:要么学生们的操作有错误,要么来自骆驼血液中的抗体不同寻常。Muyldermans的同事Raymond Hamers(1933-2021)最先反应过来,他认为这可能不是什么实验错误。
也许,骆驼的抗体就是没有轻链?这个猜想让Muyldermans兴奋起来。他在细菌中制造小鼠抗体时,遇到的难题就是细菌无法将重链和轻链蛋白质正确折叠并连接在一起。如果骆驼的抗体没有轻链,那这难题不就迎刃而解了吗?此后,Muyldermans、Hamers和同事们花了很长时间来证明骆驼的免疫系统确实可以生产这种没有轻链的非典型抗体。1993 年,他们的团队终于在《自然》杂志上报导了这一惊人发现。
事实证明,在骆驼和美洲驼这样的动物体内,既存在传统抗体,也存在这些无轻链抗体。后者被称呼为 “纳米抗体”:它们没有臂板,由重链延伸出去的手臂也更为精小,这种结构使得分子更加紧凑,与传统抗体分子量一般在150kDa左右的大小相比,“纳米抗体” 的大小仅仅只有75kDa 。 这是一个非常有趣且重要的发现。骆驼科动物在它们漫长的进化历程中似乎完成了一项壮举:修改了一个已经稳定运行了数百万年的系统。在其他动物(包括人体)中,抗体的重轻链配对所组成的Y形结构可以对抗不同的微生物入侵者。这种结构久经考验,是在免疫细胞发育过程中由重链和轻链蛋白质的基因片段混合重排的结果。
这是一个非常有趣且重要的发现。骆驼科动物在它们漫长的进化历程中似乎完成了一项壮举:修改了一个已经稳定运行了数百万年的系统。在其他动物(包括人体)中,抗体的重轻链配对所组成的Y形结构可以对抗不同的微生物入侵者。这种结构久经考验,是在免疫细胞发育过程中由重链和轻链蛋白质的基因片段混合重排的结果。
我们可以用音乐播放列表来打个比方:经典抗体的免疫曲目类似于由两个音乐合集编制的播放列表,每个音乐合集包含数千首曲目,组合可以千变万化;而纳米抗体则仅由一个合集创建。让科学家们大开眼界的是,尽管纳米抗体的多样性比传统抗体要少,但依然可以产生良好的免疫反应。
从进化学的角度来看,这个现象至今仍然无法解释。为什么会出现仅有一种链的抗体?它又是如何出现的?
美国加州州立大学(California State University)弗雷斯诺分校的结构生物学家Cory Brooks在 2018 年的一篇论文中提出了他的猜想。他认为这是一次在进化过程中发生的巧合:重链与轻链相互作用的部分发生了变化,使得两种蛋白质链分开。那这种进化巧合是否为骆驼带来了好处呢?根据Brooks的说法,这类纳米抗体似乎比普通抗体“更擅长中和病毒”:在骆驼体内有很高的病毒载量,而这些病毒并没有对骆驼产生影响。但如果其他反刍动物感染了同样的病毒,就会出现各种症状。科学家们猜测,也许在骆驼进化的漫长历史中,出现过一些致命病毒,而这些较小的抗体有助于抵抗这些病毒,从而被保留了下来。
无独有偶,这种神秘的抗体不仅仅出现在驼类生物中,也出现在鲨鱼体内。1995年,美国迈阿密大学的 Andrew Greenberg 及其同事在论文中揭示,鲨鱼使用一种单链抗体,称为“新型免疫球蛋白抗原受体”(immunoglobulin new antigen receptors ,IgNARs)。这类新型抗体常在鲨鱼、鳐鱼和其他软骨鱼类中出现,比骆驼的无轻链抗体更小、更稳定。
这不会是单纯的偶然,新型抗体一定有独到之处,才能在进化过程中被保留下来。Brooks的工作表明,分子量更小的抗体相较于传统抗体来说更加稳定,在恶劣的环境中也能为机体提供保护。
比如说,骆驼的体温很高,而鲨鱼及其亲近鱼类为了平衡海水中的高盐浓度,在体内保留了较高浓度的尿素——这两种情况下,新型抗体都能提供更好的稳定性和更高的保护效力。现在回到鲨鱼小子LeBeau。过去,他研究的正是骆驼抗体,利用这种抗体的特性来寻找癌症靶标,研究抗癌疗法和肿瘤成像技术。这些研究持续了好几年,也得到了不错的成果,因此他的团队希望接下来可以试试鲨鱼的抗体版本。很可惜,LeBeau不确定自己要如何弄到鲨鱼血液,因为他们的实验室位于美国中部,这里的鲨鱼数量为零。无奈之下,他们求助于当地的一家水族馆,水族馆很乐意提供帮助,但每条鲨鱼300公斤的体重使他们望而却步。
看来,养鲨鱼还不如养骆驼靠谱。法国制药公司赛诺菲(Sanofi)正是这么干的。它们建设了一个骆驼牧场,再利用骆驼血液中的特殊抗体发展新的疗法。赛诺菲大获成功:其中一个基于纳米抗体的疗法已经开始进入市场。2018年,赛诺菲还以 39 亿欧元(34 亿英镑)的价格收购了初创公司 Ablynx,这是一家专注于研发纳米抗体疗法的新公司。他们的研发的一般步骤是:用目标病原体感染骆驼,使骆驼产生免疫,等待 6-12 周后抽出骆驼血,再使用相同的病原体来对血中的抗体进行筛选,从而得到最佳抗体。这种策略并不是赛诺菲独有的秘诀。
实际上,它已经被很广泛地使用,业内人员形象地称之为“淘金”。在寻找能结合乳腺癌靶点的骆驼抗体时,研究人员使用的就是这种策略。利用骆驼和鲨鱼活体筛选抗体,是因为人们认为使用活体动物可以减少筛选出最佳抗体的时间——动物的免疫系统在遇到目标分子之后,会做一些额外的分子工作,来优化它们的结合结构。但每种方法都有挑战,照顾一个满是骆驼的农场并不是一个简单的选择。赛诺菲近些年来针对纳米抗体的研发做出了非常多的成果。2018年,由其研发的针对罕见血液疾病的纳米抗体 caplacizumab 在欧盟获批上市,并于次年获得美国FDA批准。赛诺菲还在针对其他靶点开发疗法,例如类风湿性关节炎和红斑狼疮等一些自身免疫疾病。
另一种由Ablynx和赛诺菲联合研发的药物ozoralizumab在日本开展了针对类风湿性关节炎的临床试验,并于今年6月宣布了临床二/三期试验的积极结果。纳米抗体具有灵活的小身材和更加稳定的性质,而且可以格式化加以设计,这些独特的优势令它们备受科学家们的青睐。正如Muyldermans所期待的那样,当不再需要传统抗体的轻链结构以后,生产过程中遇到的难题迎刃而解,这些纳米抗体可以在细菌、酵母或哺乳动物细胞中大规模克隆和生产。
不过,提高产能仅仅是优势之一。纳米抗体还有一个绝对的优势——它们可以到达传统抗体无法到达的目标分子部分。这是一个非常大的突破,这意味着在传统抗体之外,我们可以使用纳米抗体来寻找其他疾病靶标。显然,更小的体积使它们可以适应更小的间隙;不过,除了体积,独特的结构也功不可没:在传统抗体伸出的Y型手臂末端有手指状突起,作用是与分子靶标接触,但在纳米抗体中,这种抓手并不对称,其中一边突起比传统抗体更长,科学家们认为这使它们能够进一步进入目标分子表面的缝隙中,从而触及一些从未到达过的隐藏结合区域。
加州州立大学的Cory Brooks是一名结构生物学家,主要工作是使用晶体学来研究抗体与靶标结合过程中所涉及的分子结构。他的研究结果可以为纳米抗体的独到之处提供证明:当目标是病毒时(如HIV 和SARS-Cov-2),比较常规抗体和纳米抗体与相同靶标的结合情况,可见纳米抗体确实能与目标分子的隐藏部位接触。在Brooks看来,纳米抗体在治疗 Covid-19 等传染病、甚至在所有疾病领域都具有很大潜力。病毒所致的传染病可能是使用纳米抗体治疗的最佳靶标之一,特别是考虑到纳米抗体在骆驼科动物进化中可能扮演着“病毒中和剂”的角色。
怎样才能获得抗体?也许对一个大公司(比如赛诺菲)来说,建立一个骆驼农场的主意不错。但对于Lebeau这么一个一直把“免疫学无聊”挂在嘴边的人来说,鲨鱼是一种更有趣的选择。在新冠大流行暴发前不久,他已经在与苏格兰Elasmogen 公司的首席执行官 Caroline Barelle 接洽,该公司一直致力于收集鲨鱼的血液样本,以建立一个包含数十亿鲨鱼抗体的合成库,并正在寻找学术合作者,基于这个巨大合成库来研究癌症治疗。
两人第一次聊天后,LeBeau 就立即开始寻找鲨鱼缸;疫情出现后,他们一拍即合,开始了 Covid-19 中和抗体的研究。在检索了Elasmogen公司的合成文库后,他们发现了一些 Covid-19 刺突蛋白的结合剂,然后在明尼苏达州进行晶体学分析,探索它们的精细结合模式。正如 LeBeau 回忆的那样,这些基于结构的工作显示了微小的鲨鱼抗体正在做“疯狂的分子瑜伽”,以进入即使是美洲驼抗体也无法到达的刺突蛋白区域。在针对活病毒的测试中,他们的研究表明,这些来自鲨鱼的抗体在中和病毒方面可以与人类抗体的效果一样好,并且优于骆驼抗体。随着病毒的迅速发展,抗体研究很重要的方向之一是考察抗体对病毒变异株的抵抗力。在后续研究中,他们发现这些鲨鱼抗体对 Omicron 这类更具传染性的新冠病毒变异株非常有效!Omicron在去年11 月首现南非,它的刺突蛋白中包含至少30处突变。分子建模表明,即使刺突蛋白突变程度达95%,他们所研发的一种鲨鱼抗体仍然可以发挥作用。与人类体内笨重的 Covid-19 抗体相比,这些小身材的纳米抗体似乎具有优势。
人类抗体直接识别病毒与人类细胞接触的刺突蛋白区域,该区域始终处于适应和变异的压力之下。而鲨鱼抗体会深入刺突蛋白的更下方,进入 LeBeau 认为“从不变异”的区域——如果确实如此,那么这个区域就是高度保守的,这种保守性甚至可以追溯到2003年引起非典的SARS病毒。不仅如此,这个区域的保守性还可以延伸到其他来自野生动物的冠状病毒,也就是说,如果有朝一日那些不同于新冠病毒的其他病毒再次蔓延到人类身上,这类纳米抗体仍然可以发挥作用。
目前他们正在对动物进行实验以验证这个猜想,希望在人类遭遇下一次疫情之前,他们已经做好充足的准备。在这些惊人的进展发生之时,鲨鱼小子LeBeau仍在盯着鲨鱼缸。作为一名癌症研究人员,LeBeau似乎更加迷恋鲨鱼以及它们身上的奇妙抗体。用他的话说,“这些抗体看起来只是一些精巧的奇妙的蛋白质,但背后蕴藏的潜力却似乎无穷无尽。”2021年他来到威斯康星州,现在他正用癌症靶标对活鲨鱼进行免疫接种。他的同事们正在研究冠状病毒,而 Elasmogen 公司正在利用纳米抗体寻找针对关节炎和炎症性肠病的靶标。从治疗出血热到研发疫苗,这张由纳米抗体绘制成的宏伟画卷,正徐徐对我们展开。
编译来源
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 