在自身免疫性疾病中,女性患者占比高达78%,自身免疫病已成为育龄期女性的第五大主要死因。为什么自身免疫病会呈现出如此明显的性别差异?背后的生物学机制错综复杂,经过深入而广泛的研究,研究人员最终聚焦了三大主要因素——性激素、X染色体以及肠道菌群。
撰文 | 维罗妮卡(上海交通大学医学院附属瑞金医院)
01
自身免疫病群体中,近八成为女性患者
故事是从2005年开始的。那天,45岁的梅兰妮·西(Melanie See)在家中突然大汗淋漓,从卧室走到沙发的短短几步,她感到头晕目眩。非孕非哺乳期的她,乳房却意外泌乳,体重也在短时间内锐减4.5kg[1]。经过一系列细致检查,梅兰妮被诊断为Graves病(又称毒性弥漫性甲状腺肿)——一种高发于青年女性的自身免疫性甲状腺功能亢进症。
遵循医嘱规律服药治疗后,梅兰妮的症状逐渐得到控制。但三年后,她的健康状况再次恶化。她瘦得更厉害了,还感到疲惫异常。这次,她被诊断为乳糜泻(Celiac disease,又称麦胶性肠病)。这是另一种自身免疫病,患者因肠黏膜细胞酶活性不足,在食用含麸质食物(大麦、小麦等)后会出现腹痛、腹泻等症状。
时间推进至2015年,梅兰妮出现了更严重的腹痛、腹泻和肌肉疼痛。面对种种症状,医生们一度难以做出诊断。梅兰妮回忆道:“医生提出了很多种可能的诊断——血管炎、系统性红斑狼疮(systemic lupus erythematosus, SLE)等等,我也记不清了。我的血检结果不太正常,肌肉活检结果也有问题,但我不符合任何一个病的诊断标准。”经过多项化验检查,梅兰妮最终被诊断为混合性结缔组织病。这是一种罕见的自身免疫病,患者可同时具有SLE、硬皮病和皮肌炎的特征,但又不完全符合任一疾病的诊断标准。
梅兰妮的故事只是一个缩影,在她之外,还有无数饱受自身免疫性疾病困扰的女性。数据显示,在自身免疫病患者中,女性占比高达78%[2]。这类疾病涵盖广泛,包括SLE(83.7%)、干燥综合征(90.5%)、皮肌炎(65.1%)、系统性硬化症(83.8%)和类风湿性关节炎(73.4%)等[3],共同特点是患者免疫系统错误攻击自身细胞和组织。自身免疫病已赫然成为育龄期女性的第五大死因[4]。
为什么自身免疫病如此“青睐”女性?背后原因错综复杂,科学家们通过大量的研究,最终将焦点锁定在三大主要因素——性激素、X染色体与肠道菌群。此外,有学者提出,进化也在其中扮演了重要角色。胎儿和胎盘对女性身体而言是“外来物”,本应受到免疫系统的攻击。为了提高怀孕的成功率,女性进化出了高度可调节的免疫系统,代价便是自身免疫病风险的增加。
加拿大多伦多大学的免疫学家香农·邓恩(Shannon Dunn)在采访中说:“深入探究性别偏倚背后的生物学机制至关重要。解开这个谜团不仅能帮助我们理解自身免疫病的发病原因,还可能引领我们发现新的治疗策略,也有助于揭示机体在应对感染、疫苗接种、外伤和癌症中的性别差异。”
02
最早发现的元凶:性激素
早在19世纪,当自身免疫病首次进入公众视野时,医生们便观察到患者群体中女性占多数。然而,受限于当时的医学知识,医生普遍认为每种自身免疫病都具有其独特的病因。转折点发生于20世纪90年代初,科学家发现部分自身免疫病共享相似的生物学机制,并揭示CD4+辅助T细胞与类风湿关节炎、多发性硬化症和1型糖尿病等自身免疫病间存在关联。1991年,一名身患SLE的美国女性弗吉尼亚·拉德(Virginia Ladd)发现家族中有多人罹患自身免疫病。为探寻背后的机制,她创立了美国自身免疫相关性疾病协会(American Autoimmune Related Diseases Association),推动了该领域研究的快速发展。
此后,人们逐渐发现了这些疾病间的共同点:自身免疫病往往好发于处于特定生理阶段的女性。例如,SLE和多发性硬化症在育龄期女性中高发,而类风湿关节炎常见于绝经期妇女。在女性怀孕期间,类风湿关节炎、多发性硬化症和Graves病的症状常有所减轻,而SLE的症状往往会加重。青春期、妊娠期和更年期都是女性人生中的重要转折点,女性体内的雌激素、孕激素和雄激素水平会发生显著波动,影响免疫系统的功能。
雌激素作为女性体内最主要的性激素,已被证实与多种自身免疫病相关。口服避孕药和适用于绝经期女性的激素替代疗法都会提高雌激素水平,而这二者皆被证实与SLE的风险增加有关[5]。雌激素能直接影响一些免疫相关基因的表达,例如启动干扰素的基因表达。干扰素能够促进机体对外来病原体的免疫防御,但同时也可能诱发自身免疫反应。雌激素还能激活B淋巴细胞。B细胞的功能是分泌抗体,标记并攻击外来抗原,但部分B细胞会分泌自身抗体,攻击自身的细胞和组织。
孕激素在妊娠过程中起关键作用,同时也被证实参与免疫反应。许多免疫细胞表面都存在孕激素受体,包括T淋巴细胞和巨噬细胞,孕激素和受体的结合能促进Th2免疫反应。Th2免疫反应以体液免疫为主,通过抗体的分泌来抑制细胞外病原体。与之对应的是Th1免疫反应,以细胞免疫为主,活化后的CD8+ T细胞能直接杀伤被病原体入侵的细胞。前面提到,类风湿关节炎和多发性硬化症患者在怀孕时症状通常会减轻,是因为这两种自身免疫病属于Th1免疫反应,而妊娠期间孕激素水平的升高,会促进Th2免疫反应,抑制Th1免疫反应。
在女性体内,雄激素水平远低于男性。雄激素具有免疫抑制作用,能抑制多种免疫细胞的功能,包括中性粒细胞、自然杀伤细胞和巨噬细胞,在一定程度上降低了男性患自身免疫病的风险。研究发现,多发性硬化症的男性患者体内雄激素水平通常低于正常,而性腺功能减退(雄激素水平低下)的男性罹患SLE和类风湿关节炎的风险增加。
性激素对免疫系统的影响,可能与某些关键的免疫基因有关。1997年,芬兰和德国科学家联合(APECED联盟)发现了一个在自身免疫中起关键作用的基因——AIRE(Autoimmune Regulator, 自身免疫调节因子)[6],其表达于胸腺细胞,而胸腺是T细胞分裂、分化的场所。在AIRE的作用下,机体自身的抗原被呈递给发育中的T细胞,使得攻击自身抗原的那部分T细胞提前凋亡,以阻止自身免疫的发生。AIRE缺失或突变会增加自身免疫病的风险,因为攻击自身抗原的T细胞无法被清除。更重要的是,AIRE的基因表达受到性激素的调控。2016年的一项法国研究发现[7],在小鼠中,雌激素和孕激素会降低AIRE的表达,而雄激素则能增加AIRE表达量。在人类中,青春期后女性的AIRE蛋白表达量往往少于男性,这可能是由于性激素水平的影响。更少的AIRE意味着更多的自身反应性T细胞能够从胸腺中逃逸,并最终导致自身免疫性疾病。
尽管性激素起到了重要作用,但它并不能完全解释自身免疫病的性别偏倚。部分自身免疫病(例如SLE和多发性硬化症)也能发生于青春期前的女童,此时患者体内的性激素轴尚未完全建立,雌激素和孕激素水平仍较低。这意味着还有其他因素参与自身免疫病的发病,而且这种差异在生命的早期阶段便已存在。于是,研究人员把目光转向了两性间最本质的差异:性染色体。
03
X染色体带来的决定性差异
自受精卵形成之初,性染色体便已悄然布局,决定了个体的生理性别。正常男性核型为(46,XY),正常女性则为(46,XX)。男性独有的Y染色体上仅镶嵌着约100个基因,其中直接影响免疫系统活性的基因更是只有寥寥数个。相比之下,X染色体则是一座基因宝库,容纳了多达约1100个基因,其中约50个与免疫反应息息相关。事实上,X染色体中含有的免疫相关基因数量在所有染色体中位居榜首。
遗传学经典理论Lyon假说,揭示了雌性哺乳动物体细胞内X染色体的独特行为:尽管存在两条X染色体,但只有一条保持活性,从而实现X连锁基因的剂量补偿,保证雌雄个体拥有等量的X连锁基因产物;这种X染色体的失活(X chromosome inactivation, XCI)过程在胚胎发育的早期随机发生,某些细胞中来自父亲的X染色体失活,而其他细胞中则是来自母亲的X染色体失活,两类细胞镶嵌存在。但近年来有研究表明,失活的X染色体上有15%-23%的基因仍处于激活状态(又称XCI逃逸)[3],使得女性体内这部分基因所表达的蛋白质数量达到男性的两倍。在女性SLE患者中,病情严重者体内XCI逃逸的基因数量更多。
多项研究表明,许多X连锁基因与自身免疫病直接相关。其中一个典型代表是toll样受体7(Toll-like receptor-7, TLR-7)基因,其与SLE、皮肌炎、硬皮病和干燥综合征等自身免疫病关系密切。TLR-7能够识别病原体,并促进干扰素的产生。研究发现,女性儿童SLE患者中TLR-7的蛋白表达水平显著升高[8]。与之相似的是TASL(TLR adaptor interacting with SLC15A4 on the lysosome)基因,它是TLR信号通路上的接头蛋白。TASL也是常见的XCI逃逸基因,它的激活能使干扰素的产量翻倍。研究发现,SLE患者体内的淋巴母细胞中TASL存在过表达[9]。也就是说,女性内体本来应该失活的染色体造成了过度的基因表达,而这可能与自身免疫病的发生有关。
近年来,科学家们逐渐了解XCI逃逸在自身免疫病发病机制中的重要作用。2019年,美国宾夕法尼亚大学的生物学家蒙特塞拉特·安格拉(Montserrat Anguera)团队发现,雌性小鼠体内的幼稚免疫细胞在成熟过程中,失活的X染色体会发生显著变化,使得本应沉默的X连锁基因容易发生逃逸[10]。这一发现首次揭示了女性免疫细胞中XCI机制的特殊性。在小鼠体内有了重大发现后,2021年,安格拉发表了基于人类患者的数据[11]。单细胞转录组测序结果显示,与正常女性相比,儿童和成年的女性SLE患者的B细胞内X染色体失活相关的表观遗传学修饰明显减少,可能导致X连锁基因的蛋白表达量显著增加。
对于X染色体数量异常的患者,自身免疫病的发病率会不会受到影响呢?答案是肯定的。 Klinefelter综合征患者的生理性别为男性,但染色体核型为(47,XXY),即比正常男性多了一条X染色体。研究表明,他们患SLE的风险是正常男性的18.1倍[12]。而X三体综合征患者生理性别为女性,染色体核型为(47,XXX),拥有三条X染色体的她们患SLE和干燥综合征的风险分别是正常女性的2.5倍和2.9倍[13]。Turner综合征患者的染色体核型为(45,XO),其生理性别为女性,但缺少一条X染色体。值得注意的是,Turner综合征患者罹患自身免疫病的风险高于正常女性[14],但发病率最高的并非常见于女性的SLE、皮肌炎等疾病,而是通常见于男性患者的自身免疫病(反应性关节炎、强直性脊柱炎等)。
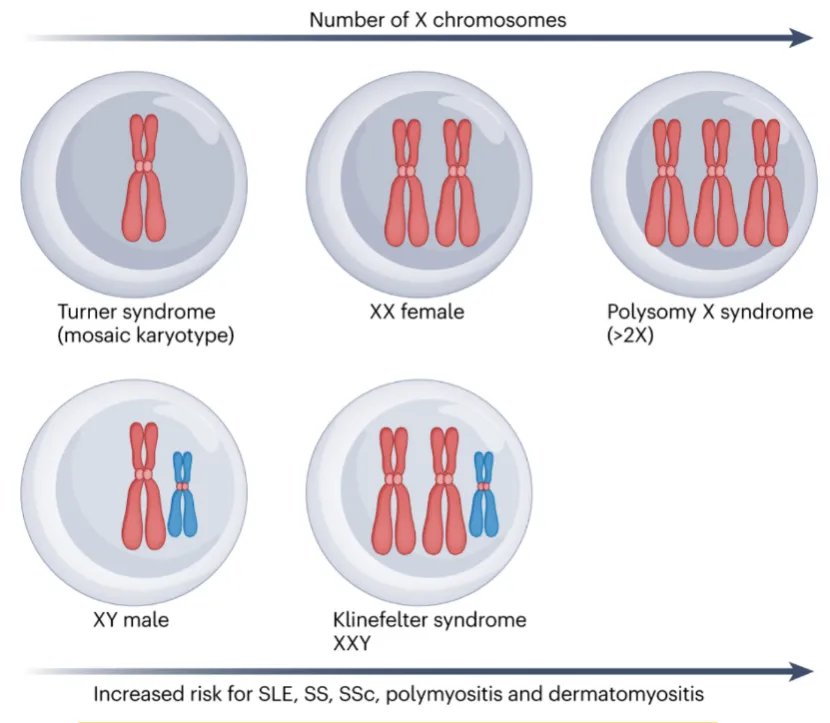
图1. 性染色体数量与自身免疫病风险。患有Klinefelter综合征(XXY)或X多体综合征(>2X)的个体中,X染色体数量增加与女性偏倚性自身免疫病系统性红斑狼疮(SLE)、干燥综合征(SS)、系统性硬化症(SSc)、多发性肌炎(polymyositis)和皮肌炎(dermatomyositis)的风险增加相关。然而,要证明这种相关性背后的因果性,仍需直接证据,例如识别X染色体上特定基因的剂量效应,并通过动物模型或细胞功能实验证实这些基因的过表达足以驱动自身免疫反应。| 图源:参考文献 [3]
面对XCI逃逸机制增加女性患自身免疫病风险的事实,不禁令人思考:这种看似不利的机制为什么会在进化过程中得以保留?从进化论的角度分析,只有能适应环境的有利变异才会被自然选择所保留,据此推测,XCI逃逸对女性而言也应该存在有利的一面。
在2019年《遗传学趋势》(Trends In Genetics)期刊上的一篇论文中,美国进化生物学家梅丽莎·威尔逊(Melissa Wilson)系统阐述了“怀孕补偿假说”(pregnancy compensation hypothesis)[15]。该假说认为,两性间免疫功能的差异是为了适应妊娠过程,该差异由性染色体上基因表达的内容和数量介导,且性激素参与调控。在怀孕期间,胎儿的存在给女性的免疫系统带来了极大的挑战。因为胎儿的DNA有一半来自父亲,这种外源性物质会遭到母亲免疫细胞的攻击。女性的免疫力在怀孕期间呈动态变化:在孕早期,免疫反应的增强有助于胎盘中新生血管的形成;在孕中期,免疫反应的减弱能促进女性对胎儿及胎盘的耐受;在临产前,免疫和炎症反应再次增强,以帮助身体适应生产过程。XCI逃逸机制的存在,使女性的免疫系统能根据妊娠需要做出灵活的调节。
威尔逊文中指出,与数百年前相比,现代工业社会中女性的怀孕、分娩次数显著减少,这一变化导致女性生命过程中免疫系统受抑制的时间大幅缩短,进一步加剧了自身免疫病在性别间的差异。相应的,与农业社会时期相比,自身免疫病在女性中的发病率呈现显著上升趋势。从某种程度上说,自身免疫病可能是女性生育所需的复杂免疫调节带来的不幸副产品。
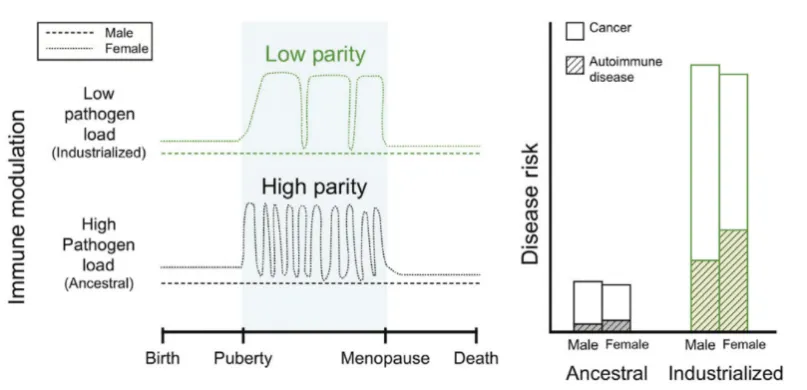
图2 工业社会与古代社会两性间免疫力与疾病风险对比。古代(ancestral)社会中,病原体负荷高(high pathogen load),女性生产次数多(high parity),而工业(industrialized)社会中则相反。低病原体负荷会同时影响男性和女性的免疫功能,导致自身免疫病(autoimmune disease)风险的升高,而低产次只影响女性的免疫系统,加剧自身免疫病在性别间的差异。| 图源:参考文献 [15]
04
肠道菌群:研究过程中的意外发现
基因虽是生命的蓝图,但并非决定人体特征的唯一因素,实际情况远比这要复杂。同卵双胞胎中,一人罹患自身免疫病,而具有相同遗传物质的另一人却不一定会患病,这表明环境因素在疾病发展过程中扮演了重要角色。可能与自身免疫病相关的环境因素有很多,目前的研究涉及微生物感染、化学品暴露、吸烟习惯、饮食结构、心理压力和肠道菌群等多个方面。其中,关于肠道菌群的证据日益增多,动物研究已初步证实肠道细菌是自身免疫病的重要驱动因素。
杰恩·丹斯卡(Jayne Danska)是加拿大多伦多大学的免疫学家,长期致力于研究自身免疫病相关基因的性别差异。2012年的一次偶然发现,让她意识到除了基因以外,环境因素——尤其是肠道菌群——同样也对自身免疫病的性别差异起着重要影响。她感慨道:“科学界常言,最重大的发现往往源于无意之举。”
彼时,杰恩正致力于寻找1型糖尿病的致病基因。1型糖尿病也是一种自身免疫病,患者体内存在能攻击胰岛β细胞的抗体,抑制胰岛素的产生,并且在人类患者中1型糖尿病的发病率不存在明显的性别差异。他们使用非肥胖糖尿病 (nonobese diabetic, NOD) 小鼠作为疾病模型,他们惊讶地发现,雌性NOD小鼠的患病风险却是雄性小鼠的两倍。
杰恩怀疑小鼠中肠道菌群的差异可能与糖尿病的性别差异有关,因此在无菌环境中培育了一组NOD小鼠,这组小鼠体内不存在任何细菌或病毒,包括肠道内的共生细菌。结果令人震惊:无菌NOD小鼠成年后,雄性小鼠和雌性小鼠的糖尿病发病率几乎相等。“性别差异竟然完全消失了,”她回忆道,“这是一个我们没有预料到的重大发现,我简直不敢相信这是真的。”但结果得到了重复实验的验证。随后,他们又提取了成年雄性NOD小鼠的肠道菌群,植入尚未发病的年轻雌性NOD小鼠体内,这批雌性小鼠最终健康成长,未患糖尿病。
杰恩的这项开创性研究于2013年发表于《科学》(Science)期刊上,首次证实肠道菌群可以影响自身免疫病的性别偏倚[16]。尽管雄性小鼠肠道菌群对1型糖尿病的保护机制仍待深入探索,但杰恩发现雄激素在其中起到重要作用。血液检测显示,无菌雄性NOD小鼠体内的雄激素水平低于普通雄性NOD小鼠,而接受雄鼠肠道菌群移植的无菌雌性NOD小鼠体内雄激素高于普通雌性NOD小鼠。此后,杰恩再次将成年雄性NOD小鼠的肠道菌群植入无菌雌性NOD小鼠,并阻断雌鼠体内的雄激素信号通路,这时雌鼠患1型糖尿病的风险与阻断信号通路前相比显著增加。这一结果与早期一项基于男性SLE患者的研究相符,该研究表明抑制雄激素通路会增加男性患者的SLE发病风险[17]。
目前尚不清楚肠道菌群是如何调节雄激素水平的,反之亦然。在青春期前后,雄性和雌性小鼠的肠道菌群组成会发生变化,显示出性别差异。这或许可以解释为什么1型糖尿病在人类中的患病率没有明显性别差异,因为它通常发生在青春期前,肠道菌群尚未发生变化。肠道菌群的变化可能受到青春期性激素水平剧烈波动的影响,但这种影响应当是双向性的,即性激素水平与肠道菌群的组成能够互相影响。
尽管从小鼠中得到的结论不一定适用于人,但杰恩的研究仍然具有深远意义。它提示我们,女性体内的肠道菌群可能对自身免疫病的发展至关重要,改变肠道菌群的组成结构或许能预防疾病发生。未来,也许科学家们会开发出针对自身免疫病高风险女性人群的靶向微生物疗法,通过塑造肠道菌群,将致病因素转化为保护因素。此前,研究多聚焦于通过调节性激素水平来降低自身免疫病风险。随着对女性易患自身免疫病的原因的深入理解,我们有望在疾病发生前进行有效干预。
05
小 结
综上所述,性激素、X染色体和肠道菌群共同增加了女性患自身免疫病的风险,人们可能会因此认为生物学对女性太不公平。但这种疾病负担其实也可以从另一个角度来理解:它反映了女性对人类生存的重要贡献。自身免疫病或许是女性为人类的生存繁衍被迫付出的代价,但我们期盼有朝一日,科学能最终找到消除这份代价的途径。
参考文献
[1] Moyer, MW. (2021). Why nearly 80 percent of autoimmune sufferers are female. Scientific American. https://www.scientificamerican.com/article/why-nearly-80-percent-of-autoimmune-sufferers-are-female/
[2] Fairweather, D. (2004). Women and autoimmune diseases. Emerging infectious diseases, 10(11): 2005–2011.
[3] Forsyth, KS. (2024). The conneXion between sex and immune responses. Nature Reviews Immunology, 24(7):487–502.
[4] Zandman-Goddard, G. (2007). Gender and autoimmunity. Autoimmunity reviews, 6(6): 366–372.
[5] Cui ,J. (2023). Risk prediction models for incident systemic lupus erythematosus among women in the Nurses' health study cohorts using genetics, family history, and lifestyle and environmental factors. Seminars in Arthritis and Rheumatism, 58:152143.
[6] Finnish-German APECED Consortium (1997). An autoimmune disease, APECED, caused by mutations in a novel gene featuring two PHD-type zinc-finger domains. Nature Genetics, 17(4):399-403.
[7] Dragin, N. (2016). Estrogen-mediated downregulation of AIRE influences sexual dimorphism in autoimmune diseases. Journal of Clinical Investigation, 126(4):1525-37.
[8] García-Ortiz, H. (2010). Association of TLR7 copy number variation with susceptibility to childhood-onset systemic lupus erythematosus in Mexican population. Annals of the Rheumatic Diseases, 69(10):1861-5.
[9] Harris, VM. (2019). Characterization of cxorf21 Provides Molecular Insight Into Female-Bias Immune Response in SLE Pathogenesis. Frontiers in Immunology, 10:2160.
[10] Syrett, CM. (2019). Altered X-chromosome inactivation in T cells may promote sex-biased autoimmune diseases. JCI Insight, 4(7).
[11] Pyfrom, S. (2021). The dynamic epigenetic regulation of the inactive X chromosome in healthy human B cells is dysregulated in lupus patients. Proceedings of the National Academy of Sciences of the United States of America, 118(24).
[12] Seminog, OO. (2015). Associations between Klinefelter's syndrome and autoimmune diseases: English national record linkage studies. Autoimmunity, 48(2):125-8.
[13] Sharma, R. (2017). Rare X Chromosome Abnormalities in Systemic Lupus Erythematosus and Sjögren's Syndrome. Arthritis & Rheumatology, 69(11):2187-2192.
[14] Jørgensen, KT. (2010). Autoimmune diseases in women with Turner's syndrome. Arthritis and Rheumatism, 62(3):658-66.
[15] Natri, H. (2019). The Pregnancy Pickle: Evolved Immune Compensation Due to Pregnancy Underlies Sex Differences in Human Diseases. Trends in Genetics, 35(7):478-488.
[16] Markle, JG. (2013). Sex differences in the gut microbiome drive hormone-dependent regulation of autoimmunity. Science, 339(6123):1084-8.
[17] Sequeira, JF. (1993). Systemic lupus erythematosus: sex hormones in male patients. Lupus, 2(5):315-7.
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 